Clear Sky Science · fr
Inhibition de l’internalisation du récepteur des cellules B (BCR) induite par l’autoantigène comme stratégie thérapeutique dans le lymphome diffus à grandes cellules B (LDGCB)
Pourquoi cela compte pour les patients
Le lymphome diffus à grandes cellules B (LDGCB) est le cancer du sang à croissance rapide le plus fréquent chez l’adulte, et de nombreux patients rechutent après la chimio‑immunothérapie standard. Cette étude explore une vulnérabilité surprenante dans un sous‑groupe majeur de ces tumeurs : leur dépendance à une antenne de surface cellulaire appelée récepteur des cellules B (BCR). En montrant que bloquer la manière dont cette antenne est internalisée peut compromettre la survie des cellules cancéreuses, le travail ouvre la voie au repositionnement de médicaments anti‑nausée et antipsychotiques anciens comme adjuvants ciblés contre le lymphome.
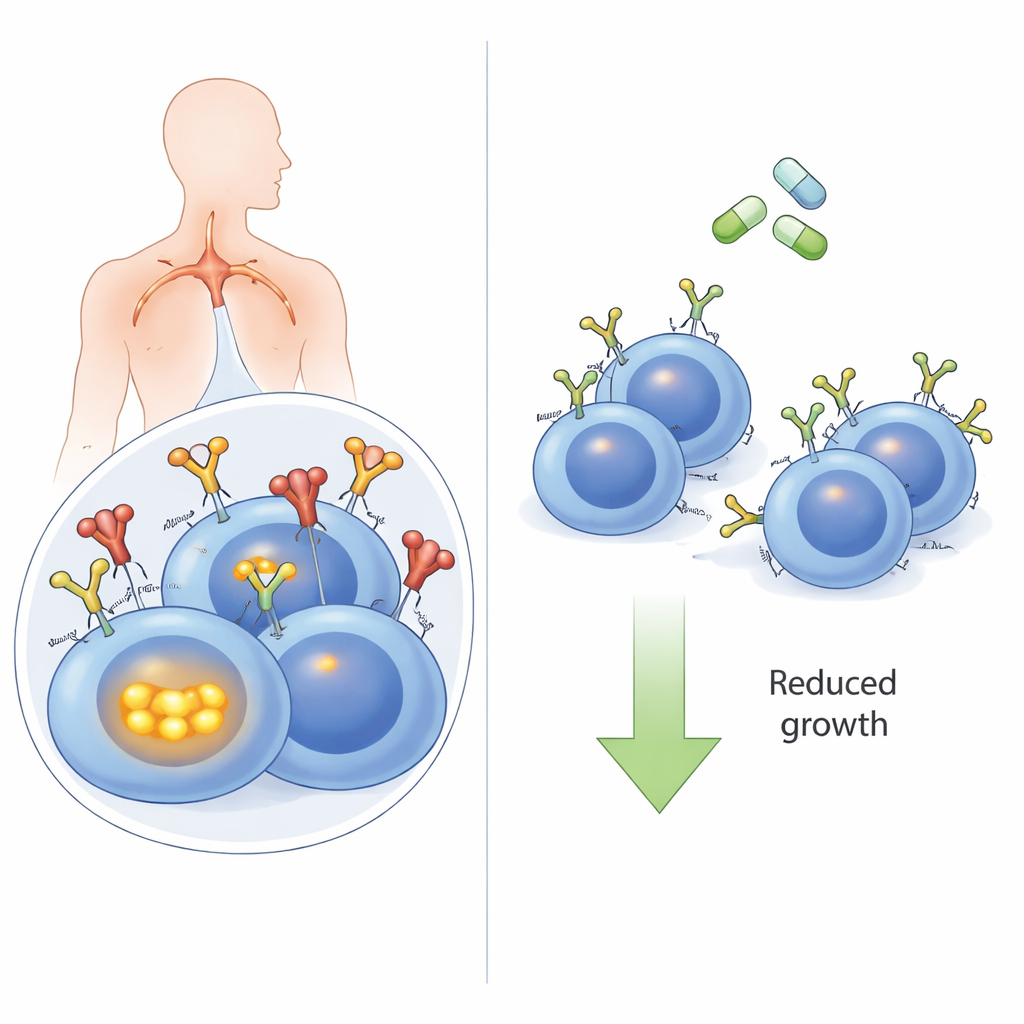
L’antenne de la cellule cancéreuse
Les cellules B, un type de globules blancs, utilisent le récepteur des cellules B à leur surface pour reconnaître les menaces. Dans de nombreux LDGCB, en particulier le sous‑type « cellules B activées » (ABC) à haut risque, ce même récepteur est détourné pour envoyer en continu des messages « reste en vie et prolifère ». Souvent, ces BCR reconnaissent les propres molécules de l’organisme (autoantigènes), qui agissent comme une sonnette coincée. Lorsque les autoantigènes se lient, le BCR ne se contente pas de signaler à la surface : il est entraîné à l’intérieur de la cellule et rejoint un complexe protéique interne contenant des senseurs tels que TLR9 et MYD88. Ce super‑complexe active alors NFκB, une voie de signalisation puissante favorisant la croissance. Jusqu’ici, on ignorait si ce trajet vers l’intérieur du récepteur était réellement nécessaire aux signaux oncogéniques.
Reprogrammer l’antenne pour tester ses limites
Pour répondre à cette question, les chercheurs ont utilisé l’édition génique CRISPR pour modifier précisément les « pointes » du BCR dans des lignées de lymphome. Ils ont remplacé les régions de reconnaissance naturelles, autoréactives, par des versions reconnaissant l’ovalbumine, une protéine d’œuf inoffensive utilisée comme outil en laboratoire. Ces récepteurs modifiés ne captaient plus leurs autoantigènes habituels, mais pouvaient néanmoins être activés de façon contrôlée par ajout d’ovalbumine. Dans des cellules de lymphome de type ABC qui dépendent normalement de la liaison à des autoantigènes, ce remplacement a fortement réduit l’activité de nombreuses enzymes de signalisation clés et atténué les gènes répondant à NFκB. Les cellules proliféraient plus lentement, malgré une augmentation du nombre de BCR à leur surface, ce qui montre que l’engagement continu par des autoantigènes et la signalisation interne qui s’ensuit sont essentiels à leur survie.
Internalisation des récepteurs : une étape cruciale
L’équipe a ensuite observé directement ce qui arrive au BCR après sa rencontre avec l’antigène. Dans leurs modèles ingénierés, aussi bien des déclencheurs à base d’anticorps que l’ovalbumine ont provoqué la disparition du récepteur de la surface cellulaire en quelques minutes, confirmant une internalisation rapide. Cela s’est produit non seulement quand l’antigène était flottant à l’extérieur de la cellule, mais aussi lorsqu’il était affiché artificiellement sur la membrane de la même cellule, mimant certaines situations réelles de tumeur. Bloquer ce trafic vers l’intérieur génétiquement, en utilisant une forme dominante‑négative d’une protéine appelée dynamine‑2, essentielle à l’endocytose dépendante de la clathrine, a maintenu le BCR à la surface, réduit les complexes internes BCR–TLR9–NFκB, diminué les gènes cibles de NFκB et ralenti la croissance cellulaire. Fait intéressant, lorsque l’endocytose était bloquée, certains signaux « de fond » du BCR à la surface augmentaient, suggérant que les cellules cancéreuses tenteraient de compenser en renforçant un mode de signalisation tonique, plus faible.
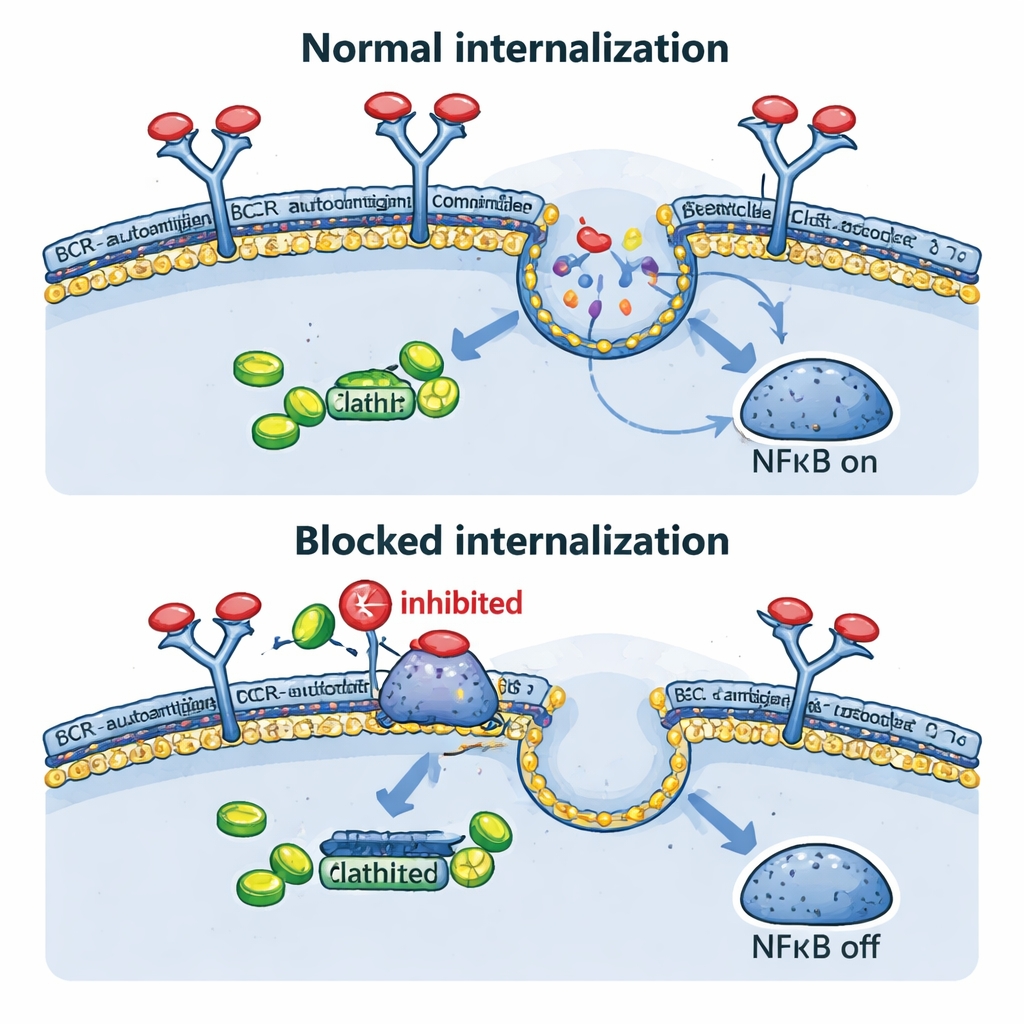
Anciens médicaments, nouvelles idées
Parce que développer de nouveaux médicaments est long et coûteux, les auteurs ont ensuite testé si des médicaments existants qui inhibent l’endocytose pouvaient reproduire les expériences génétiques. Les phénothiazines, une famille de médicaments antipsychotiques et anti‑nauséeux, sont connues pour inhiber la dynamine‑2 et l’absorption dépendante de la clathrine des récepteurs. Dans les cellules de lymphome, des composés comme le prochlorpérazine et la chlorpromazine ont augmenté les niveaux de BCR à la surface et fortement réduit l’internalisation induite par l’antigène. Cela a entraîné une baisse de l’activité des gènes sous contrôle de NFκB et une diminution de la viabilité des cellules LDGCB de type ABC, en particulier celles avec des composants BCR intacts. Chez des souris porteuses de greffes de lymphome humain, le prochlorpérazine à des doses cliniquement réalisables a ralenti de manière significative la croissance tumorale. De plus, l’association des phénothiazines avec des inhibiteurs d’autres enzymes liées au BCR, comme SYK et PI3Kδ, a produit des effets cytotoxiques plus puissants que chaque traitement pris séparément.
Ce que cela pourrait signifier pour le traitement
Dans l’ensemble, l’étude montre que pour un sous‑groupe substantiel de LDGCB, les signaux oncogéniques ne proviennent pas simplement de récepteurs à la surface cellulaire : ils dépendent de manière critique de l’internalisation du complexe BCR–antigène via une voie d’endocytose spécifique. Interrompre cette étape — soit par des manipulations génétiques, soit par des phénothiazines — affaiblit la signalisation NFκB et compromet la survie des cellules tumorales, tout en potentiellement sensibilisant les cellules aux inhibiteurs existants de la voie BCR. Comme les phénothiazines ont déjà des schémas posologiques et des profils de sécurité bien connus en tant qu’anti‑nauséeux, ce travail fournit une feuille de route réaliste pour des essais cliniques les testant, seuls ou en combinaison, chez des patients dont les lymphomes présentent une activité BCR dépendante d’autoantigènes.
Citation: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
Mots-clés: lymphome diffus à grandes cellules B, récepteur des cellules B, endocytose, phénothiazines, signalisation NFkB