Clear Sky Science · fr
Analyse multi-omique temporelle de l’exposition au paclitaxel dans des neurones sensoriels humains dérivés de cellules iPSC dévoile les mécanismes de la neuropathie périphérique induite par la chimiothérapie
Pourquoi certains médicaments anticancéreux endommagent les nerfs
La chimiothérapie a permis à des millions de personnes de survivre au cancer, mais de nombreux patients en paient le prix caché : des mois ou des années de douleur brûlante, de picotements et d’engourdissements dans les mains et les pieds. Cette étude pose une question simple mais importante : que fait exactement le paclitaxel, un médicament anticancéreux largement utilisé, aux cellules nerveuses sensorielles humaines, et la compréhension de ces changements peut‑elle indiquer des pistes pour mieux prévenir et traiter ces lésions nerveuses ?
Des cellules de patients aux nerfs sensoriels cultivés en laboratoire
Plutôt que de s’appuyer sur des expériences animales, les chercheurs ont commencé avec des cellules provenant de cinq donneurs humains, y compris des patientes atteintes d’un cancer du sein ayant reçu du paclitaxel. Ils ont reprogrammés ces cellules en cellules souches pluripotentes induites (iPSC) puis les ont guidées pour devenir des neurones sensoriels — le même type de cellule nerveuse qui transmet les sensations de toucher et de douleur de la peau vers la moelle épinière. Ces neurones cultivés en laboratoire ont formé de longs fibres délicates et ont montré une activité électrique proche de celle des véritables nerfs sensitifs. L’équipe les a ensuite exposés à des doses croissantes de paclitaxel, reproduisant les concentrations observées chez les patients, et a suivi la santé cellulaire sur plusieurs jours. À faibles concentrations, les neurones ont bien tenu le coup, mais à une dose cliniquement pertinente (100 nM) leur survie a commencé à chuter au bout d’environ deux jours, marquant le début d’un dommage nerveux toxique.
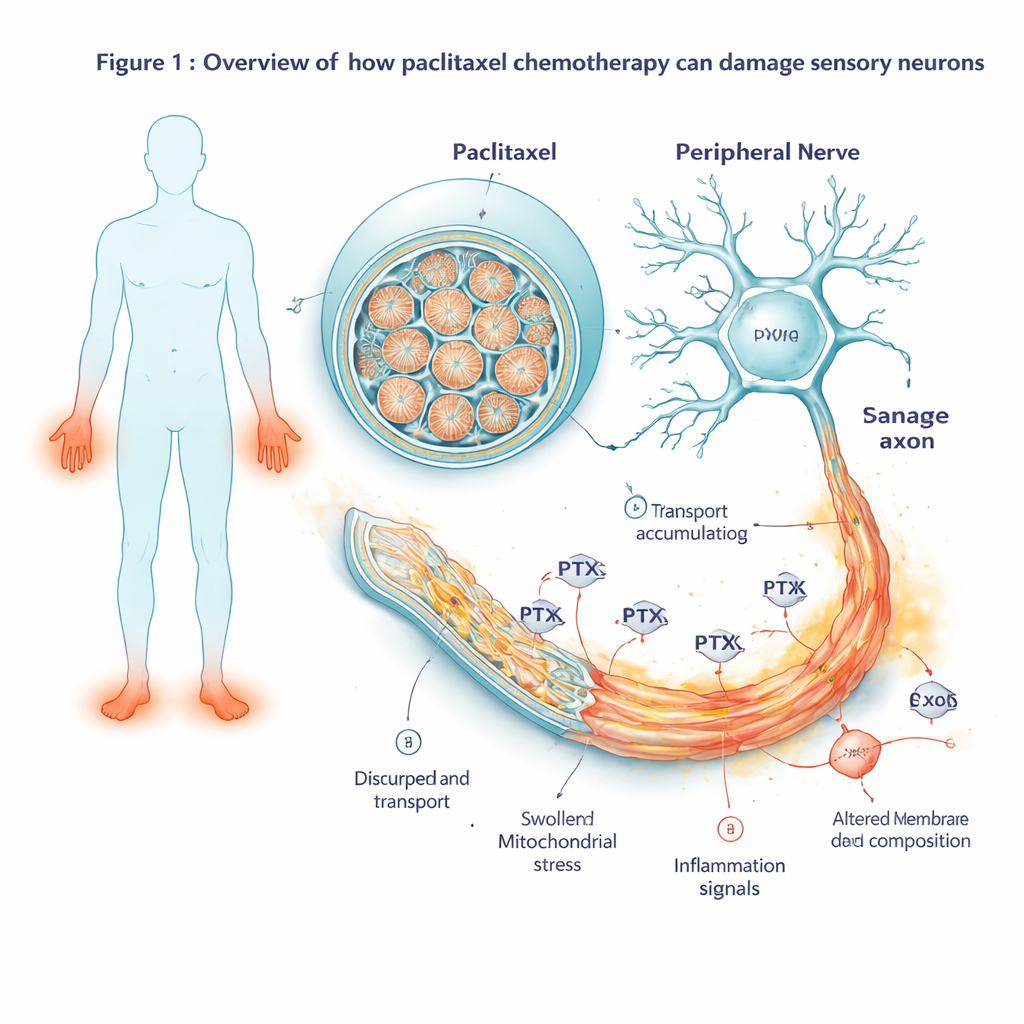
Observer l’évolution de l’activité génétique dans le temps
Pour voir comment les cellules réagissaient avant leur détérioration visible, les scientifiques ont mesuré quels gènes s’activaient ou s’éteignaient à plusieurs moments, de deux heures après l’exposition au médicament jusqu’à plusieurs jours après son élimination. Au début, ils ont observé l’activation d’un programme de stress cellulaire classique centré sur un gène appelé JUN. À mesure que l’exposition se poursuivait, ce signal de stress s’est étendu en une véritable cascade d’auto‑destruction : les gènes favorisant la mort cellulaire programmée étaient fortement activés, tandis que les partenaires protecteurs étaient submergés. Parallèlement, les gènes liés à l’inflammation et à la transmission de la douleur sont devenus plus actifs. Les neurones ont commencé à produire davantage de messagers inflammatoires, de peptides liés à la douleur et de récepteurs rendant les cellules plus sensibles aux stimuli nocifs, des changements qui reflètent ce que l’on observe dans les troubles nerveux douloureux.
Examen approfondi des protéines et des lipides à l’intérieur des neurones
Puisque les gènes ne sont que des plans, l’équipe a également examiné les protéines réellement présentes dans les neurones, ainsi que leur composition en lipides (graisses). Après 48 heures d’exposition au paclitaxel, de nombreux signaux de stress et d’inflammation détectés au niveau de l’ARN se sont aussi retrouvés au niveau protéique, confirmant que les neurones mettaient en œuvre ces programmes nocifs. De façon frappante, les protéines nécessaires au transport axonal — les moteurs moléculaires et les échafaudages qui déplacent les cargaisons le long des longues fibres nerveuses — étaient fortement réduites. Cela inclut des kinésines et des protéines régulatrices qui stabilisent les rails de microtubules. Au niveau lipidique, les neurones ont montré une baisse des éléments constitutifs clés du cholestérol et des lipides membranaires, parallèlement à une augmentation des graisses stockées appelées triacylglycérols. Ensemble, ces changements suggèrent que le paclitaxel ne déclenche pas seulement des voies de mort cellulaire, mais affaiblit aussi la structure physique et l’équilibre énergétique des fibres nerveuses.
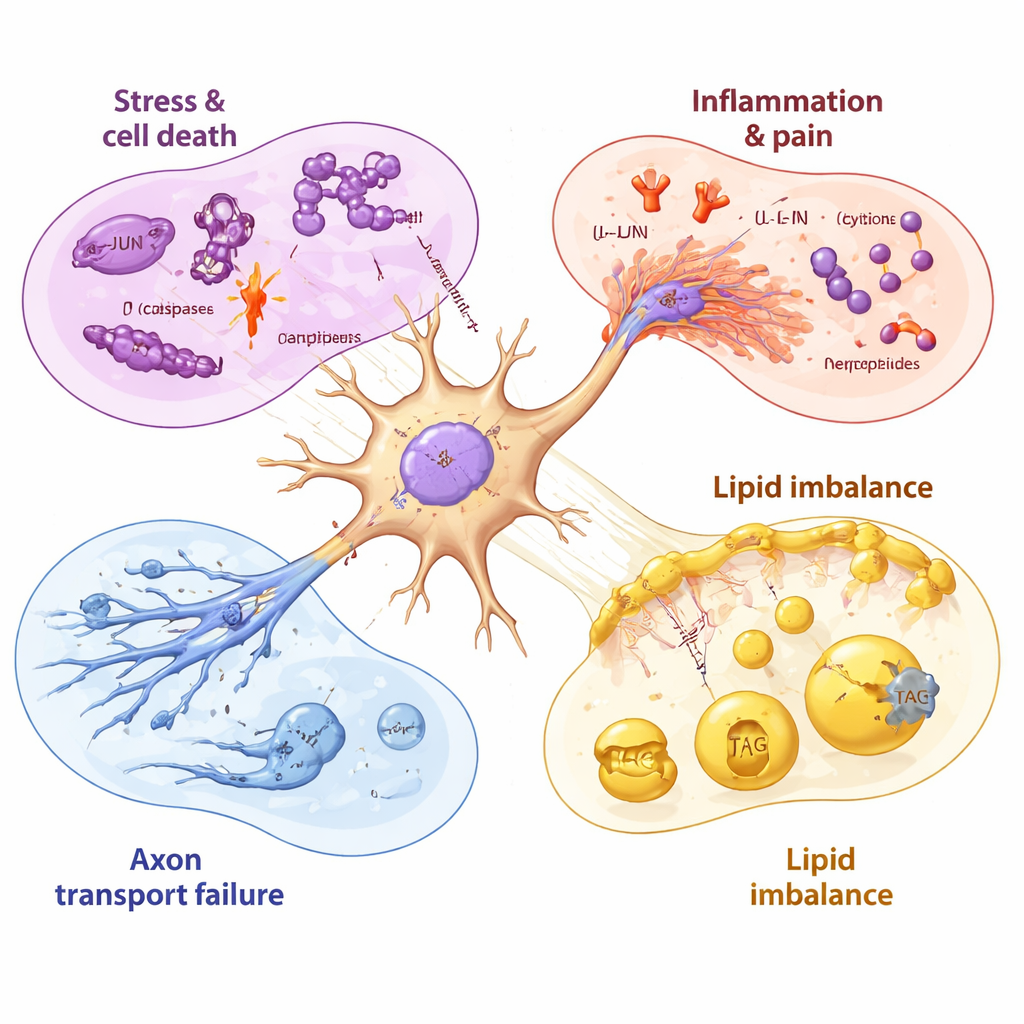
Une chronologie des blessures nerveuses et d’une récupération incomplète
En échantillonnant les neurones avant, pendant et après l’exposition au médicament, les chercheurs ont pu ordonner ces événements dans le temps. Les gènes mitochondriaux (liés à l’énergie) ont été perturbés en quelques heures, suivis par le gène de stress JUN, puis par une activation plus marquée des programmes de mort cellulaire et d’inflammation lorsque la viabilité a commencé à chuter. Même après le retrait du paclitaxel, de nombreux signaux nocifs sont restés élevés pendant des jours, tandis que les gènes nécessaires à la fabrication de lipides membranaires sains continuaient de décliner. Quelques molécules apparaissant tardivement, comme une pompe d’efflux de médicaments pouvant expulser le paclitaxel et certains facteurs de croissance, laissaient entendre que les neurones tentaient de se protéger et de se réparer — mais ces réponses semblaient relativement lentes et incomplètes comparées à la poussée rapide et précoce vers les dommages.
Ce que cela signifie pour les patients vivant avec des douleurs nerveuses
Pour un non‑spécialiste, le message est que le paclitaxel nuit aux nerfs sensoriels par une série coordonnée d’atteintes : il perturbe leurs systèmes énergétiques, déclenche des bascules génétiques vers la mort cellulaire, stimule l’inflammation et la transmission de la douleur, perturbe les « autoroutes » internes de transport dans les fibres nerveuses et modifie les lipides qui stabilisent les membranes nerveuses. En cartographiant ces changements dans des neurones d’origine humaine avec une grande finesse, l’étude met en évidence des cibles concrètes et pharmacologiquement accessibles — comme des régulateurs du stress spécifiques, des récepteurs inflammatoires et des enzymes de synthèse lipidique — qui pourraient être bloquées ou soutenues pour protéger les nerfs sans affaiblir le traitement du cancer. Bien que de nouveaux traitements nécessitent des tests supplémentaires, ce travail offre une feuille de route plus claire pour prévenir ou atténuer les lésions nerveuses induites par la chimiothérapie, améliorant ainsi la qualité de vie des survivants du cancer.
Citation: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
Mots-clés: neuropathie périphérique induite par la chimiothérapie, paclitaxel, neurones sensoriels, neuroinflammation, dégénérescence axonale