Clear Sky Science · fr
La méthylation réversible de l’arginine régule l’activité mitochondriale d’IDH2 : contrôle coordonné par CARM1 et KDM3A/4A
Régler finement les centrales énergétiques de la cellule
Les mitochondries, souvent qualifiées de centrales énergétiques de nos cellules, font bien plus que produire de l’énergie. Elles ajustent en permanence la façon dont elles brûlent les carburants pour répondre aux besoins de l’organisme, et lorsqu’elles fonctionnent mal cela peut contribuer à des maladies comme le diabète, l’insuffisance cardiaque ou le cancer. Cette étude met au jour un « variateur » caché à l’intérieur des mitochondries : une petite marque chimique sur un seul résidu d’un enzyme clé, IDH2, qui aide à décider si les mitochondries tournent au ralenti ou augmentent leur production d’énergie.
Une petite marque aux grandes conséquences
Les protéines de nos cellules ne sont pas statiques ; elles subissent fréquemment de petites modifications chimiques qui modulent leur comportement. Alors que de nombreuses modifications dans le noyau et le cytosol sont bien connues, celles qui se produisent à l’intérieur des mitochondries sont moins explorées. Les auteurs se sont intéressés à un type particulier de marque appelé méthylation de l’arginine et ont demandé si elle pouvait contrôler l’activité des enzymes mitochondriales. Ils se sont concentrés sur l’enzyme IDH2, un acteur central du cycle de l’acide tricarboxylique (TCA), qui aide à transformer les nutriments en énergie et en éléments de construction métaboliques importants. Grâce à des outils biochimiques et à la spectrométrie de masse, ils ont découvert qu’IDH2 porte une marque de méthylation sur un acide aminé précis, l’arginine 188, et que cette marque est apposée par une enzyme appelée CARM1 qui, de manière surprenante, agit à l’intérieur des mitochondries.
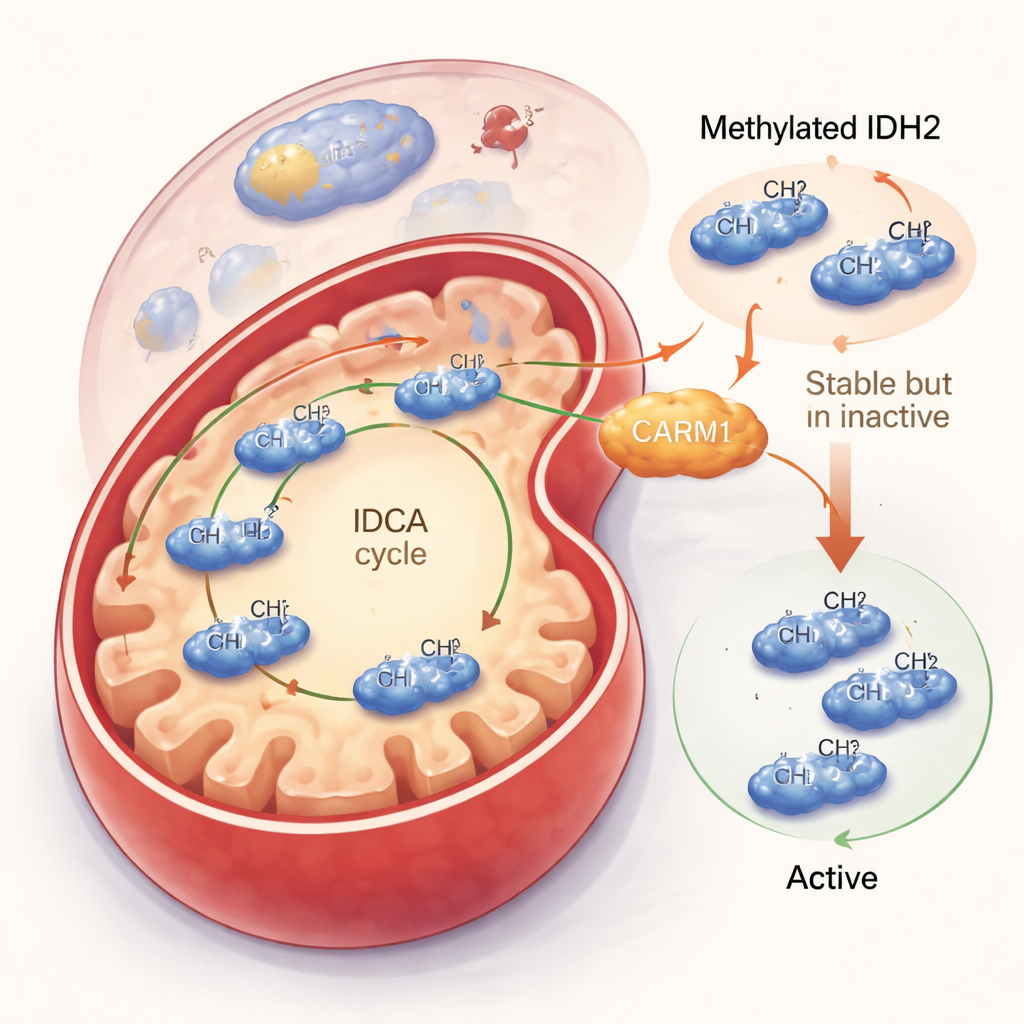
Diminuer l’activité d’IDH2 tout en prolongeant sa durée de vie
L’équipe a ensuite cherché à savoir ce que fait réellement cette marque méthyl. Lorsque CARM1 est actif et peut méthyler IDH2, la protéine IDH2 devient plus stable et persiste plus longtemps dans la cellule. Mais cet avantage apparent s’accompagne d’un compromis : l’IDH2 méthylé est moins actif. Dans des expériences cellulaires et sur protéine purifiée, l’IDH2 méthylé produisait moins de son produit principal, l’alpha‑céto‑glutarate, et générait moins de la molécule protectrice NADPH. En revanche, une version d’IDH2 qui ne peut pas être méthylée en l’arginine 188 favorisait la formation de son dimère actif, fonctionnait plus rapidement et augmentait à la fois les niveaux d’alpha‑céto‑glutarate et de NADPH. Même si la quantité totale de cet IDH2 non méthylé était moindre, chaque molécule travaillait davantage, conduisant à une augmentation nette de la production mitochondriale.
Un interrupteur réversible avec deux effaceurs
Fait crucial, cette marque de méthylation n’est pas permanente. Les chercheurs ont montré que deux enzymes connues pour enlever un autre type de marque, les déméthylases des lysines KDM3A et KDM4A, peuvent aussi effacer la méthylation de l’arginine sur IDH2. Lorsque ces déméthylases sont présentes, l’arginine méthylée en position 188 perd ses groupes chimiques additionnels, IDH2 devient moins stable mais plus actif, et sa forme dimérique augmente. Les cellules exprimant davantage de KDM3A ou KDM4A présentaient un potentiel de membrane mitochondriale plus élevé et consommaient plus d’oxygène, signes d’un métabolisme oxydatif plus intense. Lorsque ces enzymes étaient réduites, l’effet inverse s’observait : l’activité d’IDH2 diminuait et la performance mitochondriale déclinait, ce qui souligne qu’il s’agit d’un système de contrôle réversible plutôt que d’un changement unidirectionnel.
Relier métabolisme et maladie
Étant donné que l’IDH2 est impliquée dans le cancer et d’autres pathologies, les auteurs ont examiné l’importance de cet interrupteur de méthylation dans des contextes proches de la maladie. Dans plusieurs lignées cellulaires normales et cancéreuses, ils ont observé que des niveaux plus élevés de protéine IDH2 allaient souvent de pair avec une méthylation accrue et, de manière surprenante, une activité enzymatique plus faible, suggérant que « plus de protéine » ne signifie pas toujours « plus de fonction ». Dans des jeux de données sur le cancer du sein, les patientes présentant des niveaux protéiques d’IDH2 plus élevés avaient tendance à une survie plus mauvaise, alors que l’activité génique d’IDH2 ne corrélait pas avec l’issue. Les résultats soutiennent un modèle dans lequel la méthylation conduite par CARM1 ralentit le cycle TCA et oriente les cellules vers des voies alternatives d’utilisation des nutriments favorisées par le cancer, tandis que des déméthylases comme KDM3A et KDM4A peuvent ramener les cellules vers une production d’énergie plus efficace.
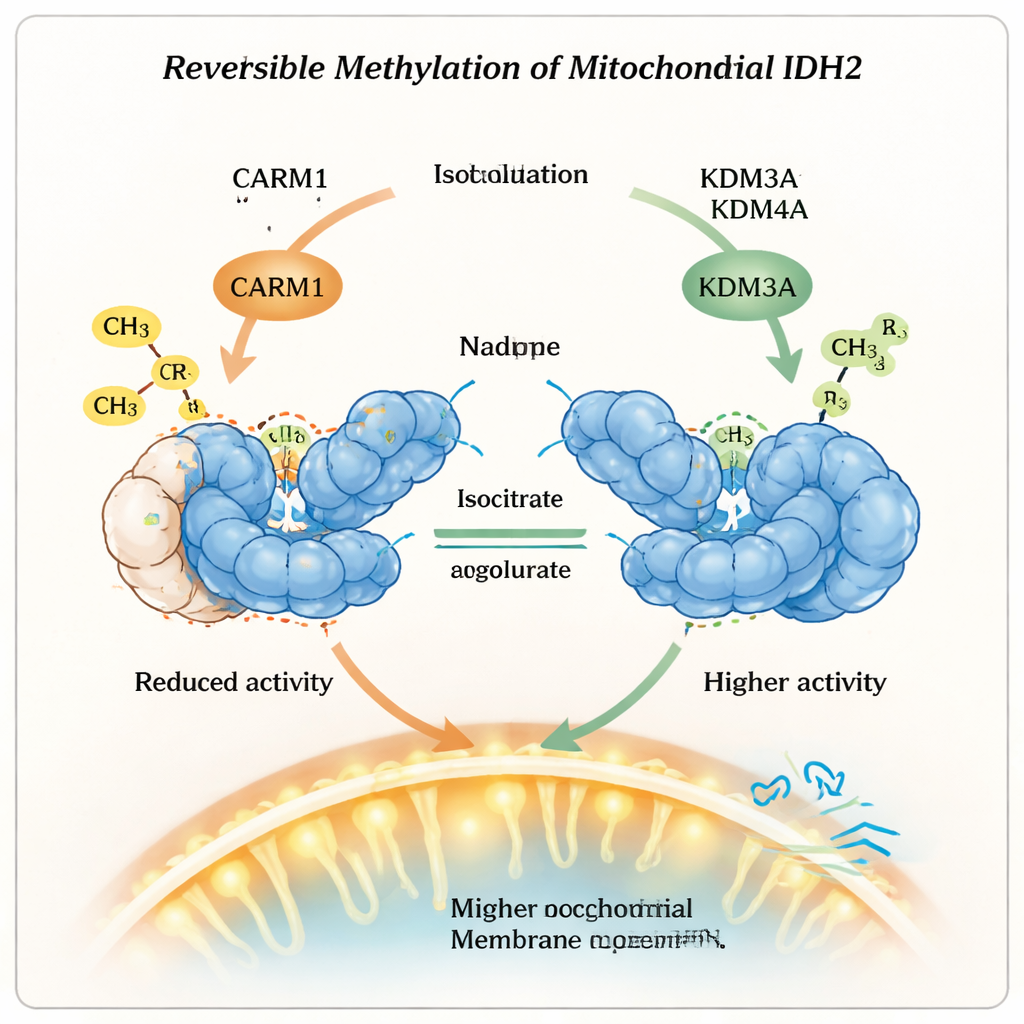
Ce que cela signifie pour la santé et la thérapie
En termes simples, ce travail montre que les mitochondries n’allument pas ou n’éteignent pas simplement des enzymes, mais utilisent des marques chimiques réversibles comme des boutons de réglage fins. En ajoutant un groupe méthyle, CARM1 transforme IDH2 en une forme plus durable mais moins active ; en retirant cette marque, KDM3A et KDM4A sacrifient un peu de stabilité pour gagner en puissance. Cet équilibre influence le choix des cellules entre une combustion rapide mais inefficace du glucose et une production d’énergie plus lente mais plus efficiente. Comprendre ce « variateur » de méthylation sur IDH2 ouvre de nouvelles possibilités thérapeutiques visant à corriger les dysfonctionnements du métabolisme mitochondrial dans des pathologies comme le cancer et les maladies métaboliques, en ciblant les enzymes qui écrivent et effacent ces petites mais puissantes marques chimiques.
Citation: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Mots-clés: mitochondries, IDH2, méthylation de l’arginine, métabolisme cellulaire, CARM1