Clear Sky Science · fr
Une boucle inflammatoire MIF-p38-GSDMD dans les kératinocytes sous-tend le lupus cutané induit par les UVB
Pourquoi la lumière du soleil peut poser un grave problème dans le lupus
Pour la plupart des gens, le soleil provoque simplement un bronzage ou, au pire, un coup de soleil. Mais pour de nombreux patients atteints de lupus, quelques minutes d’exposition aux ultraviolets B (UVB) peuvent déclencher des éruptions douloureuses et durables et même aggraver leur maladie systémique. Cette étude met au jour une « boucle de rétroaction » cachée à l’intérieur des cellules cutanées qui aide à expliquer pourquoi leur peau est si sensible à la lumière — et pointe vers de nouveaux traitements très locaux susceptibles d’atténuer la réaction sans supprimer l’ensemble du système immunitaire.
Les cellules cutanées, fauteurs de troubles inattendus
Les cliniciens savent depuis longtemps que le lupus érythémateux cutané (LEC) implique une inflammation chronique et des cicatrices de la peau, mais l’attention s’est souvent portée sur les cellules immunitaires infiltrantes. En utilisant le séquençage d’ARN cellulaire à l’échelle d’une seule cellule, les auteurs se sont plutôt intéressés aux cellules constitutives de la peau — les kératinocytes dans la couche externe et les fibroblastes en dessous. Ils ont constaté que, chez les patients atteints de lupus, des sous‑populations spécifiques de kératinocytes sont amplifiées et présentent une forte « signature interféron », un profil d’activation permanente de gènes d’alerte antivirale. Parmi ces kératinocytes anormaux, une protéine messagère a émergé : le facteur inhibiteur de la migration des macrophages, ou MIF, produit à des niveaux beaucoup plus élevés que des molécules inflammatoires plus familières comme le TNF ou l’IL‑6.
Un messager caché libéré par la lumière
La présence élevée de MIF à l’intérieur des kératinocytes n’expliquait pas encore pourquoi la lumière du soleil est si dangereuse. Lorsque l’équipe a exposé des kératinocytes cultivés aux UVB, elle a découvert que la quantité totale de MIF dans les cellules changeait peu — mais que la protéine était libérée dans le milieu environnant de façon dépendante de la dose. Plus l’exposition aux UVB était importante, plus le MIF fuyait, en corrélation étroite avec un marqueur de dommages membranaires. Quand ce milieu riche en MIF a été appliqué sur des kératinocytes et fibroblastes frais, il a déclenché des modifications typiques du LEC : augmentation des cytokines inflammatoires et des enzymes qui dégradent et remodelent la matrice de soutien de la peau. Éteindre le MIF par des outils génétiques ou le bloquer par une petite molécule a fortement réduit ces réactions nocives, montrant que le MIF dérivé des kératinocytes n’est pas un simple spectateur mais un amplificateur clé des dégâts induits par les UVB. 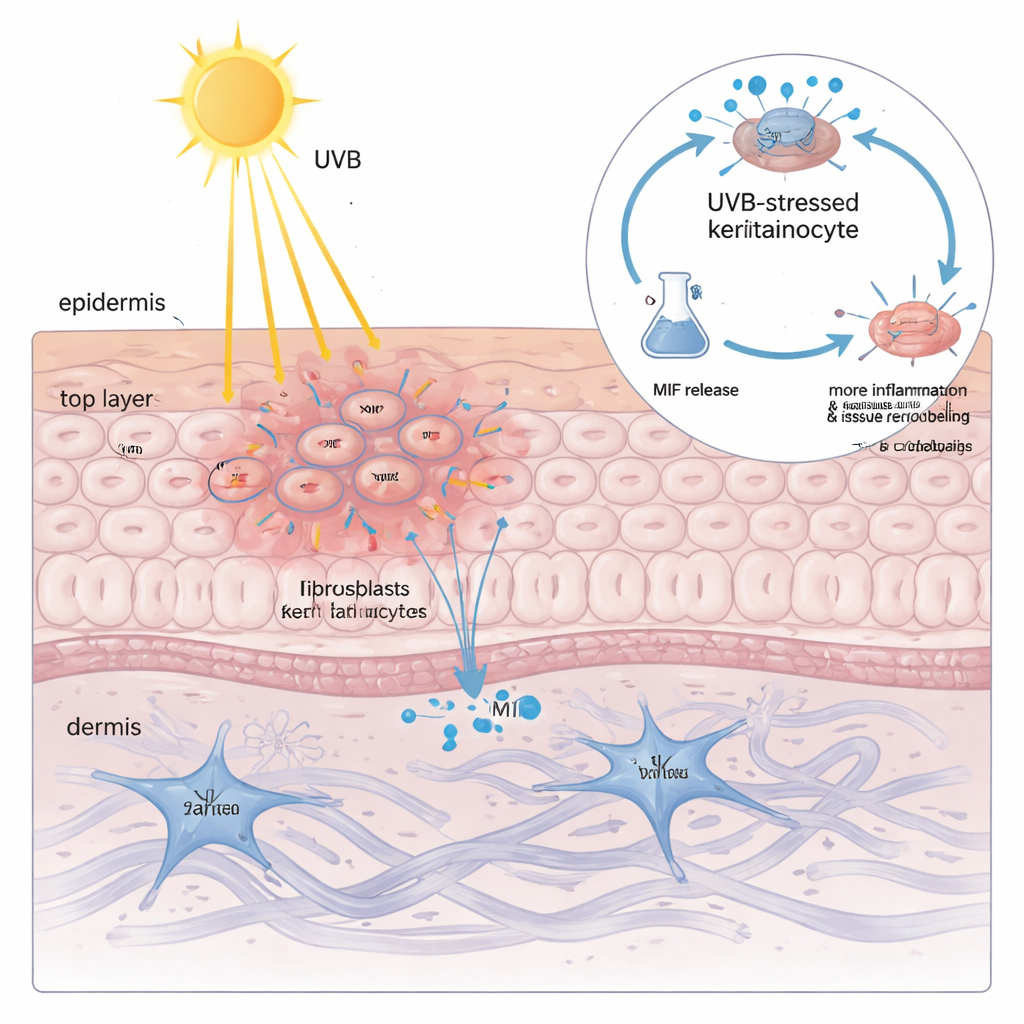
Une boucle inflammatoire auto‑entretenue dans les kératinocytes
Pour comprendre comment les UVB forcent les kératinocytes à libérer le MIF, les chercheurs ont construit un modèle de kératinocyte « de type lupus » en chargeant les cellules avec leur propre ADN et ARN, mimant les débris génétiques mal gérés observés dans le lupus. Dans cet état préparé, les UVB ont activé une réponse de stress ribotoxique : un signal de dommage émanant des ribosomes qui a activé une kinase nommée ZAKα et, à son tour, l’enzyme de stress p38. Cette voie a renforcé une autre protéine, le facteur de transcription C/EBPβ, qui s’est liée à la région de contrôle du gène NLRP3 et l’a activé. NLRP3 a ensuite conduit à la clivage de GSDMD, une protéine formant des pores qui perce des trous dans la membrane cellulaire et provoque une forme inflammatoire de mort cellulaire connue sous le nom de pyroptose. De manière cruciale, le MIF s’échappait principalement par ces pores GSDMD — et non via les vésicules sécrétoires habituelles. Une fois à l’extérieur, le MIF se liait à son récepteur de surface CD74 sur les kératinocytes, réactivant p38, NLRP3 et GSDMD et bouclant ainsi un cercle vicieux : UVB → p38 → NLRP3 → pores GSDMD → libération de MIF → activation accrue de p38.
Du mécanisme moléculaire à de nouveaux traitements locaux
Cette boucle n’était pas qu’une curiosité de laboratoire. Chez une souche de souris prédisposée au lupus, l’exposition aux UVB a produit de sévères lésions cutanées avec des niveaux élevés de MIF, une activation de p38, NLRP3 et GSDMD clivé dans l’épiderme. Lorsque les chercheurs ont utilisé un virus de thérapie génique pour réduire spécifiquement l’expression du gène Mif dans la peau, les éruptions induites par les UVB sont devenues beaucoup plus légères, et les marqueurs d’inflammation et de remodelage tissulaire ont diminué à la fois dans les kératinocytes et les fibroblastes. Pour éviter les effets indésirables systémiques des médicaments, ils ont aussi conçu des patchs de micro‑aiguilles dissolvables chargés de l’inhibiteur de MIF ISO‑1. Pressées brièvement sur la peau, ces minuscules aiguilles délivraient indolorement le médicament dans les couches supérieures. Les souris prédisposées au lupus traitées ont développé bien moins de lésions et moins sévères après UVB, et la signature moléculaire de la boucle MIF‑p38‑GSDMD a été fortement atténuée. 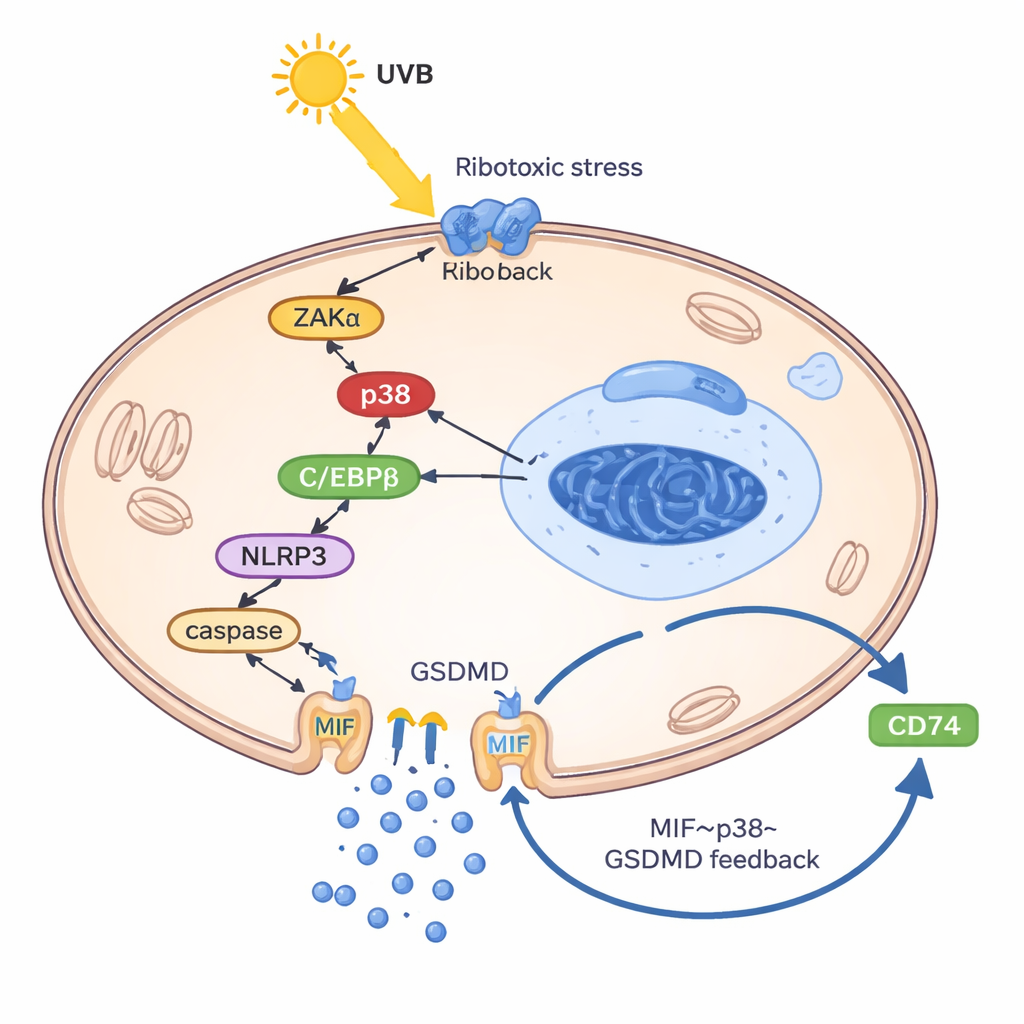
Ce que cela signifie pour les personnes atteintes de lupus
En termes clairs, ce travail montre que, dans le lupus, certaines cellules de la peau sont programmées pour sur‑réagir aux UVB en libérant une molécule « amplificatrice » puissante, le MIF, à travers des pores membranaires auto‑infligés. Cette amplification alimente ensuite à son tour la machinerie inflammatoire, même après la fin de l’exposition initiale à la lumière. En cartographiant cette boucle étape par étape, l’étude suggère que bloquer le MIF directement dans la peau — par silencement génique ou par des systèmes de délivrance intelligents comme des patchs à micro‑aiguilles — pourrait rompre le cycle des poussées photosensibles sans supprimer de manière globale le système immunitaire. Si des stratégies similaires s’avèrent sûres et efficaces chez l’humain, elles pourraient offrir aux personnes atteintes de lupus de nouvelles manières de vivre plus confortablement à la lumière.
Citation: Guo, C., Luo, S., Luo, J. et al. A MIF-p38-GSDMD inflammatory loop in keratinocytes underlies UVB-induced cutaneous lupus. Cell Death Dis 17, 198 (2026). https://doi.org/10.1038/s41419-026-08443-4
Mots-clés: lupus cutané, photosensibilité, kératinocytes, boucle inflammatoire, thérapie par micro-aiguilles