Clear Sky Science · fr
Le honokiol bloque le développement tumoral et les métastases par des effets ciblés sur les mitochondries
Transformer un composé d’arbre en anti‑cancer
De nombreux médicaments anticancéreux proviennent de plantes, et les chercheurs découvrent encore comment certaines de ces molécules naturelles agissent à l’intérieur de nos cellules. Cette étude se concentre sur le honokiol, une substance extraite de l’écorce du magnolia utilisée depuis longtemps en médecine traditionnelle, et montre comment il peut cibler directement les petites centrales énergétiques des cellules cancéreuses pour ralentir la croissance tumorale et bloquer la dissémination, tout en épargnant largement les cellules normales.
Les centrales électriques à l’intérieur de nos cellules
Chaque cellule dépend des mitochondries, souvent qualifiées de « centrales électriques » de la cellule, pour produire la molécule énergétique ATP. Dans le cancer, les mitochondries font plus que fournir du carburant — elles contribuent à décider si une cellule survit ou meurt. Une grande machinerie moléculaire, l’ATP synthase, est intégrée dans la membrane interne des mitochondries et synthétise l’ATP. Les cellules cancéreuses produisent souvent en excès une protéine associée appelée IF1 qui se fixe à l’ATP synthase et agit comme un verrou de sécurité, aidant les tumeurs à résister à une forme d’autodestruction connue sous le nom de transition de perméabilité mitochondriale et à la mort cellulaire qui s’ensuit.
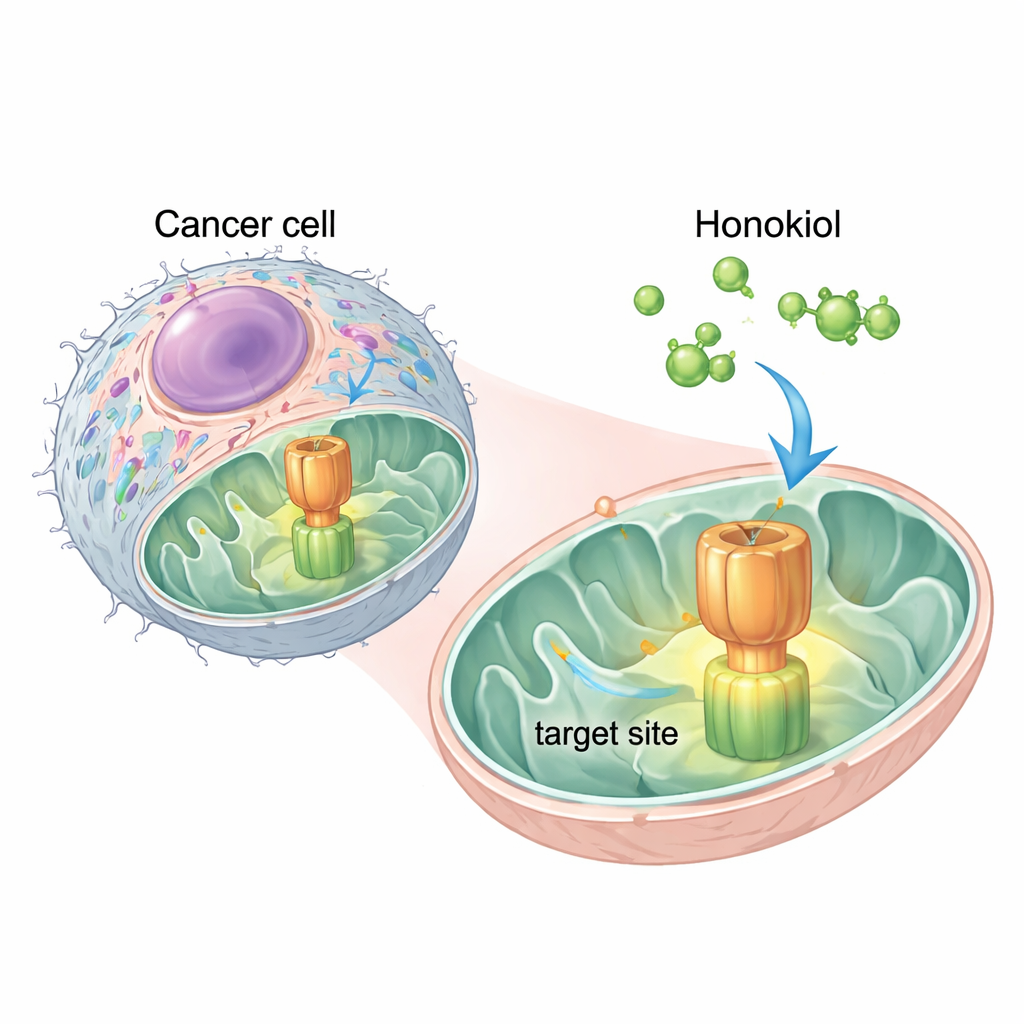
Une molécule naturelle trouve un interrupteur critique
Les chercheurs ont utilisé des simulations informatiques pour déterminer où le honokiol pourrait se fixer sur l’ATP synthase. Ils ont identifié deux sites de « docking » prometteurs sur l’un de ses composants, une région appelée OSCP. Le site le plus fort coïncidait avec la même zone qu’utilise IF1 pour se fixer à l’ATP synthase. Cela suggérait que le honokiol pourrait agir comme une cale moléculaire, s’insérant dans l’OSCP et repoussant IF1. Des expériences sur des cellules humaines de cancer du col utérin HeLa ont confirmé cette idée : l’ajout de honokiol a réduit le contact physique entre IF1 et OSCP, sans perturber d’autres parties de l’enzyme, démontrant que l’effet était spécifique.
Des cellules aux animaux vivants : moins de tumeur, moins de dissémination
Pour savoir si cette poussée moléculaire avait un impact réel, l’équipe a implanté des cellules cancéreuses humaines fluorescentes dans de petits embryons de poisson zèbre, un modèle animal complet bien établi pour suivre la croissance tumorale et les métastases. Chez les poissons injectés avec des cellules HeLa normales riches en IF1, le traitement au honokiol a significativement réduit la taille des masses tumorales et le nombre de cellules cancéreuses ayant migré vers des zones éloignées, rendant le profil similaire à celui observé chez les poissons injectés avec des cellules knock‑out pour IF1, dépourvues de la protéine protectrice. Fait intéressant, le honokiol a aussi diminué le nombre de cellules métastatiques même en l’absence d’IF1, suggérant une seconde voie indépendante d’IF1 limitant la dissémination cancéreuse.
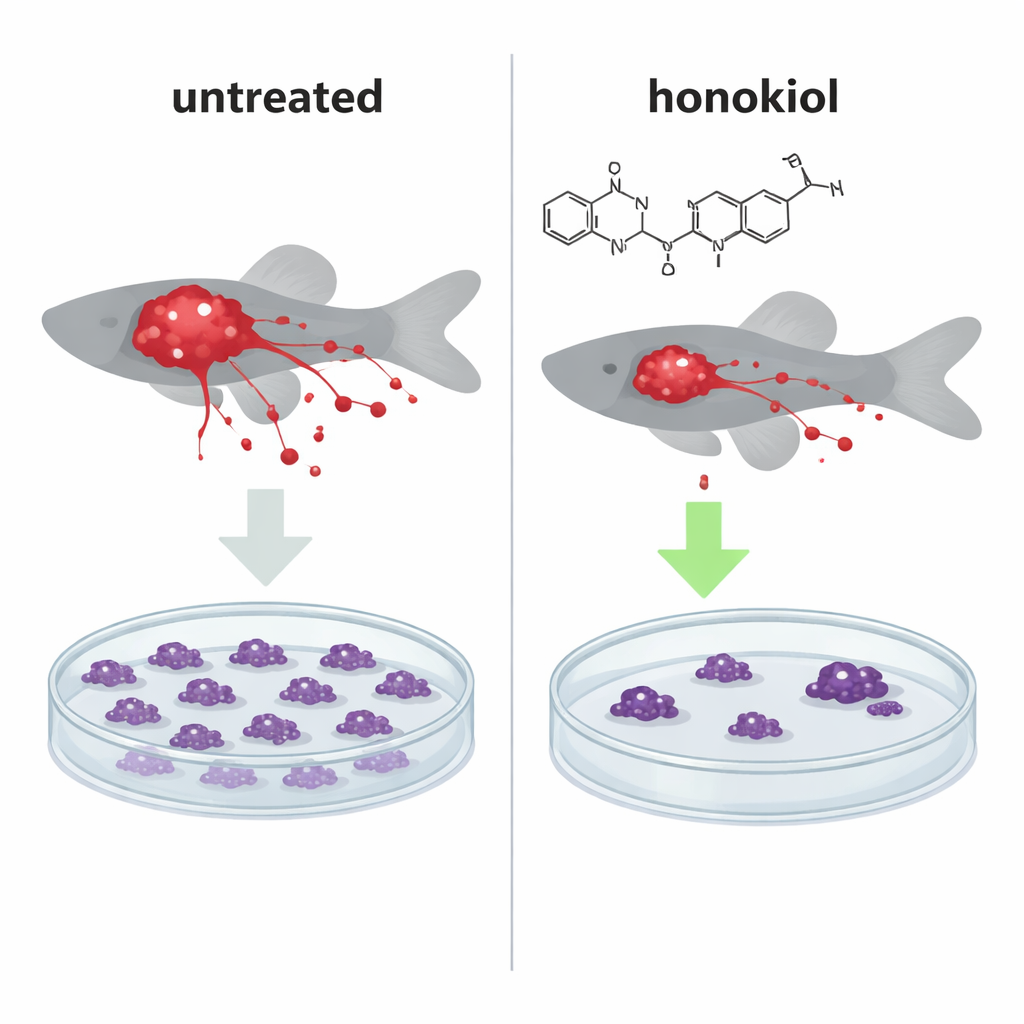
Forcer des centrales défectueuses à déclencher l’autodestruction
En culture, le honokiol a réduit la capacité des cellules cancéreuses à former de grandes colonies en agar mou, un test qui imite les conditions stressantes et hypoxiques des tumeurs solides. Cela s’est produit sans ralentissement majeur de la division cellulaire ordinaire ni de la respiration mitochondriale de base, indiquant plutôt une modification de la façon dont les mitochondries tranchent entre la vie et la mort. Des mesures de la gestion du calcium ont montré que le honokiol faisait ouvrir la pore de transition de perméabilité mitochondriale à des niveaux de calcium plus faibles, un déclencheur connu du gonflement et de la libération de facteurs pro‑mort. À des doses modestes, cet effet dépendait du déplacement d’IF1 ; à des doses plus élevées, le honokiol agissait via son second site de liaison sur OSCP et par une augmentation des espèces réactives de l’oxygène, sensibilisant même les cellules déficientes en IF1 à la mort cellulaire programmée.
Empêcher les cellules cancéreuses de se déplacer
Le cancer devient le plus dangereux lorsque des cellules se détachent et migrent vers de nouveaux organes. Dans des essais de type « scratch » simulant une blessure, le honokiol a fortement ralenti la migration collective de nappes cellulaires tumorales et réduit des marqueurs de la transition épithélio‑mésenchymateuse, un processus qui permet aux cellules tumorales de se déplacer et d’envahir. Des images détaillées en microscopie électronique ont révélé que les cellules en migration augmentent et remodèlent normalement leurs mitochondries, ajoutant des replis internes pour répondre aux fortes demandes énergétiques à l’avant. Avec le honokiol, ces mitochondries de front sont devenues gonflées et structurellement endommagées — caractéristiques de l’ouverture de la pore de transition de perméabilité — tandis que les mitochondries des régions non mobiles étaient moins affectées ou même augmentées en nombre, selon la présence d’IF1.
Ce que cela signifie pour les traitements anticancéreux futurs
En termes simples, ce travail montre que le honokiol peut viser une petite région régulatrice de la machinerie mitochondriale de production d’ATP et actionner un interrupteur de sécurité intégré que les cellules cancéreuses maintiennent souvent verrouillé. En délogeant IF1 et en poussant directement la pore vers l’ouverture, le honokiol encourage les cellules tumorales à s’autodétruire et rend plus difficile leur migration et l’ensemencement de métastases. Parce que ces effets proviennent de caractéristiques partagées par de nombreux cancers — plutôt que d’un seul marqueur de surface — cibler la région OSCP de l’ATP synthase pourrait inspirer une nouvelle classe de thérapies exploitant les vulnérabilités des centrales énergétiques des cellules cancéreuses tout en limitant les dommages aux tissus sains.
Citation: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
Mots-clés: honokiol, mitochondries, ATP synthase, apoptose, métastase