Clear Sky Science · fr
Pneumopathie liée aux inhibiteurs de points de contrôle immunitaires : avancées actuelles et rôle putatif de la thérapie par cellules souches mésenchymateuses
Quand le traitement du cancer se retourne contre les poumons
Les médicaments qui libèrent le système immunitaire contre le cancer ont transformé la prise en charge de maladies comme le cancer du poumon et le mélanome. Mais ce nouveau pouvoir a un prix : chez certains patients, la même attaque immunitaire qui cible les tumeurs se retourne contre les poumons et provoque une affection appelée pneumopathie liée aux inhibiteurs de points de contrôle immunitaires (ICIP). Cette revue explique ce qu’est l’ICIP, pourquoi elle survient, comment les médecins la traitent actuellement, et pourquoi un type particulier de cellules souches — les cellules souches mésenchymateuses (CSM) — pourrait un jour offrir un moyen plus sûr et plus précis d’apaiser la réaction sans sacrifier le contrôle du cancer. 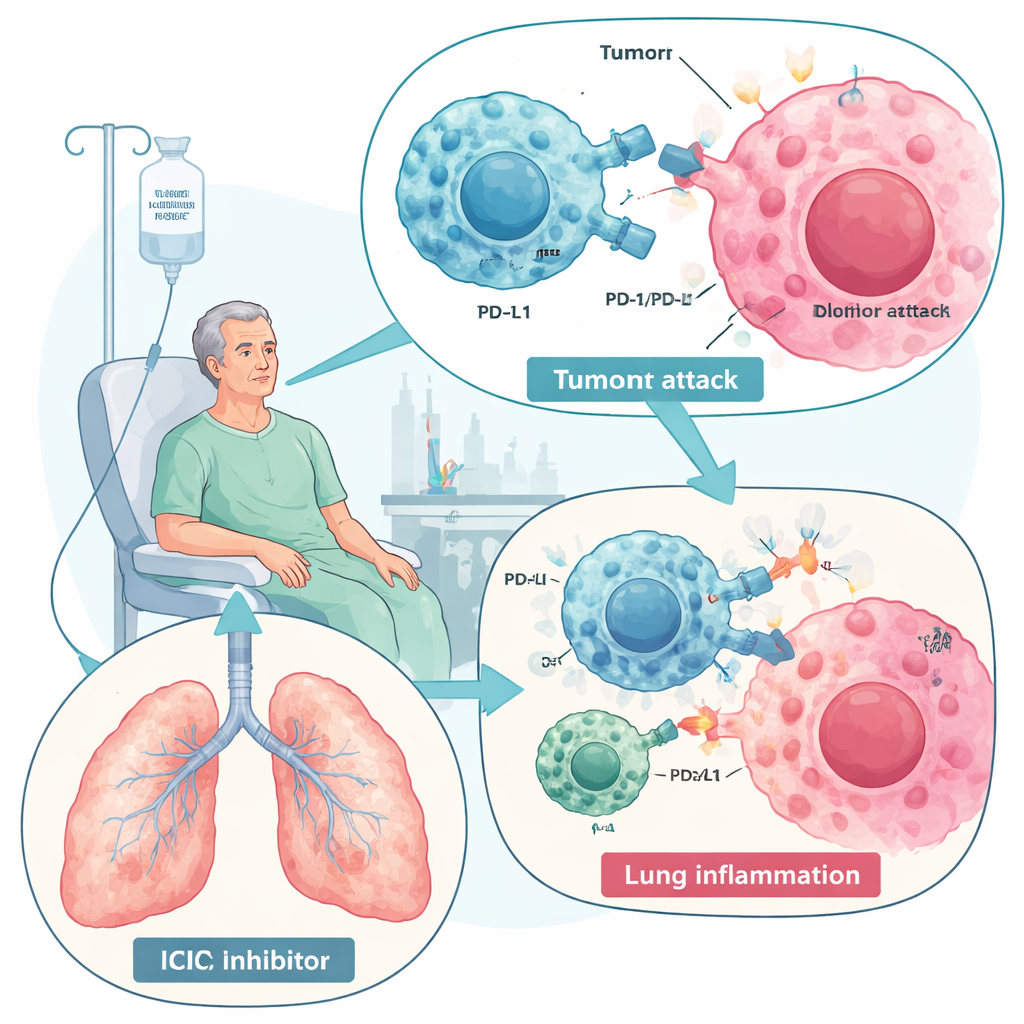
Médicaments anticancéreux puissants avec un risque pulmonaire caché
Les inhibiteurs de points de contrôle immunitaires, en particulier ceux qui bloquent PD-1 et PD-L1, agissent en supprimant les « freins » moléculaires qui limitent normalement les réponses immunitaires. Une fois ces freins levés, les lymphocytes T reconnaissent et détruisent mieux les cellules cancéreuses, améliorant la survie dans de nombreux types de tumeurs. Mais cette stimulation peut aussi perturber la tolérance normale et déclencher des effets indésirables immunitaires dans plusieurs organes. L’ICIP est la complication pulmonaire la plus grave liée à ces médicaments et l’une des principales causes de décès associés aux réactions immunitaires. Elle touche de quelques pourcents jusqu’à près d’un tiers des patients dans certaines études en conditions réelles, surtout chez les personnes atteintes de cancer du poumon ou de maladies pulmonaires préexistantes telles que la BPCO ou les pneumopathies interstitielles. Les symptômes vont d’une toux légère et d’un essoufflement à une insuffisance respiratoire potentiellement mortelle.
Comment le système immunitaire endommage le poumon
La revue décrit l’ICIP comme le résultat d’un déséquilibre immunitaire au sein des poumons. Des cellules « combattantes » hyperactives — lymphocytes T CD8, certains lymphocytes T auxiliaires, macrophages inflammatoires, neutrophiles et cellules NK — affluents dans le tissu pulmonaire et libèrent des protéines de signalisation agressives, notamment l’interféron‑gamma, le TNF‑alpha et des interleukines comme IL‑6 et IL‑17. Parallèlement, les cellules normalement protectrices qui atténuent l’inflammation, telles que les lymphocytes T régulateurs et les macrophages orientés vers la réparation, sont diminuées. Certains patients montrent aussi une augmentation d’anticorps autoréactifs avant ou pendant le traitement, ce qui suggère que l’ICIP peut partiellement ressembler à une maladie auto-immune. Dans le liquide de lavage broncho‑alvéolaire, les médecins retrouvent un profil inflammatoire riche en lymphocytes T et un cocktail de cytokines distincts d’une infection ou d’une progression tumorale, ce qui peut aider au diagnostic.
Détection, gradation et prise en charge des lésions
À la tomodensitométrie, l’ICIP se manifeste le plus souvent par des zones en verre dépoli ou des condensations parcellaires disséminées dans les deux poumons, des schémas qui diffèrent des lésions post‑radiation qui restent limitées au champ irradié. Le diagnostic d’ICIP repose sur la combinaison des données scannographiques, des symptômes et d’une exclusion rigoureuse des infections et autres causes. Les recommandations internationales gradent ensuite la gravité de 1 (léger, souvent uniquement radiologique) à 4 (insuffisance respiratoire mettant en jeu le pronostic vital). Le traitement actuel de base repose sur les glucocorticoïdes — stéroïdes anti‑inflammatoires puissants — parfois associés à d’autres agents immunosuppresseurs comme le tocilizumab (bloquant IL‑6) ou l’infliximab (bloquant TNF‑alpha) dans les cas graves ou résistants aux corticoïdes. Ces approches peuvent sauver des vies, mais ce sont des outils peu précis : les corticoïdes entraînent de nombreux effets indésirables, certains patients ne répondent pas, et l’immunosuppression large peut affaiblir la réponse antitumorale que ces traitements visaient à renforcer.
Pourquoi les cellules souches entrent dans la discussion
Les cellules souches mésenchymateuses, récupérables dans la moelle osseuse, le tissu adipeux ou le cordon ombilical, sont apparues comme de prometteurs « modulateurs immunitaires » plutôt que de simples constructeurs tissulaires. Une fois injectées dans la circulation, beaucoup de ces cellules se retrouvent temporairement piégées dans les petits vaisseaux du poumon — un effet dit de premier passage — ce qui est un inconvénient pour traiter des organes distants mais un avantage potentiel pour les maladies pulmonaires. Dans des modèles animaux et des essais humains précoces sur des affections comme la pneumonie sévère, le syndrome de détresse respiratoire aiguë, les maladies inflammatoires de l’intestin et la maladie du greffon contre l’hôte, les CSM atténuent les réponses immunitaires hyperactives, réorientent les cellules immunitaires vers un état plus équilibré et sécrètent des facteurs de croissance qui favorisent la réparation tissulaire tout en limitant la fibrose. Il est important de noter que leurs bénéfices proviennent souvent non pas de leur différenciation en cellules pulmonaires mais du mélange de molécules de signalisation et de petites vésicules qu’elles libèrent. 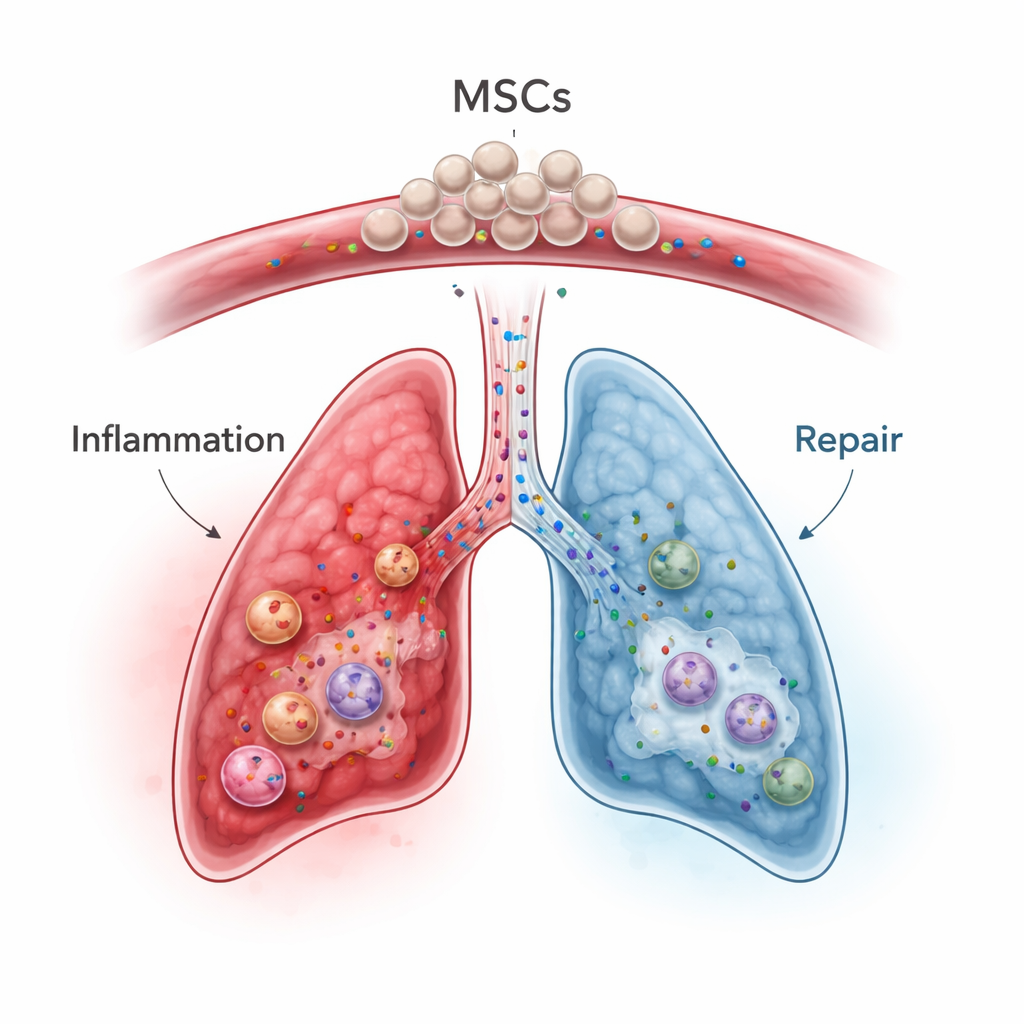
Comment les CSM pourraient calmer l’ICIP sans compromettre la guérison
Dans le contexte de l’ICIP, les CSM pourraient théoriquement résoudre plusieurs problèmes simultanément. Elles peuvent restreindre directement les lymphocytes T activés, favoriser la croissance et la fonction des lymphocytes T régulateurs et pousser les macrophages à quitter un phénotype agressif et lésant vers un mode réparateur. Elles réduisent aussi des médiateurs inflammatoires clés tels que IL‑6, IL‑1β et TNF‑alpha, et augmentent des facteurs anti‑inflammatoires et des protéines protectrices comme TSG‑6 qui aident à limiter les lésions pulmonaires et la fibrose. Des travaux précliniques suggèrent que les CSM ou des exosomes dérivés de CSM peuvent réduire les tempêtes cytokiniques et les atteintes d’organes induites par les inhibiteurs de points de contrôle ou la radiothérapie, tout en préservant, dans certains contextes, l’activité antitumorale mieux que des immunosuppresseurs classiques. Néanmoins, les auteurs mettent en garde : les CSM peuvent aussi interagir avec les tumeurs et la coagulation sanguine de façon complexe, et leurs effets dépendent fortement de l’environnement inflammatoire ambiant et même de la source des CSM (moelle osseuse, tissu adipeux ou cordon ombilical).
Perspectives : un espoir nécessitant des tests rigoureux
Pour les patients dont le traitement anticancéreux est interrompu ou menacé par une toxicité pulmonaire sévère, les thérapies à base de CSM pourraient éventuellement offrir une manière plus ciblée d’éteindre l’inflammation, de réparer le tissu pulmonaire et de prévenir la fibrose à long terme — idéalement sans annuler les bénéfices vitaux de l’inhibition des points de contrôle immunitaires. Cependant, aucun essai spécifique de CSM pour l’ICIP n’a encore été achevé. Les auteurs soutiennent que des études animales bien conçues et des essais cliniques sont urgemment nécessaires pour définir quel type de CSM ou de produit d’exosomes est le plus efficace, quelle posologie utiliser, à quel moment l’administrer par rapport aux corticoïdes et à l’immunothérapie, et comment surveiller les risques tels que la croissance tumorale ou la thrombose. Jusqu’à ce moment, les CSM restent une option prometteuse mais encore expérimentale à l’horizon pour la prise en charge de cet effet secondaire grave des soins oncologiques modernes.
Citation: Li, Z., Zheng, X., Xia, H. et al. Immune checkpoint inhibitor-related pneumonitis: current advances and the putative role of mesenchymal stem cell therapy. Cell Death Dis 17, 200 (2026). https://doi.org/10.1038/s41419-026-08440-7
Mots-clés: effets secondaires de l'immunothérapie, pneumopathie, inhibiteurs de points de contrôle, cellules souches mésenchymateuses, inflammation pulmonaire