Clear Sky Science · fr
c-Myc/GRPEL1 maintient la synthèse des acides gras via FASN pour soutenir la prolifération des cellules PDAC
Pourquoi l’appétit des cellules cancéreuses pour les graisses est important
Le cancer du pancréas est l’un des plus meurtriers, en partie parce que ses cellules sont expertes pour reprogrammer leur propre métabolisme afin de survivre et de croître. Cette étude examine un aspect inattendu de ce phénomène : comment les cellules tumorales pancréatiques activent leurs « usines à graisses » internes pour alimenter une croissance implacable, et comment bloquer ce processus pourrait ouvrir de nouvelles options thérapeutiques pour les patients.
Un cancer difficile avec un avantage métabolique
La plupart des cancers du pancréas sont un type appelé adénocarcinome canalaire pancréatique (PDAC), généralement détecté tard et peu réceptif aux traitements actuels. Les cellules PDAC vivent dans un environnement hostile, pauvre en oxygène et en nutriments, et pourtant elles prospèrent en réécrivant leur utilisation du glucose, des lipides et d’autres carburants. Leurs mitochondries — de petites centrales énergétiques à l’intérieur des cellules — jouent un rôle central dans cette réorganisation. Pour maintenir ces centrales en fonction, les cellules surveillent et réparent en permanence des milliers de protéines mitochondriales, un processus appelé contrôle de qualité des protéines mitochondriales. Jusqu’à présent, on ignorait comment cette machinerie de contrôle de qualité se reliait à la façon dont les tumeurs pancréatiques se nourrissent.
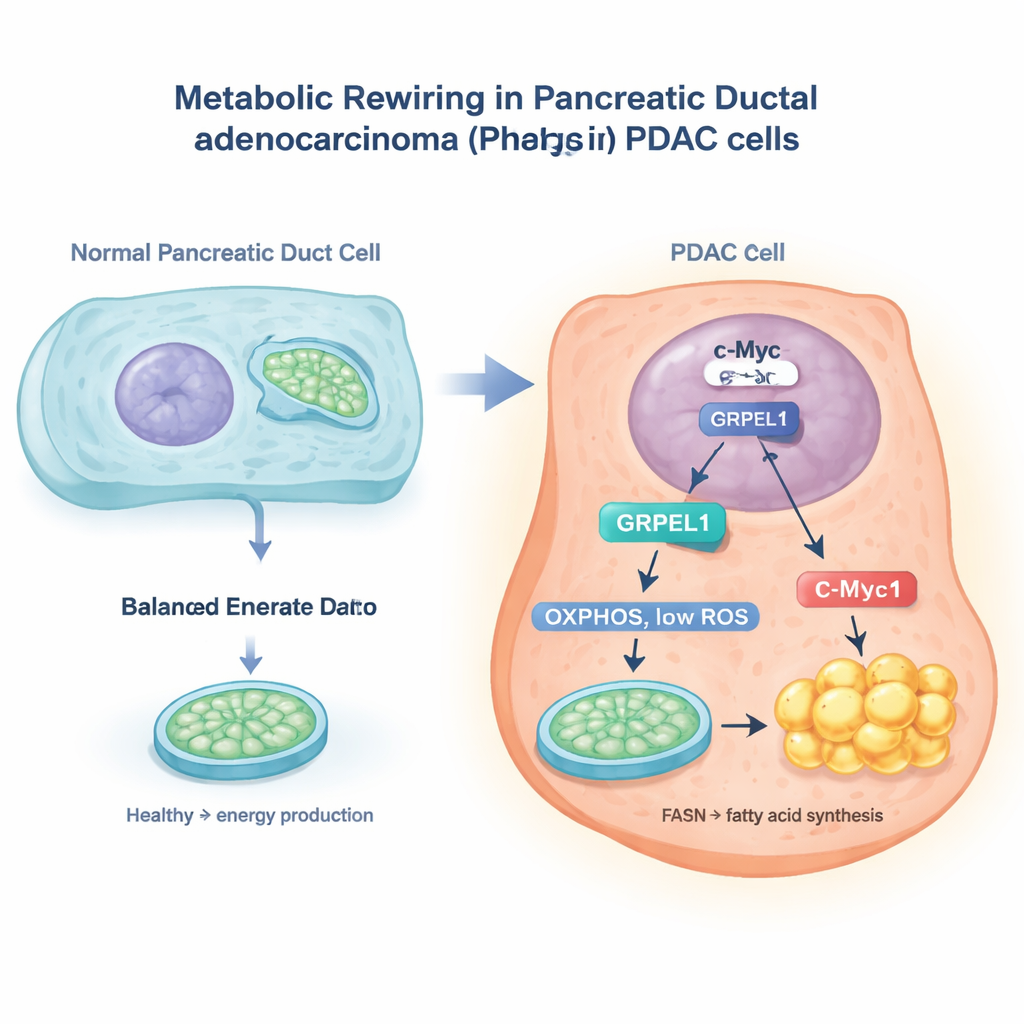
Le commutateur c-Myc et un assistant mitochondrial
Les chercheurs ont utilisé de larges bases de données sur le cancer et des expériences sur des cellules de cancer pancréatique pour se concentrer sur une protéine appelée GRPEL1, une aide impliquée dans la gestion des protéines mitochondriales. Ils ont découvert qu’un gène connu du cancer, c-Myc, agit comme un interrupteur moléculaire dans le noyau cellulaire qui active le gène GRPEL1. Lorsque les niveaux de c-Myc diminuaient, ceux de GRPEL1 baissaient ; lorsque c-Myc augmentait, GRPEL1 augmentait. Les prélèvements tumoraux de patients montraient aussi que c-Myc et GRPEL1 avaient tendance à être élevés simultanément, et que les deux étaient liés à de moins bons résultats. Dans des cellules PDAC cultivées en laboratoire, réduire GRPEL1 ralentissait la division cellulaire et la formation de colonies, tandis qu’ajouter du GRPEL1 supplémentaire favorisait la prolifération, en particulier lorsque c-Myc était par ailleurs bloqué.
Des mitochondries à la production de graisses
En creusant davantage, l’équipe a constaté que GRPEL1 fait plus que maintenir l’ordre parmi les protéines mitochondriales. Lorsque GRPEL1 était épuisé, les mitochondries des cellules PDAC devenaient moins efficaces pour produire de l’énergie, perdaient leur forme normale et libéraient davantage d’espèces réactives de l’oxygène (ROS) — des sous-produits chimiquement réactifs parfois appelés « rouille » cellulaire. Cette augmentation des ROS avait un effet en cascade : elle réduisait les niveaux de la synthase des acides gras (FASN), une enzyme clé qui construit de nouveaux acides gras à l’intérieur des cellules. Avec FASN diminuée, les cellules produisaient moins de lipides, stockaient moins de graisses et leur croissance ralentissait. Lorsque les chercheurs ont neutralisé les ROS avec un antioxydant, les niveaux de FASN remontaient, montrant que le lien GRPEL1–FASN est médié par les ROS. Fait intéressant, c-Myc lui-même ne semblait pas activer directement le gène FASN dans ce système, mais influençait FASN indirectement via GRPEL1 et le stress mitochondrial.
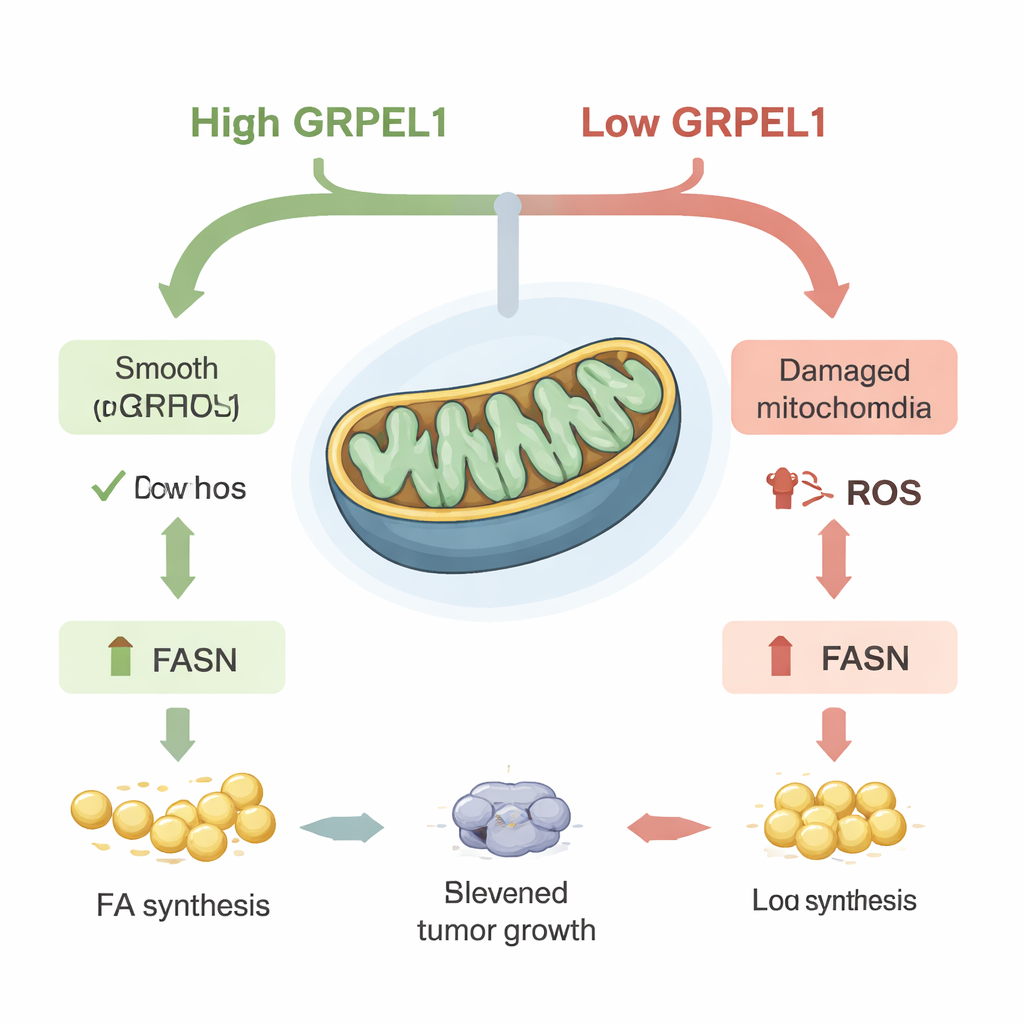
La graisse comme carburant pour la croissance tumorale
Puisque FASN est au cœur de la fabrication des graisses, les scientifiques se sont demandé si le restaurer pouvait sauver la croissance des cellules tumorales lorsque GRPEL1 était faible. En culture cellulaire, forcer les cellules à produire plus de FASN a partiellement inversé le ralentissement de la croissance et de la formation de colonies causé par la perte de GRPEL1. Il en allait de même chez la souris : les tumeurs formées à partir de cellules appauvries en GRPEL1 croissaient plus lentement, mais la réintroduction de FASN a ravivé à la fois la taille des tumeurs et leur contenu en lipides. Des analyses détaillées des métabolites et des lipides ont montré des baisses générales de nombreuses molécules liées aux graisses lorsque GRPEL1 ou c-Myc étaient réduits. Fait important, l’apport externe d’acides gras ou d’un mélange lipidique a partiellement restauré la croissance tant dans des lignées cellulaires cancéreuses que dans des organoïdes pancréatiques dérivés de patients — mini-tumeurs cultivées en 3D — suggérant que le problème principal était la perte de graisses nouvellement synthétisées.
Transformer une vulnérabilité en thérapie
Dans l’ensemble, ce travail brosse un tableau clair : dans le cancer du pancréas, c-Myc augmente GRPEL1, ce qui aide les mitochondries à fonctionner correctement et maintient les ROS sous contrôle. Cet environnement mitochondrial calme permet aux cellules de conserver des niveaux élevés de FASN, produisant de nouveaux acides gras qui servent de briques pour les membranes, de réserves énergétiques et de signaux de croissance. Lorsque GRPEL1 est bloqué, les mitochondries défaillent, les ROS augmentent, FASN diminue et les cellules cancéreuses peinent à croître — un effet qui peut être en partie contourné si des graisses sont fournies de l’extérieur. Pour un lectorat non spécialisé, la conclusion est que les tumeurs pancréatiques dépendent d’un circuit interne de « fabrication des graisses », piloté par c-Myc, GRPEL1 et FASN. Des médicaments qui perturbent cet axe de production d’acides gras, en particulier dans les tumeurs où il est très actif, pourraient offrir une nouvelle manière prometteuse d’affamer les cellules du cancer du pancréas tout en épargnant davantage les tissus normaux.
Citation: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
Mots-clés: cancer du pancréas, métabolisme tumoral, synthèse des acides gras, mitochondries, c-Myc