Clear Sky Science · fr
KDM5B coopère avec le complexe CRL4B pour favoriser la tumorigenèse du cancer du sein ER+ en régulant le métabolisme du cholestérol
Pourquoi cette recherche importe pour la santé au quotidien
Le cancer du sein est le cancer le plus fréquent chez les femmes, et de nombreuses tumeurs croissent en réponse à l’hormone œstrogène. Ces cancers ne se contentent pas de se diviser rapidement : ils reconfigurent aussi leur utilisation des lipides, comme le cholestérol. Cette étude révèle comment une protéine régulatrice de gènes appelée KDM5B s’associe à un autre complexe protéique, CRL4B, pour augmenter le cholestérol à l’intérieur des cellules de cancer du sein récepteurs d’œstrogènes positifs (ER+). Comprendre ce partenariat caché peut aider les scientifiques à trouver de nouvelles façons de ralentir la croissance tumorale et d’améliorer des traitements existants, tels que l’hormonothérapie et les médicaments abaissant le cholestérol.
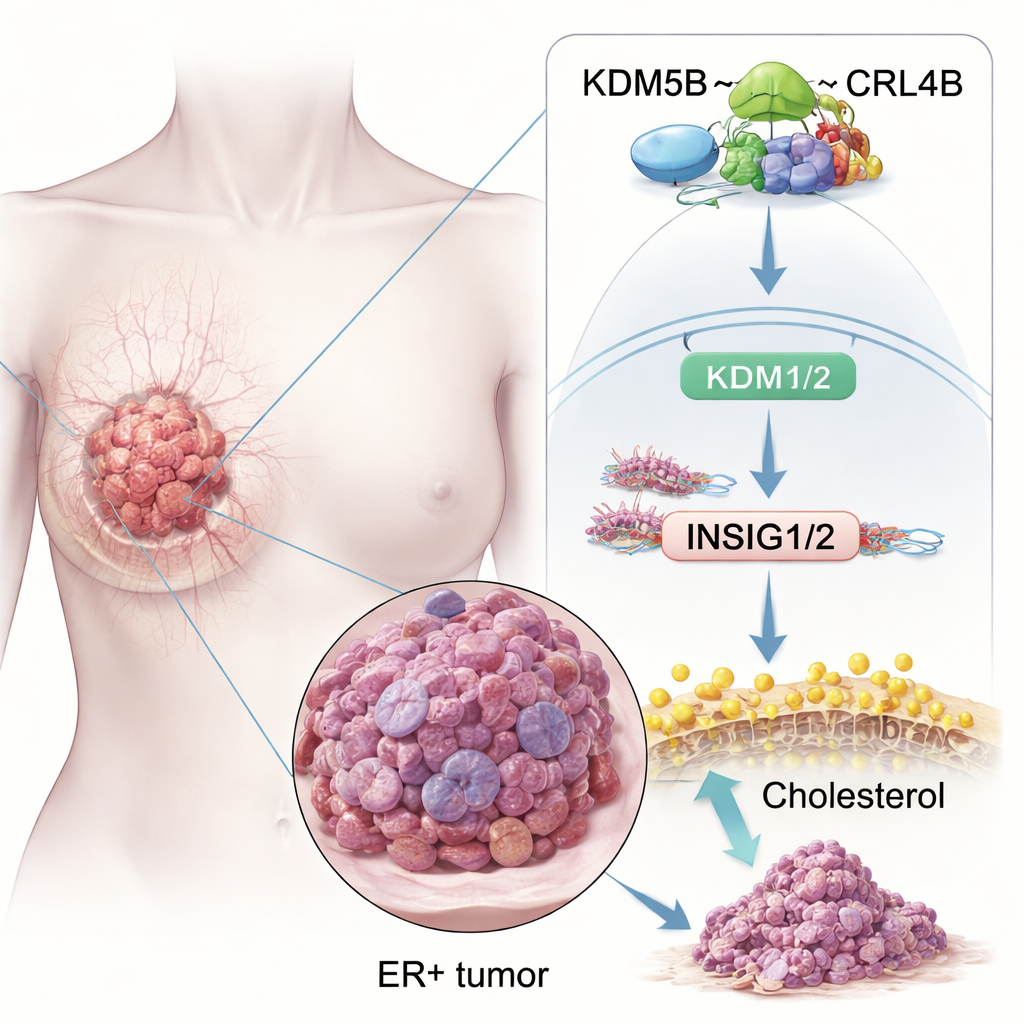
Une protéine qui fait pencher la balance vers le cancer
Les chercheurs ont d’abord cherché à savoir si KDM5B est simplement présent dans les cancers ER+ ou s’il contribue réellement à les entraîner. En analysant de larges bases de données sur le cancer et des échantillons de tissus, ils ont constaté que les taux de KDM5B sont plus élevés dans les tumeurs mammaires que dans le tissu mammaire normal, et particulièrement élevés dans les tumeurs ER+. Les patientes dont les cancers expriment davantage KDM5B présentent une survie moins bonne, même lorsqu’elles reçoivent une chimiothérapie standard ou une hormonothérapie. In vitro, la surexpression de KDM5B a rendu les cellules de cancer du sein ER+ plus prolifératives, plus invasives et plus aptes à former des amas à caractère de cellules souches, supposés initier de nouvelles tumeurs. À l’inverse, l’inhibition de KDM5B réduisait les colonies en culture et la croissance tumorale chez la souris.
Un partenariat puissant au sein des cellules cancéreuses
Pour comprendre comment KDM5B produit ces effets, l’équipe a recherché ses partenaires protéiques. Ils ont découvert que KDM5B se lie physiquement à des composants d’une machinerie moléculaire appelée complexe CRL4B, un système enzymatique qui marque des protéines et modifie aussi l’emballage de l’ADN. Des tests biochimiques détaillés ont montré que KDM5B interagit directement avec deux composants de CRL4B, CUL4B et DDB1, via des régions spécifiques de chaque protéine. Dans les cellules de cancer du sein ER+, ce complexe KDM5B–CRL4B agit sur de nombreux gènes au niveau de leurs interrupteurs d’activation. Des cartographies à l’échelle du génome ont révélé que KDM5B et CUL4B occupent souvent ensemble les promoteurs de gènes, où ils modifient des marques chimiques sur les histones — les bobines autour desquelles l’ADN est enroulé — pour réprimer l’expression des gènes.
Relâcher les freins sur le cholestérol
Parmi les voies affectées, le métabolisme du cholestérol s’est distingué. Les cellules cancéreuses ont besoin d’un surplus de cholestérol pour construire leurs membranes et résister au stress, et les tumeurs ER+ utilisent aussi des molécules dérivées du cholestérol pour mimer l’œstrogène. L’étude montre que le complexe KDM5B–CRL4B se lie directement aux régions de contrôle de deux gènes « freins », INSIG1 et INSIG2. Ces gènes contribuent normalement à maintenir sous contrôle un régulateur maître du cholestérol, SREBP2. KDM5B–CRL4B ajoute une marque répressive (H2AK119ub1) et enlève une marque activateur (H3K4me3) sur les histones aux promoteurs d’INSIG1/2, diminuant ainsi leur expression. Avec moins de protéines INSIG1/2, SREBP2 est libéré pour activer les gènes de biosynthèse du cholestérol, augmentant les niveaux de cholestérol à l’intérieur des cellules ER+ et favorisant leur comportement invasif. Lorsque les chercheurs ont perturbé KDM5B ou CRL4B, INSIG1/2 augmentait, l’activité de SREBP2 diminuait et le cholestérol total intracellulaire reculait.
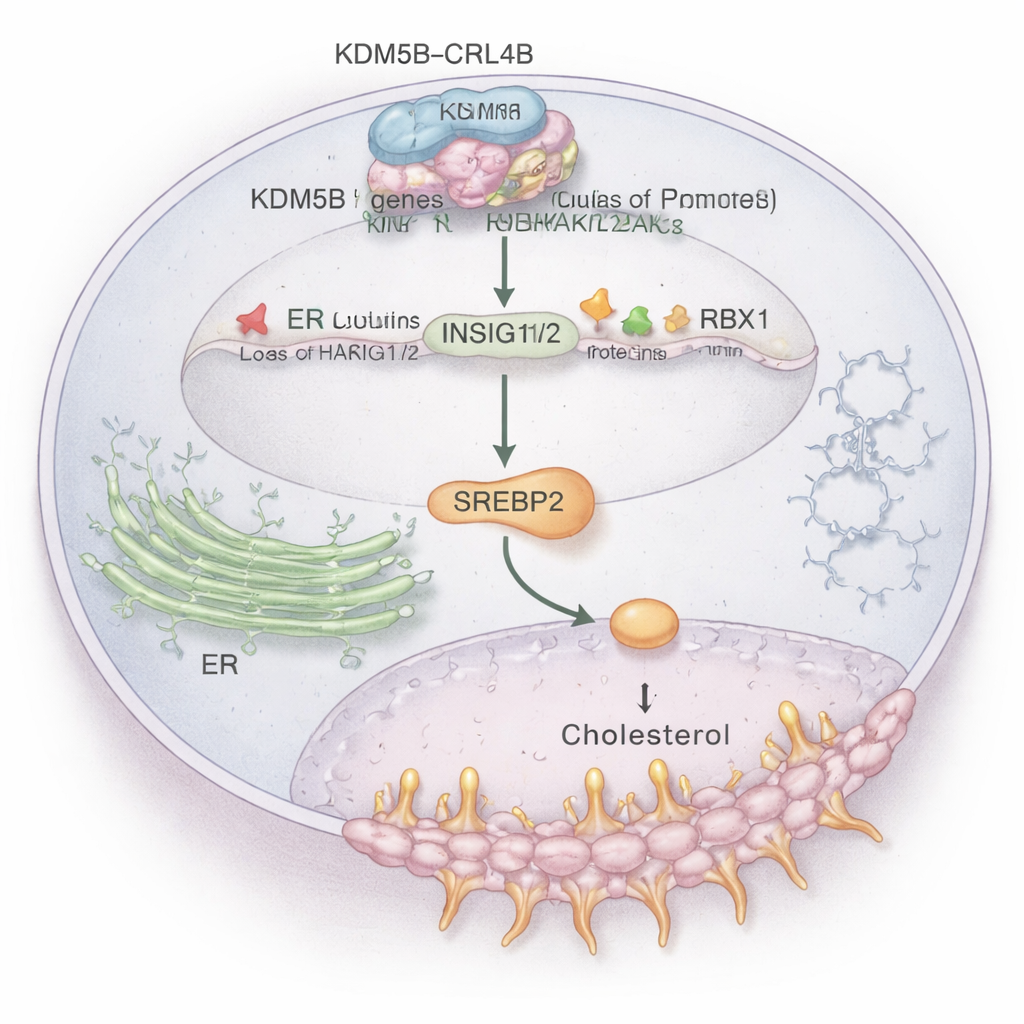
Les médicaments hypocholestérolémiants croisent les voies du cancer
Les travaux relient aussi cette voie à un signal dérivé du cholestérol, le 27‑hydroxycholestérol (27‑HC), une molécule déjà connue pour promouvoir le cancer du sein ER+. Le traitement de cellules ER+ par le 27‑HC augmentait les niveaux de KDM5B et réprimait encore davantage INSIG1/2, poussant les cellules vers une plus grande prolifération et invasivité. De façon importante, bloquer KDM5B ou CRL4B atténuait ces effets agressifs, suggérant que le 27‑HC agit en partie en alimentant l’axe KDM5B–CRL4B. Par ailleurs, les chercheurs ont montré que la simvastatine, une statine largement utilisée pour abaisser le cholestérol, ralentissait la croissance des cellules de cancer du sein, et que son association à un inhibiteur de KDM5B renforçait l’effet anti‑tumoral. Cela laisse entrevoir que combiner des médicaments ciblant la production de cholestérol avec des traitements visant l’activité régulatrice de KDM5B pourrait constituer une stratégie thérapeutique prometteuse.
Ce que cela signifie pour les patientes et les traitements futurs
Cette étude révèle une nouvelle chaîne d’événements au sein des cellules de cancer du sein ER+ : un signal lié au cholestérol (27‑HC) augmente KDM5B ; KDM5B s’associe au complexe CRL4B pour réprimer INSIG1 et INSIG2 ; cela libère SREBP2, stimule la production de cholestérol et favorise la croissance tumorale, l’invasion et le maintien de cellules de type souche. Comme KDM5B est également élevé et associé à une survie défavorable dans plusieurs autres cancers, bloquer cette protéine — ou restaurer les freins INSIG1/2 — pourrait offrir de nouvelles pistes pour contrôler la croissance tumorale. Bien que des travaux supplémentaires soient nécessaires avant une application clinique, ces résultats soulignent à quel point le comportement des cancers est lié à des molécules du quotidien comme le cholestérol, et comment des médicaments existants, tels que les statines, pourraient un jour être combinés à des thérapies épigénétiques pour améliorer les résultats.
Citation: Yang, Y., Gao, T., Yuan, B. et al. KDM5B cooperates with CRL4B complex to promote the tumorigenesis of ER+ breast cancer via regulating cholesterol metabolism. Cell Death Dis 17, 207 (2026). https://doi.org/10.1038/s41419-026-08438-1
Mots-clés: cancer du sein ER‑positif, métabolisme du cholestérol, KDM5B, INSIG1/INSIG2, thérapie épigénétique