Clear Sky Science · fr
La signalisation TGFβ favorise la progression du cycle cellulaire et la résistance à l’inhibiteur CDK4/6 palbociclib via la modulation transcriptionnelle de SOX4 dans les cellules mammaires cancéreuses
Quand les cellules cancéreuses détournent un signal normalement protecteur
Notre organisme repose sur d’innombrables signaux chimiques pour lancer la division cellulaire lorsque c’est nécessaire et l’arrêter quand il le faut. L’un de ces signaux, appelé facteur de croissance transformant bêta (TGFβ), contribue normalement à prévenir les tumeurs. Cette étude montre comment, dans certains cancers du sein, le même signal TGFβ peut être détourné pour favoriser la croissance des cellules tumorales et leur résistance à un médicament important, le palbociclib. Comprendre ce basculement pourrait orienter de meilleures combinaisons thérapeutiques pour les patientes dont les tumeurs cessent de répondre au traitement.
Du frein à la croissance à un signal à double tranchant
Dans les tissus sains, le TGFβ agit généralement comme un frein : il ralentit la division cellulaire et limite l’inflammation, contribuant ainsi à prévenir la formation précoce de tumeurs. Mais dans des cancers établis, en particulier dans les tumeurs mammaires qui ont déjà accumulé des mutations oncogéniques, le TGFβ peut avoir l’effet inverse — en favorisant la migration, l’invasion et la dissémination des cellules. Pour explorer ce comportement double, les chercheurs ont utilisé des « mini-tumeurs » tridimensionnelles cultivées à partir de cellules mammaires humaines. Ils ont comparé des cellules d’aspect normal à des cellules par ailleurs identiques porteuses d’une mutation oncogénique HRAS, qui les pousse vers le cancer. Ce modèle contrôlé leur a permis d’étudier comment le même signal TGFβ se manifeste dans un environnement pré-cancéreux versus un environnement de type cancéreux. 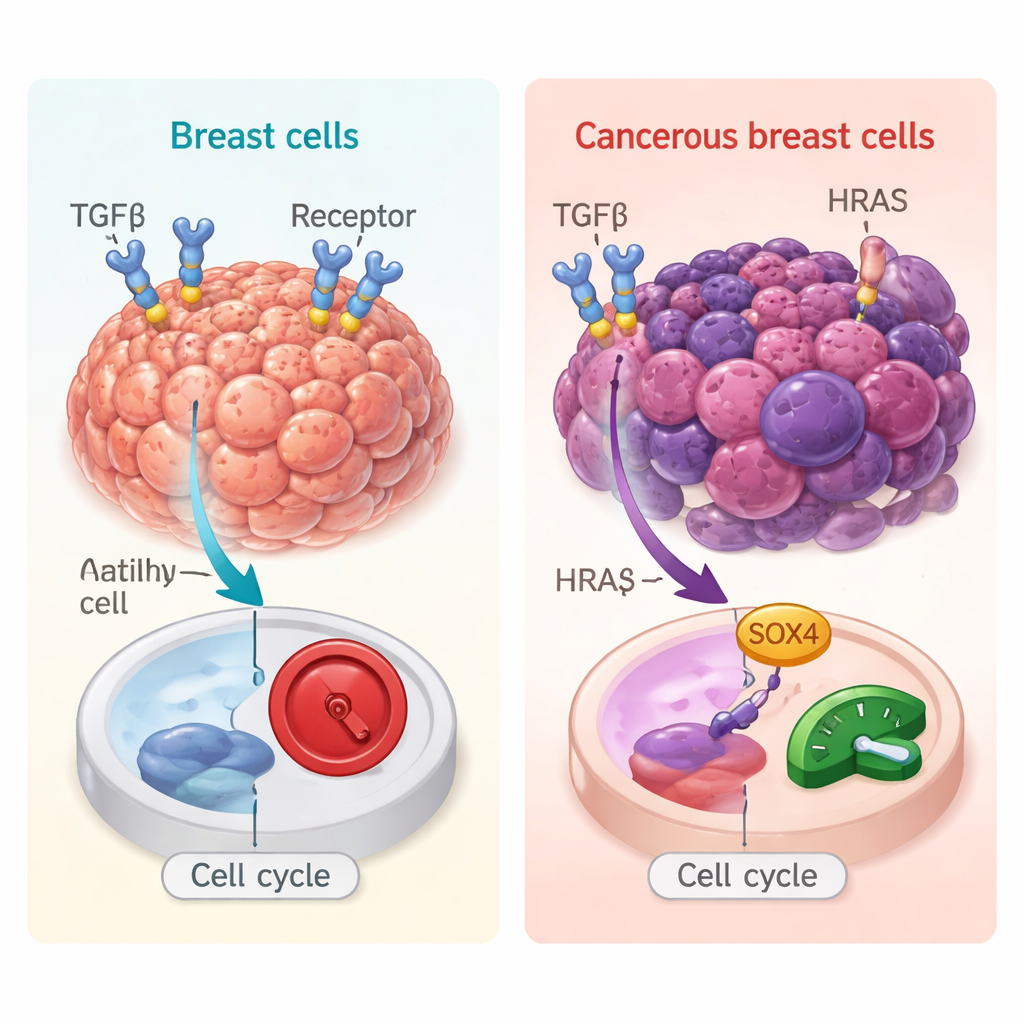
Reconfigurer les interrupteurs marche/arrêt du génome
L’équipe s’est intéressée à la chromatine, l’emballage d’ADN et de protéines qui contrôle l’accessibilité des gènes et leur activation potentielle. Après traitement des amas cellulaires 3D par le TGFβ, ils ont observé une ouverture généralisée de la chromatine aux sites de départ des gènes et aux régions amplificatrices distales, tant dans les cellules d’aspect normal que dans les cellules mutants HRAS. Cependant, le profil des nouveaux sites accessibles différait nettement entre les deux. Dans les cellules de type cancéreux, les sites de liaison pour un facteur de transcription nommé SOX4 étaient particulièrement enrichis. Parallèlement, le profil d’expression génique montrait que le TGFβ n’activait plus seulement des programmes bien connus comme la transition épithélio–mésenchymateuse (liée à l’invasion) et des réorientations métaboliques ; dans les cellules HRAS-mutantes, il stimulait aussi des gènes impliqués dans la réplication de l’ADN, la réparation de l’ADN et la progression à travers des points de contrôle clés du cycle cellulaire.
SOX4, un intermédiaire moléculaire
En creusant davantage, les chercheurs ont montré que SOX4 occupe le cœur de ce basculement. Les données de séquençage ARN unicellulaire provenant de tumeurs mammaires primaires ont révélé que SOX4 est co-exprimé avec des moteurs du cycle cellulaire tels que CDK4, CDK6 et cycline D1 (CCND1), en particulier dans les cellules cancéreuses en division active. Dans leurs modèles 3D, le TGFβ augmentait les niveaux de SOX4, et SOX4 était retrouvé lié près des régions de contrôle de ces gènes du cycle cellulaire, en particulier CDK4. Lorsque SOX4 était réduit par des outils génétiques, le TGFβ ne parvenait plus à activer efficacement bon nombre de ses gènes cibles, y compris ceux liés à la division cellulaire et au remodelage tissulaire, et les sphères de type cancéreux devenaient moins invasives et plus stables. Des expériences biochimiques ont en outre démontré que SOX4 coopère avec SMAD3, un transducteur clé du signal TGFβ, formant un module coopératif dans le noyau qui amplifie l’activation génique.
Saper un médicament de première ligne contre le cancer du sein
Le palbociclib est un médicament largement utilisé qui bloque CDK4 et CDK6, des protéines qui poussent les cellules d’un état quiescent vers la division active. De nombreuses patientes développent finalement une résistance à ce traitement. Les auteurs ont combiné de vastes jeux de données de réponse aux médicaments avec des expériences en laboratoire sur plusieurs lignées cellulaires mammaires et cultures 3D. Ils ont constaté qu’une activité TGFβ plus forte, associée à SOX4 et à des signatures géniques apparentées, coïncide avec des doses de palbociclib plus élevées nécessaires pour inhiber la croissance. En laboratoire, l’ajout de TGFβ rendait les cellules cancéreuses moins sensibles au palbociclib, tandis que le blocage de la signalisation TGFβ ou l’abaissement de SOX4 restaurait la sensibilité. Une exposition prolongée au palbociclib a produit des lignées résistantes présentant une signalisation TGFβ renforcée, des niveaux accrus de SOX4 et des marques de chromatine active plus marquées au niveau du gène SOX4 lui-même. Dans des modèles de poisson-zèbre, l’inhibition du TGFβ réduisait substantiellement la croissance de tumeurs dérivées de cellules résistantes au palbociclib. 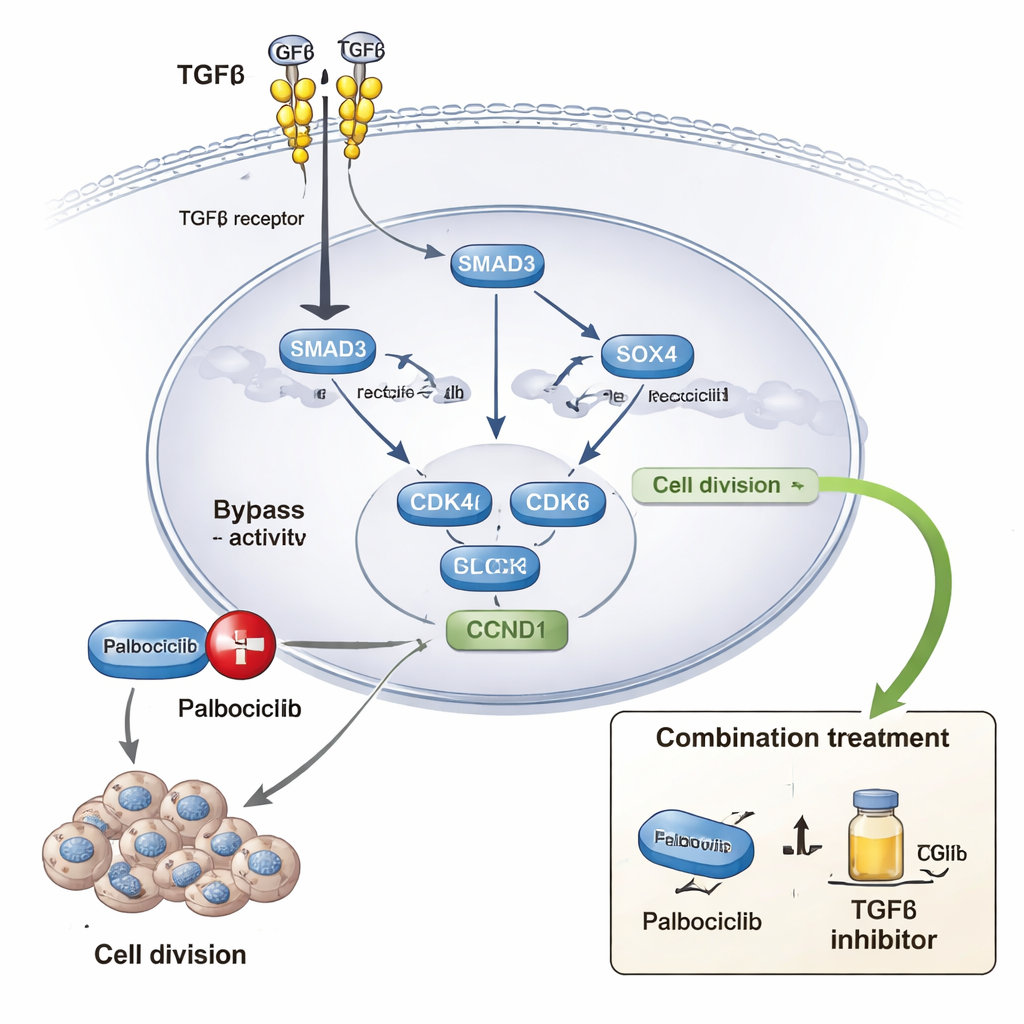
Ce que cela signifie pour les patientes et les thérapies futures
Pour un non-spécialiste, le message principal est qu’un signal destiné à nous protéger du cancer peut, dans un contexte inapproprié, être coopté pour aider les tumeurs à survivre et à déjouer les médicaments. Ici, le TGFβ s’allie à SOX4 pour ouvrir des régions cruciales du génome, activer des moteurs du cycle cellulaire comme CDK4 et CDK6, et atténuer l’efficacité du palbociclib. Ces résultats suggèrent que, pour certains cancers du sein, combiner des inhibiteurs CDK4/6 avec des médicaments bloquant la signalisation TGFβ — ou ciblant les programmes pilotés par SOX4 — pourrait retarder ou surmonter la résistance. Bien que des travaux cliniques supplémentaires soient nécessaires, cette étude cartographie une voie d’échappement moléculaire détaillée utilisée par les cellules cancéreuses et indique de nouvelles approches pour l’interrompre.
Citation: Ali, M.M., Itoh, Y., Badji, A.M.P. et al. TGFβ signaling promotes cell cycle progression and resistance to the CDK4/6 inhibitor palbociclib through SOX4 transcriptional modulation in breast cancer cells. Cell Death Dis 17, 209 (2026). https://doi.org/10.1038/s41419-026-08435-4
Mots-clés: cancer du sein, signalisation TGF-bêta, SOX4, résistance au palbociclib, cycle cellulaire