Clear Sky Science · fr
BCL-xL comme cible thérapeutique dans le cancer colorectal réfractaire au cetuximab
Pourquoi cela importe pour les personnes atteintes d’un cancer du côlon
Le cancer colorectal (du côlon et du rectum) est l’un des cancers les plus fréquents dans le monde, et de nombreux patients atteints de formes avancées reçoivent un anticorps ciblé appelé cetuximab. Ce médicament peut faire diminuer les tumeurs au début, mais chez la plupart des patients le cancer trouve des moyens d’échapper au traitement en quelques mois, laissant peu d’options satisfaisantes aux médecins. Cette étude pose une question cruciale : lorsque les tumeurs colorectales ne répondent plus au cetuximab, existe-t-il un autre point faible que de nouveaux médicaments peuvent exploiter pour provoquer la mort des cellules cancéreuses ?
Quand un médicament ciblé cesse de fonctionner
Le cetuximab agit en bloquant une antenne de surface sur les cellules cancéreuses appelée récepteur du facteur de croissance épidermique (EGFR), qui stimule leur croissance. L’équipe a créé un modèle de laboratoire de résistance en exposant une lignée cellulaire colorectale sensible (LIM1215) à des doses progressivement croissantes de cetuximab pendant six mois. Deux populations cellulaires résistantes, dérivées indépendamment, sont apparues et ont continué de croître même à des concentrations élevées du médicament, tout en retrouvant un aspect aussi sain et une croissance aussi rapide que les cellules d’origine lorsque le médicament était retiré. Fait important, les cellules résistantes portaient toujours la cible du médicament à leur surface et le cetuximab pouvait encore s’y lier, ce qui suggère que le cancer ne s’était pas simplement « caché » ni n’avait modifié le récepteur.
Les cellules résistantes contournent les signaux de croissance
Pour comprendre comment les cellules contournent l’effet du cetuximab, les chercheurs ont examiné les voies de croissance clés à l’intérieur de la cellule. Dans les cellules parentales, le cetuximab atténuait normalement la voie MAPK, un moteur majeur de la division cellulaire. Dans les cellules résistantes, l’activité MAPK restait élevée même lorsque l’EGFR était bloqué, montrant que le signal de croissance avait été découplé du récepteur d’origine. Le séquençage de l’ARN cellulaire a révélé de nouvelles mutations activatrices dans un autre gène RAS, HRAS, dans des sous-populations des cellules résistantes, mais pas dans d’autres suspects habituels tels que KRAS, NRAS ou BRAF. Les tentatives pour inhiber ce signal de rechange avec un inhibiteur de MEK (qui agit en aval de RAS) n’ont réduit la croissance que modestement. Cela a souligné que, plutôt que de courir après chaque nouvelle mutation, il pourrait être plus efficace d’attaquer la machinerie cellulaire de la vie ou de la mort partagée par différents clones résistants. 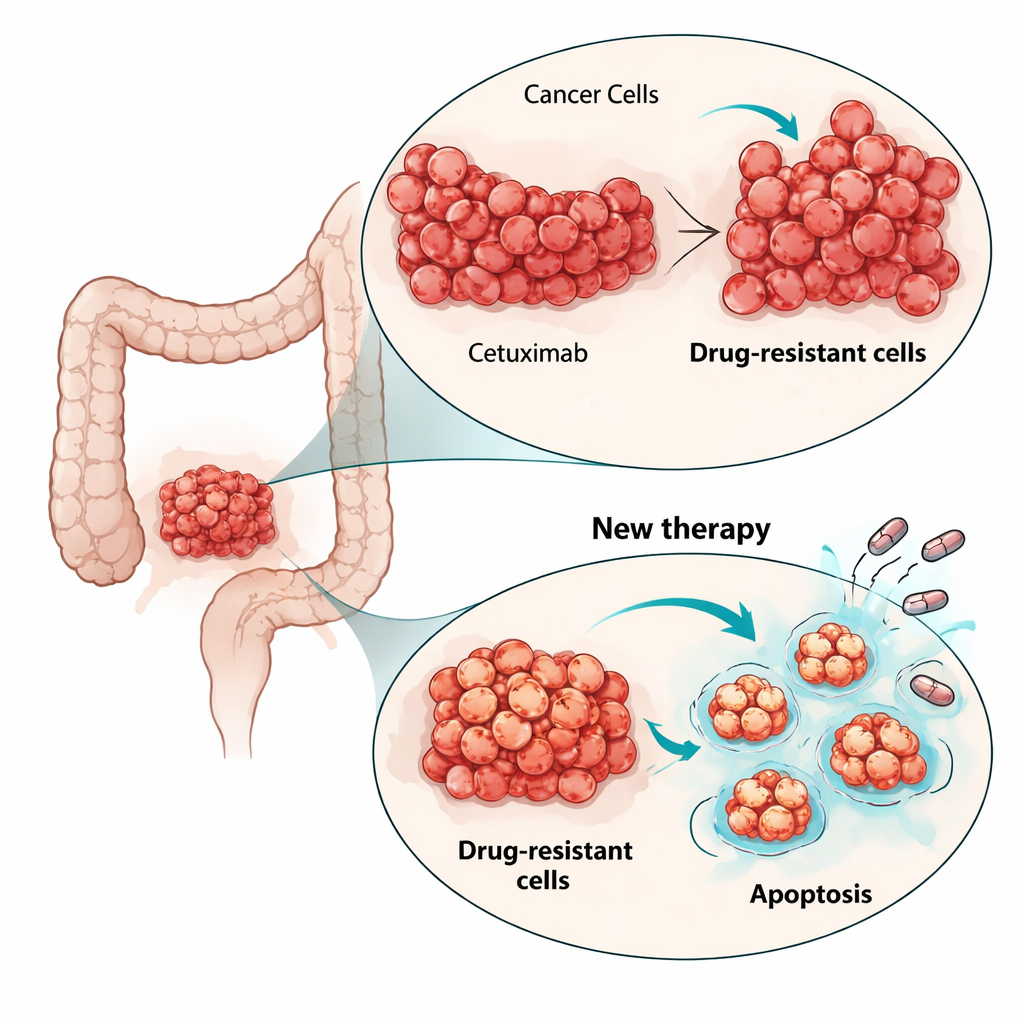
Toucher le système de survie des cellules cancéreuses
Les scientifiques ont orienté leur attention vers l’apoptose, le programme de suicide cellulaire intégré que les cancers suppriment souvent. L’analyse de l’expression génique a montré que les voies liées à l’apoptose étaient altérées dans les cellules résistantes. En particulier, la protéine anti‑mort BCL-xL était plus élevée dans une population résistante et légèrement augmentée dans l’autre, tandis qu’une autre protéine de survie, MCL-1, était également présente. L’équipe a testé des petites molécules appelées mimétiques BH3, conçues pour bloquer ces protéines de survie et libérer la machinerie de mort. En culture bidimensionnelle, les trois lignées cellulaires — parentale et résistantes — étaient sensibles aux médicaments bloquant BCL-xL ou MCL-1, mais, de façon frappante, des doses plus faibles tuaient les cellules résistantes au cetuximab plus efficacement. L’ajout d’une faible dose de l’inhibiteur du protéasome bortézomib, qui favorise l’accumulation de signaux pro‑mort, a renforcé la mort cellulaire, en particulier en combinaison avec le bloqueur de MCL-1.
Des plats plats aux mini‑tumeurs 3D et aux tissus de patients
Étant donné que les couches cellulaires plates ne reproduisent pas entièrement les tumeurs in vivo, l’équipe a ensuite cultivé les cellules sous forme de sphéroïdes tridimensionnels incorporés dans un gel, reflétant mieux l’architecture et les défis de pénétration des médicaments des tumeurs réelles. Là encore, le blocage de BCL-xL ou de MCL-1 a réduit la viabilité des sphéroïdes, et la combinaison de ces médicaments avec le bortézomib a provoqué des baisses spectaculaires de l’activité métabolique et des signes évidents de mort cellulaire. Pour tester si cette vulnérabilité existe dans des tissus tumoraux humains plus réalistes, ils ont utilisé des tranches minces de cancers colorectaux résistants au cetuximab, cultivées chez la souris à partir de tumeurs de patients (xénogreffes dérivées de patients). Ces modèles étaient tous de type sauvage pour KRAS comme les cellules LIM1215 d’origine mais portaient des mutations additionnelles diverses, y compris dans BRAF et TP53, reflétant la variété génétique observée en clinique. 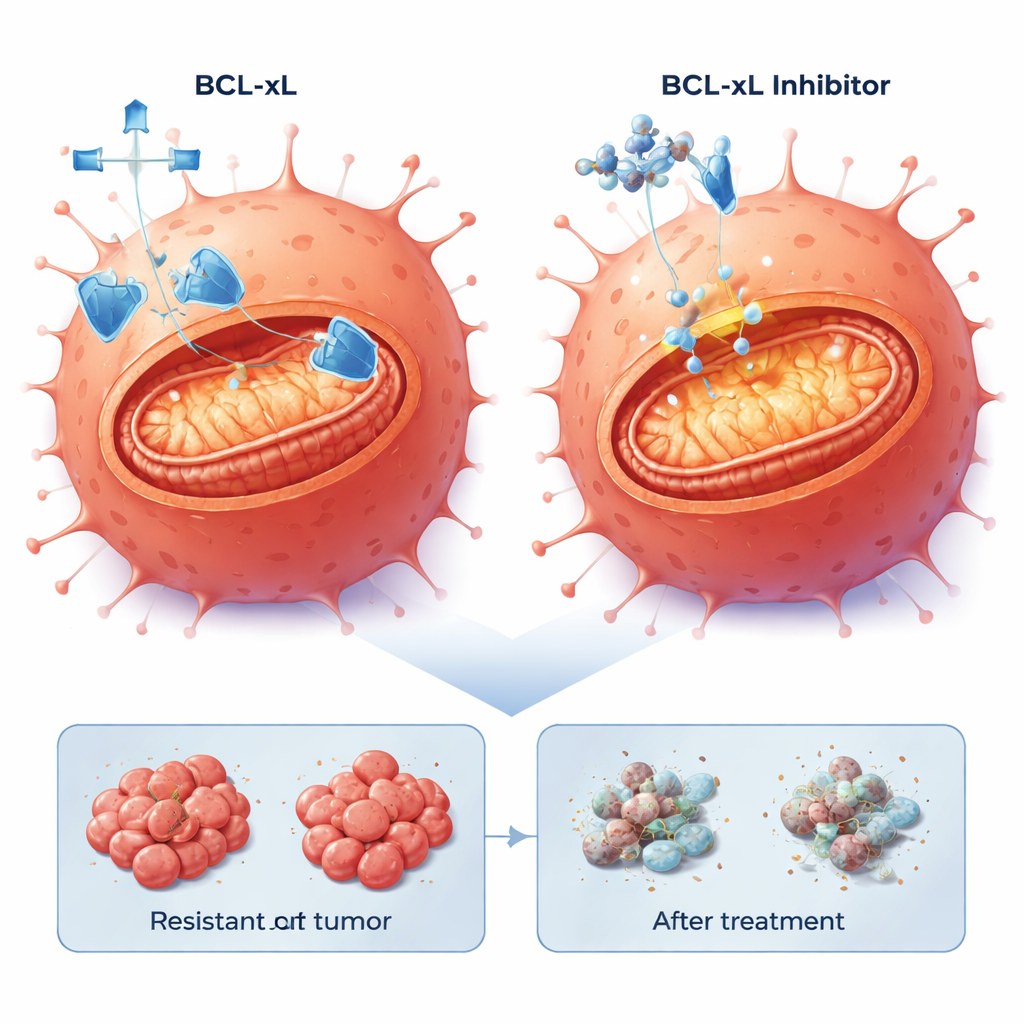
Le ciblage de BCL-xL fonctionne à travers des tumeurs résistantes diverses
Dans ces tranches tumorales dérivées de patients, la combinaison d’un inhibiteur de BCL-xL avec une faible dose de bortézomib a déclenché de façon constante une mort cellulaire robuste dans 20–40 % des cellules tumorales à travers quatre modèles différents, y compris ceux porteurs de mutations agressives de BRAF. En revanche, le blocage de MCL-1 avec bortézomib n’a produit des effets forts que dans un sous‑ensemble de tumeurs. Fait important, la capacité des cellules résistantes à subir l’apoptose était préservée : une fois le filet de sécurité BCL-xL retiré, le programme interne de mort pouvait encore être activé, indépendamment de la voie génétique spécifique par laquelle la tumeur avait échappé au cetuximab.
Ce que cela signifie pour les patients
Pour les personnes dont le cancer colorectal ne répond plus au cetuximab, cette étude apporte un optimisme prudent. Elle suggère que même après que les tumeurs deviennent résistantes à la thérapie ciblant l’EGFR, de nombreuses cellules cancéreuses restent prêtes à mourir si une protéine clé de survie, BCL-xL, est bloquée. Bien que les inhibiteurs de BCL-xL puissent avoir des effets secondaires, notamment sur les plaquettes sanguines, ce travail oriente vers des stratégies d’association et d’optimisation des doses qui pourraient limiter la toxicité tout en exploitant un talon d’Achille commun aux tumeurs difficiles à traiter. À l’avenir, des médicaments désarmant BCL-xL pourraient constituer l’armature de nouveaux traitements de seconde ligne pour le cancer colorectal réfractaire au cetuximab, moins dépendants du paysage mutationnel changeant de la tumeur.
Citation: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
Mots-clés: cancer colorectal, résistance aux médicaments, cetuximab, inhibition de BCL-xL, apoptose