Clear Sky Science · fr
LAP2α favorise la tumorigenèse mammaire en atténuant le stress de réplication
Pourquoi cela compte pour le cancer du sein
Les tumeurs mammaires croissent en partie parce que les cellules cancéreuses trouvent des moyens de survivre au stress constant qu’elles subissent lors de la copie de leur ADN. Cette étude révèle comment une protéine peu connue, appelée LAP2α, aide les cellules du cancer du sein à protéger leur ADN pendant la réplication, favorisant ainsi la croissance tumorale et rendant les cancers plus difficiles à traiter. Comprendre ce réseau de soutien caché suggère de nouvelles façons d’affaiblir les tumeurs et d’améliorer l’efficacité des traitements existants.
Un assistant caché à l’intérieur des noyaux tumoraux
À chaque division, une cellule doit copier son ADN avec précision. Dans les cellules cancéreuses, ce processus est particulièrement mis à rude épreuve : les signaux de croissance restent constamment activés et la machinerie de réplication est poussée à ses limites. Cette pression, appelée stress de réplication, laisse des segments d’ADN simple brin qui doivent être rapidement enrobés et stabilisés par un complexe protéique nommé RPA. Les auteurs avaient précédemment montré que LAP2α, une protéine associée au « charpente » interne du noyau, peut se lier à RPA et l’aider à atteindre l’ADN endommagé. Dans ce travail, ils ont cherché à savoir si ce partenariat LAP2α–RPA alimente réellement le développement des tumeurs mammaires et influence la réponse des tumeurs au traitement.
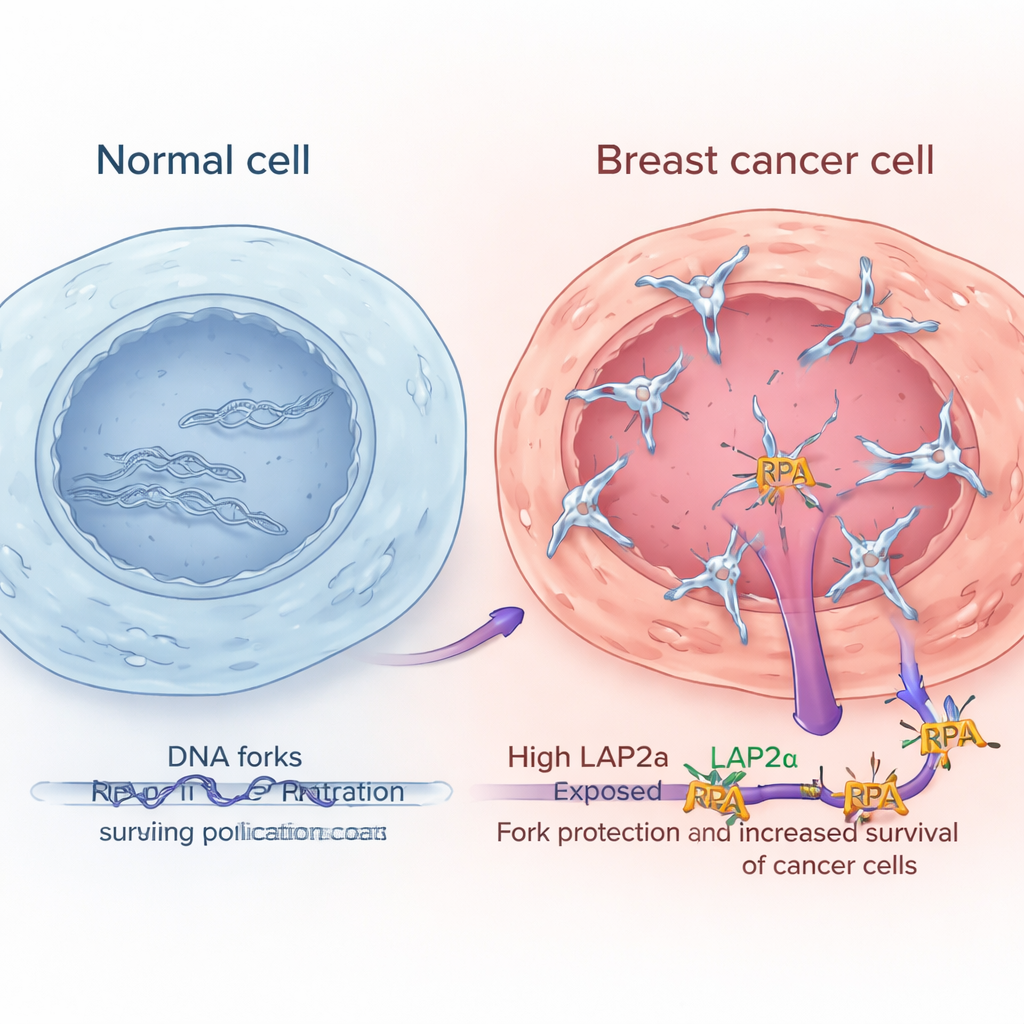
Des niveaux élevés de LAP2α caractérisent des tumeurs mammaires plus agressives
En analysant de larges bases de données publiques d’expression génique et en examinant des échantillons tumoraux au microscope, les chercheurs ont montré que LAP2α est systématiquement plus abondant dans les tissus cancéreux du sein que dans les tissus mammaires sains adjacents. Son expression augmente avec le grade tumoral, ce qui signifie que les cancers plus anormaux et agressifs ont tendance à présenter davantage de LAP2α. Ce schéma est apparu dans plusieurs sous-types majeurs du cancer du sein, y compris les tumeurs « hormono-réceptrices », enrichies en HER2 et triple négatives. Fait important pour les patients, ceux dont les tumeurs présentaient des niveaux élevés de LAP2α avaient tendance à avoir un pronostic de survie plus mauvais. En revanche, les composantes centrales de RPA elles‑mêmes n’affichaient pas de changements similaires ni d’associations nettes avec l’issue, ce qui suggère que c’est la fonction renforcée de LAP2α, plutôt que l’augmentation simple de RPA, qui aide les cellules cancéreuses à mieux faire face au stress de réplication.
Désactiver LAP2α ralentit les tumeurs et révèle leurs points faibles
Pour aller au‑delà des corrélations, l’équipe a utilisé des modèles murins de cancer du sein dans lesquels LAP2α pouvait être supprimée de façon sélective. Une fois les tumeurs mammaires formées, la suppression génétique de LAP2α a ralenti la croissance tumorale et prolongé la survie des animaux. Les cellules tumorales dépourvues de LAP2α se divisaient moins et présentaient davantage de signes de lésions de l’ADN, comme l’ont montré une augmentation de la coloration pour les marqueurs de cassures d’ADN et une réduction de l’enrobage par RPA. Lorsque ces cellules tumorales déficientes en LAP2α ont été transplantées chez de nouvelles souris, elles ont de nouveau formé des tumeurs plus petites et montré une sensibilité accrue aux chimiothérapies endommageant l’ADN, y compris le platine cisplatine et un inhibiteur de PARP. Des expériences similaires sur des lignées cellulaires humaines de cancer du sein ont confirmé que la réduction de LAP2α rendait les cellules plus vulnérables à plusieurs médicaments génotoxiques, tandis que la restauration d’un LAP2α normal — mais pas d’une forme mutante incapable de se lier à RPA — rétablissait à la fois la protection de l’ADN et la résistance aux traitements.
Comment LAP2α protège les brins d’ADN fragiles
Pour disséquer le mécanisme, les chercheurs ont recréé les étapes de liaison à l’ADN dans des essais en éprouvette. Ils ont mélangé RPA purifié, de l’ADN simple brin et soit LAP2α normal soit une variante incapable d’interagir avec RPA. Ils ont constaté que LAP2α augmentait directement l’efficacité avec laquelle RPA enrobait l’ADN simple brin et aidait RPA à étirer et stabiliser ces régions fragiles, agissant comme un chargeur ou chaperon. En présence d’ADN, RPA avait tendance à se détacher de LAP2α pour se fixer définitivement au simple brin, montrant que LAP2α ne fait pas partie du manteau protecteur final mais remet plutôt RPA à l’ADN. En l’absence d’une interaction fonctionnelle LAP2α–RPA, davantage de fourches de réplication s’effondraient, des cassures d’ADN s’accumulaient et les cellules cancéreuses étaient plus susceptibles de mourir, surtout lorsque des dommages supplémentaires étaient induits par la chimiothérapie.
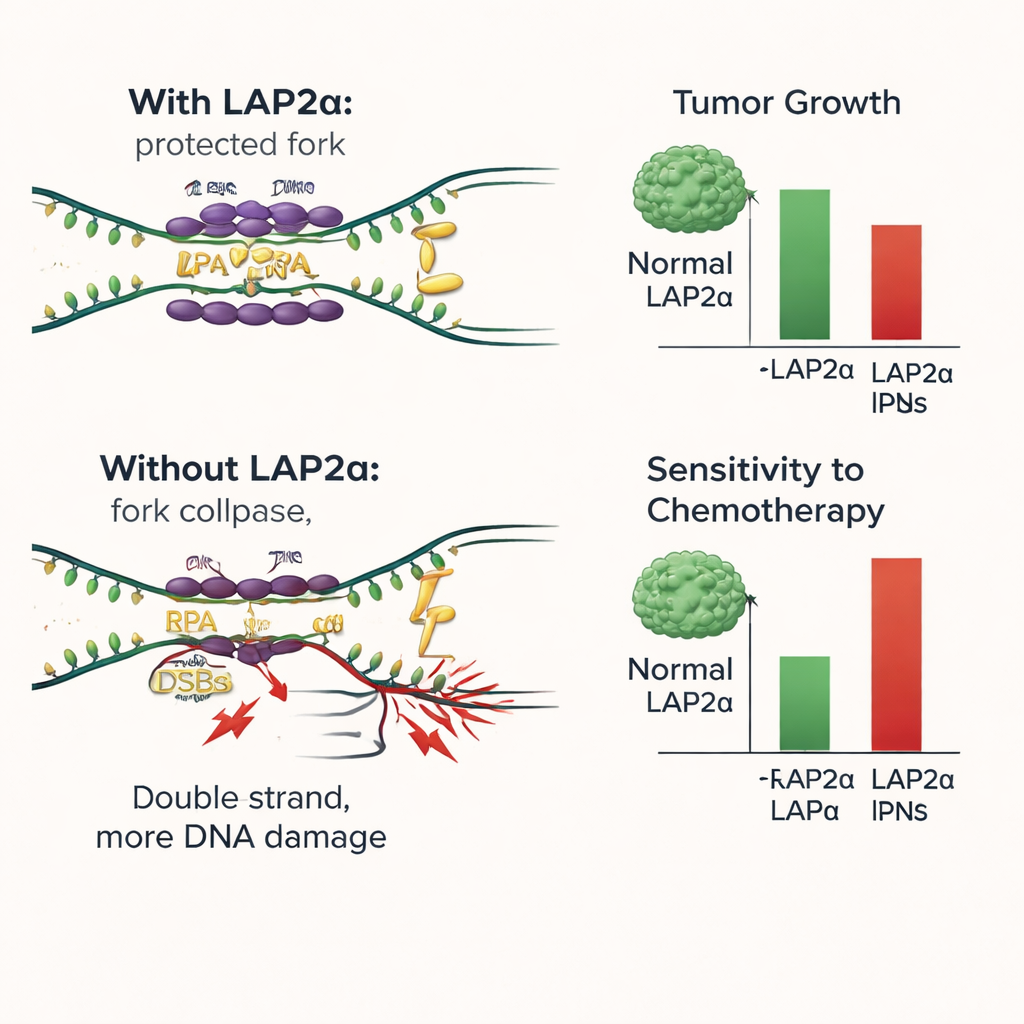
Ce que cela signifie pour le traitement futur du cancer du sein
Concrètement, cette étude montre que LAP2α agit comme un assistant en coulisse qui aide les cellules du cancer du sein à survivre à la tension imposée par la copie de leur ADN. En chargeant efficacement RPA sur l’ADN vulnérable, LAP2α réduit les lésions et soutient la croissance tumorale continue. En supprimer ou neutraliser son activité renverse la situation : les dommages à l’ADN s’accumulent, les cellules cessent de se diviser et les médicaments conventionnels qui visent l’ADN deviennent plus efficaces. Ces résultats suggèrent que LAP2α pourrait servir de marqueur de mauvais pronostic et de nouvelle cible thérapeutique. Des médicaments bloquant LAP2α ou son interaction avec RPA pourraient augmenter l’efficacité d’agents existants tels que les composés à base de platine et les inhibiteurs de PARP, notamment dans les tumeurs qui dépendent fortement de ce système d’amortissement du stress.
Citation: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
Mots-clés: cancer du sein, stress de réplication de l’ADN, LAP2 alpha, protéine de réplication A, sensibilité à la chimiothérapie