Clear Sky Science · fr
Cibler la biosynthèse des glycéro‑phospholipides surmonte la chimiorésistance induite par la perte de SLFN11 dans le sarcome d’Ewing
Pourquoi cette recherche compte pour les cancers pédiatriques
Le sarcome d’Ewing est un cancer rare mais agressif qui touche principalement les enfants et les adolescents. Beaucoup de patients répondent bien initialement à la chimiothérapie, mais lorsque la maladie récidive, les traitements actuels échouent souvent. Cette étude pose une question cruciale : quand les cellules du sarcome d’Ewing deviennent résistantes à la chimiothérapie, quels changements internes leur permettent de survivre — et ces changements peuvent‑ils constituer de nouvelles vulnérabilités exploitables par la médecine ?
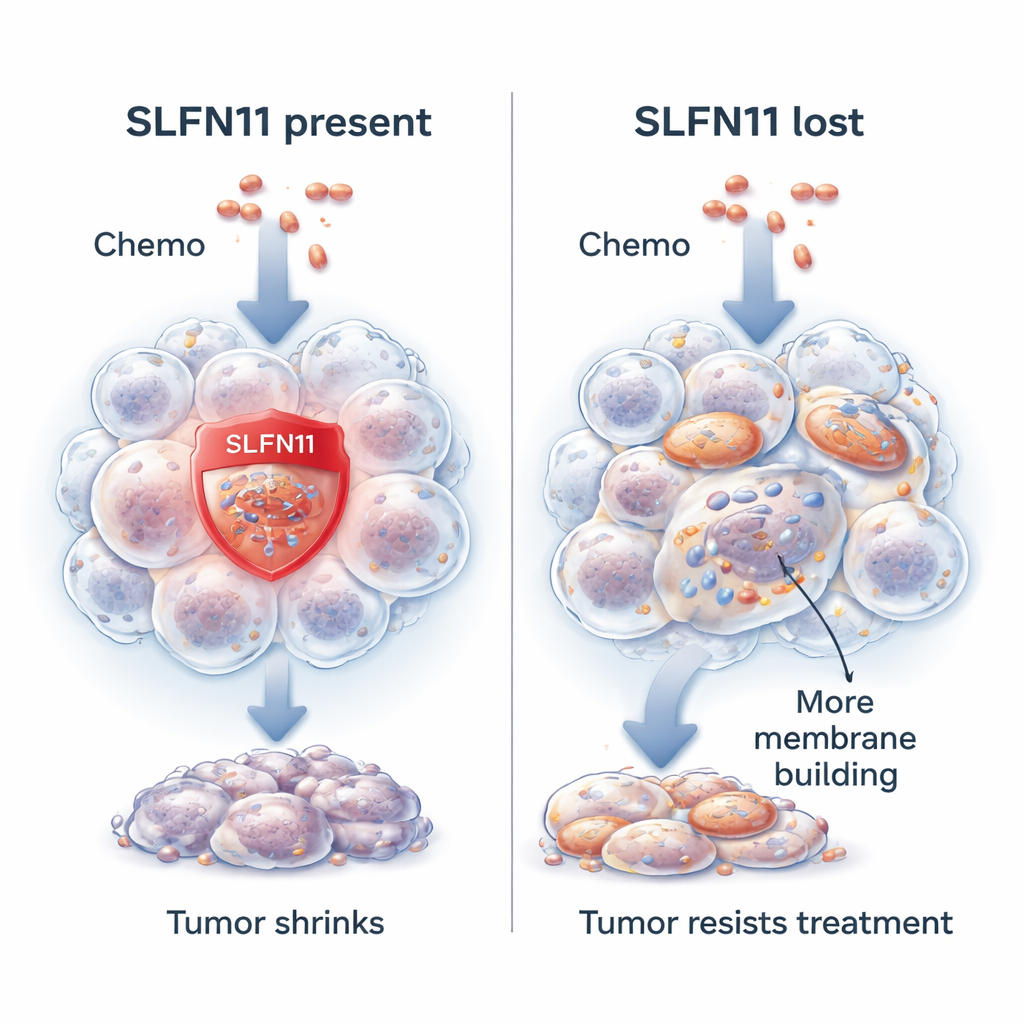
Un gène qui rend les cellules cancéreuses plus faciles à éliminer
Les chercheurs se concentrent sur un gène appelé SLFN11. Dans de nombreux tumeurs de sarcome d’Ewing, SLFN11 est fortement exprimé et rend les cellules cancéreuses beaucoup plus sensibles aux médicaments qui endommagent l’ADN, le plan génétique de la cellule. Lors de l’administration de ces médicaments, SLFN11 contribue à bloquer la réparation de l’ADN et pousse la cellule cancéreuse vers la mort. Les patients dont les tumeurs présentent des niveaux élevés de SLFN11 ont tendance à vivre plus longtemps et à mieux répondre au traitement. Cependant, environ un cancer sur dix commence avec peu ou pas de SLFN11 ou perd ce gène au cours de la thérapie. Lorsque cela se produit, la même chimiothérapie devient beaucoup moins efficace, alors que les cellules cancéreuses conservent pleinement leur capacité de prolifération.
Comment les cellules cancéreuses réorientent leur usage des carburants et des lipides
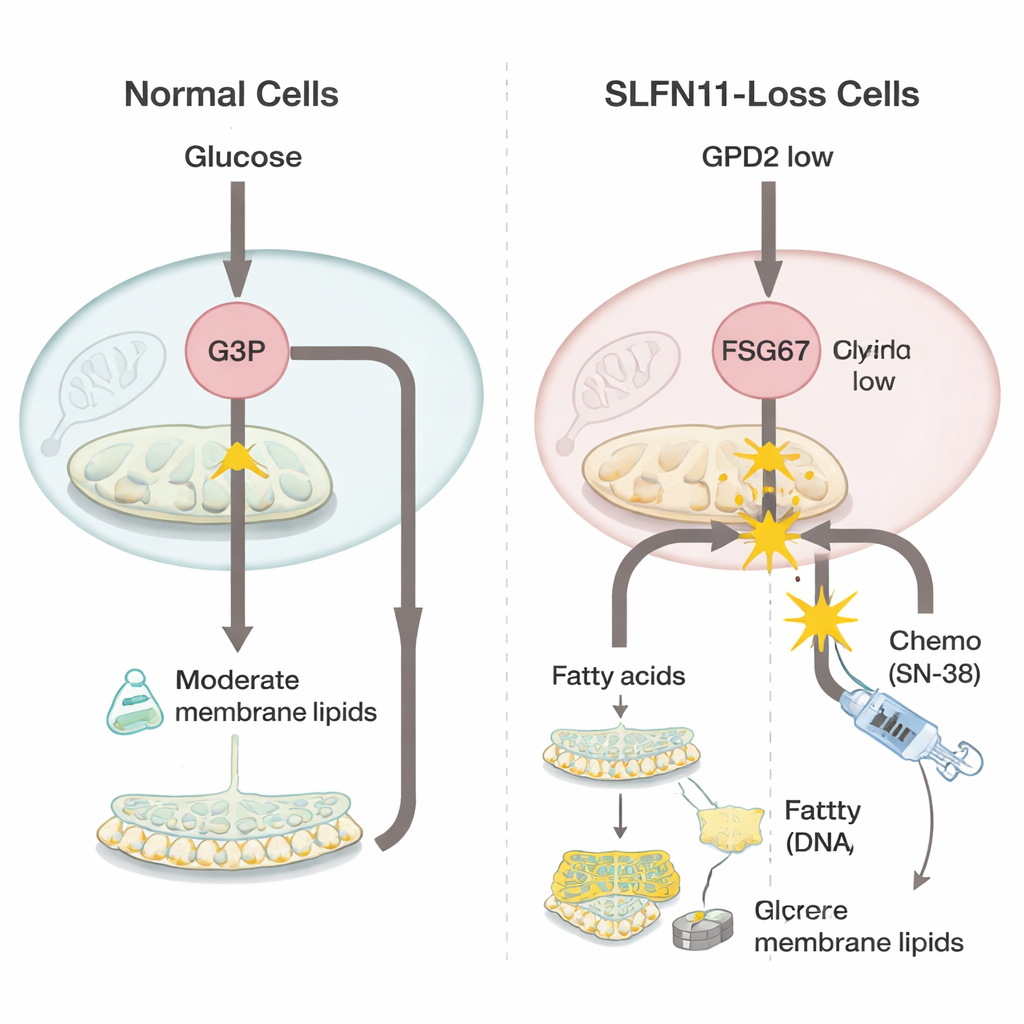
Pour comprendre ce qui change quand SLFN11 est perdu, l’équipe a comparé des cellules de sarcome d’Ewing avec et sans ce gène en utilisant de puissants outils « omiques » qui mesurent des milliers de gènes et de petites molécules simultanément. Ils ont découvert que les cellules dépourvues de SLFN11 réduisent l’expression d’une enzyme mitochondriale appelée GPD2, qui participe normalement à l’oxydation du glycérol‑3‑phosphate dans la production d’énergie. Quand GPD2 diminue, le glycérol‑3‑phosphate s’accumule. Plutôt que d’être perdu, ce bloc de construction supplémentaire est détourné vers la synthèse de davantage de molécules grasses qui composent les membranes cellulaires, un groupe connu sous le nom de glycéro‑phospholipides. Les cellules montraient aussi des signes d’augmentation des acides gras insaturés, plus flexibles, ce qui peut aider les tumeurs à croissance rapide à s’adapter au stress.
Transformer une astuce de survie en point faible
Parce que ces cellules déficientes en SLFN11 misent davantage sur la construction de membranes, les scientifiques ont testé si bloquer ce processus pouvait rétablir la sensibilité à la chimiothérapie. Ils ont utilisé un composé nommé FSG67, qui inhibe une étape clé de la production des glycéro‑phospholipides. Seul, le médicament standard endommageant l’ADN SN‑38 était devenu beaucoup moins puissant dans les cellules dépourvues de SLFN11, reflétant le problème clinique de résistance. Mais lorsque SN‑38 a été combiné avec FSG67, les cellules auparavant résistantes ont été beaucoup plus affectées, et les deux médicaments ont agi de façon synergiques, au‑delà de leurs effets individuels attendus. En revanche, dans les cellules qui conservaient SLFN11 et étaient déjà très sensibles à SN‑38, l’ajout de FSG67 apportait peu d’avantage supplémentaire et pouvait même être légèrement contre‑productif. Ce schéma suggère que la nouvelle dépendance à la synthèse lipidique et membranaire est spécifique à l’état résistant et à faible SLFN11.
Un signal potentiellement non invasif de tumeurs difficiles à traiter
Les chercheurs ont ensuite demandé si ce reparamétrage métabolique pouvait être détecté dans de véritables tumeurs, et pas seulement dans des cultures cellulaires. Ils ont fait croître des tumeurs de sarcome d’Ewing chez la souris, avec ou sans SLFN11, et ont utilisé la résonance magnétique nucléaire (RMN) pour analyser la composition chimique des extraits tumoraux. Les tumeurs dépourvues de SLFN11 présentaient un ratio plus élevé de deux molécules contenant de la choline liées au renouvellement membranaire : la phosphocholine et la glycéro‑phosphocholine. Un rapport phosphocholine/glycéro‑phosphocholine élevé a été associé dans d’autres cancers à un comportement plus agressif et à une moins bonne réponse au traitement. Comme les signaux de choline peuvent être mesurés par des techniques d’imagerie avancées, ce type de basculement pourrait un jour servir de marqueur non invasif pour repérer les tumeurs de sarcome d’Ewing ayant adopté ce mode résistant axé sur la synthèse membranaire.
Ce que cela pourrait signifier pour les traitements futurs
Dans l’ensemble, l’étude montre que lorsque les cellules du sarcome d’Ewing perdent SLFN11 et deviennent moins sensibles aux chimiothérapies mésurant l’ADN, elles compensent en réorientant leur métabolisme vers la production de davantage de lipides membranaires. Ce changement n’aide pas seulement les cellules à survivre ; il crée aussi un nouveau talon d’Achille. Bloquer la production de glycéro‑phospholipides avec une molécule comme FSG67 peut partiellement restaurer l’efficacité cytotoxique de la chimiothérapie dans ces cellules résistantes. Bien que FSG67 ne soit pas encore un médicament clinique, ces travaux indiquent une stratégie potentielle où les cliniciens pourraient un jour caractériser les tumeurs des patients selon le statut SLFN11 et les traits métaboliques, puis associer des thérapies délétères pour l’ADN avec des inhibiteurs ciblés de la synthèse lipidique et membranaire pour surmonter la résistance.
Citation: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Mots-clés: Sarcome d’Ewing, chimiorésistance, SLFN11, métabolisme du cancer, biosynthèse des lipides