Clear Sky Science · fr
Cibler l’IGFBP2 exosomal hypoxique surmonte l’évasion immunitaire médiée par CD47 dans le glioblastome
Pourquoi priver les tumeurs d’oxygène peut se retourner contre nous
Les médecins savent depuis longtemps que le glioblastome, un cancer cérébral mortel, se développe souvent dans des régions pauvres en oxygène. Ces poches hypoxiques rendent la tumeur plus difficile à traiter. Cette étude montre comment le faible apport en oxygène aide les cellules cancéreuses à se dissimuler du système immunitaire et propose une nouvelle combinaison thérapeutique susceptible de faciliter leur élimination par l’organisme.
Une tumeur cérébrale mortelle qui échappe à nos défenses
Le glioblastome est la tumeur cérébrale la plus agressive et la plus fréquente chez l’adulte, avec une survie typique mesurée en mois. Bien que des cellules immunitaires infiltrent ces tumeurs, les cellules cancéreuses échappent souvent à la destruction. Une voie d’évasion clé repose sur une protéine de surface appelée CD47, parfois qualifiée de signal « ne me mangez pas », qui indique aux cellules immunitaires voisines, comme les macrophages, de ne pas engloutir et détruire la cellule tumorale. Des médicaments bloquant CD47 sont déjà en essai, mais les résultats dans les tumeurs solides comme le glioblastome ont été mitigés, ce qui suggère que d’autres facteurs du microenvironnement tumoral peuvent compromettre ces thérapies.
Zones hypoxiques et petites parcelles cancéreuses
Au moyen du séquençage ARN unicellulaire, les chercheurs ont cartographié des milliers de cellules issues de différentes régions d’échantillons de glioblastome, en comparant le noyau tumoral pauvre en oxygène à sa périphérie. Ils ont identifié un sous-type cellulaire particulièrement agressif dans le noyau hypoxique, appelé cellules GBM de type mésenchymateux, qui exprimait fortement CD47 et une protéine nommée IGFBP2. Parallèlement, ils ont découvert que ces cellules centrales libéraient un grand nombre de vésicules nanoscopiques connues sous le nom d’exosomes, qui portaient IGFBP2 à leur surface. Comme les exosomes peuvent voyager dans le cerveau et même atteindre la circulation sanguine, ils peuvent diffuser des signaux bien au-delà de leur lieu d’origine. 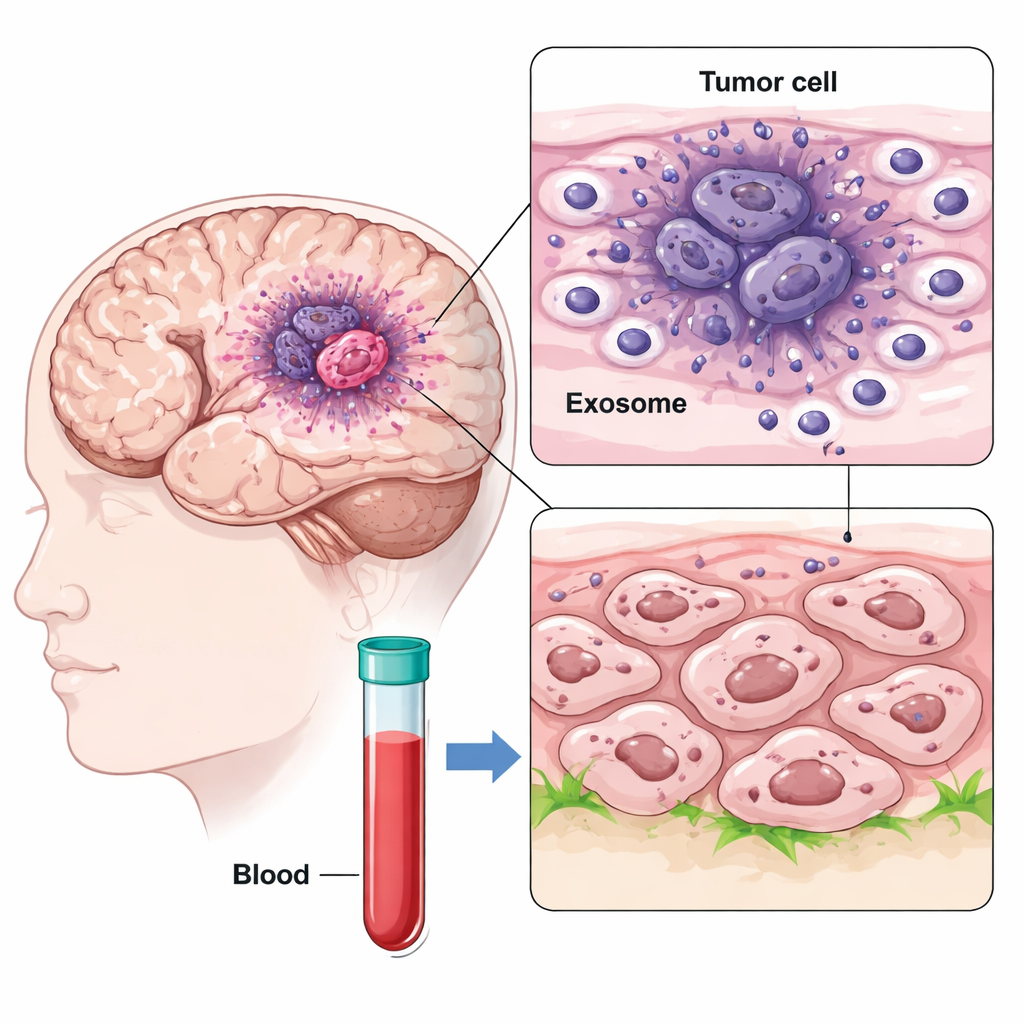
Comment une protéine partenaire renforce le signal « ne me mangez pas »
L’équipe a ensuite étudié le rôle de l’IGFBP2. Ils ont montré que, en conditions d’hypoxie, une protéine capteur d’hypoxie nommée HIF-2α active le gène IGFBP2 dans les cellules tumorales. IGFBP2 se lie alors à des récepteurs spécifiques appelés intégrines à la surface des exosomes, en en recouvrant la membrane externe. Lorsque ces exosomes enduits d’IGFBP2 fusionnent avec d’autres cellules tumorales, ils déclenchent une cascade de signaux intracellulaires impliquant des protéines telles que FAK et STAT3. Cette cascade augmente finalement la quantité de CD47 à la surface des cellules tumorales, renforçant le message « ne me mangez pas » auprès des macrophages et protégeant davantage les cellules cancéreuses contre l’attaque immunitaire. 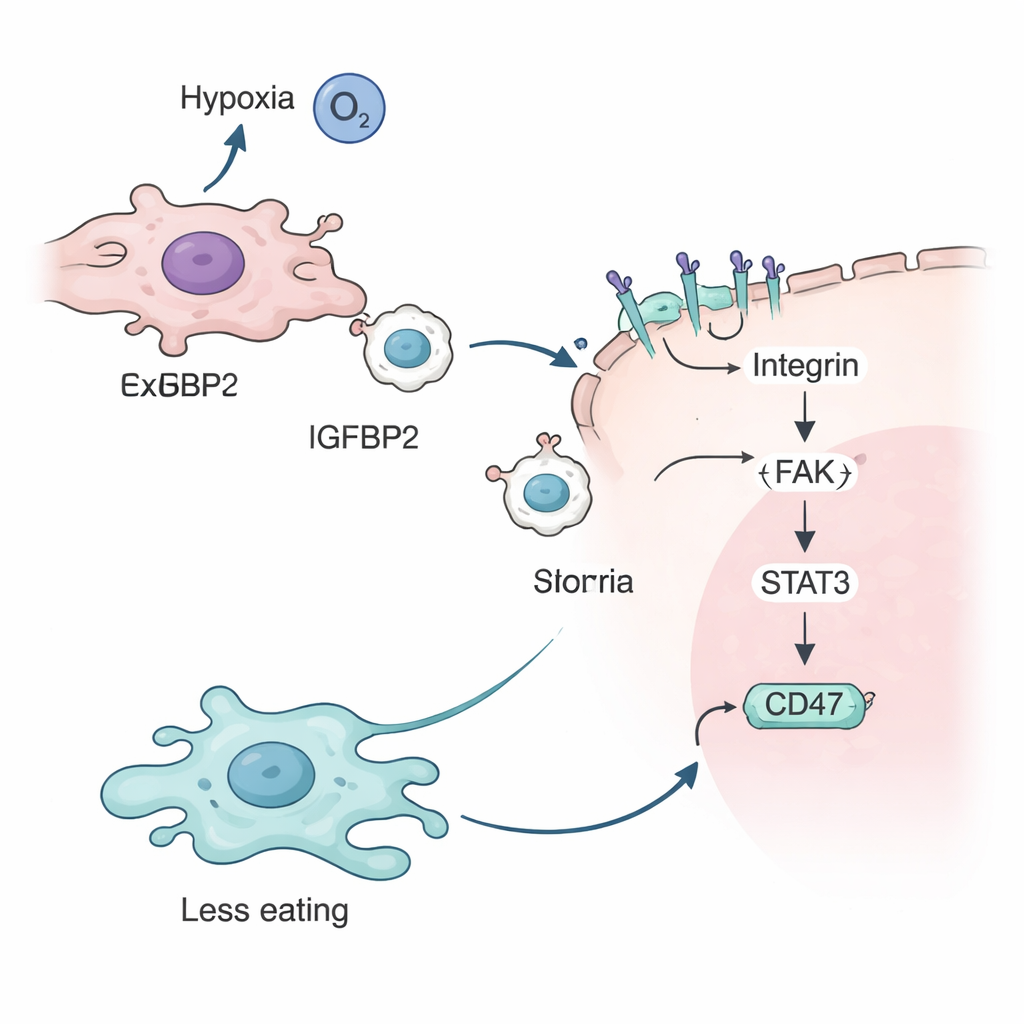
Preuves issues d’échantillons de patients et de modèles animaux
Pour relier ces observations de laboratoire à la maladie réelle, les chercheurs ont examiné des tissus tumoraux et du sang de personnes atteintes de gliome. Ils ont constaté que les niveaux d’IGFBP2 étaient plus élevés à la fois dans les tumeurs et dans les exosomes sanguins des patients présentant une maladie plus avancée, ce qui suggère que les exosomes positifs pour IGFBP2 pourraient servir de marqueur sanguin du grade tumoral. Dans des modèles murins, la réduction de l’IGFBP2 dans les cellules de glioblastome les rendait plus vulnérables à l’élimination par les macrophages, ralentissait la croissance tumorale et prolongeait la survie. À l’inverse, l’ajout d’exosomes riches en IGFBP2 augmentait les niveaux de CD47, réduisait la phagocytose par les cellules immunitaires et accélèrait la progression tumorale.
Un coup de poing thérapeutique prometteur en deux temps
Enfin, l’équipe a testé si le blocage de l’IGFBP2 pouvait renforcer l’efficacité d’une thérapie ciblant CD47. Chez la souris porteuse de tumeurs cérébrales, un traitement par anticorps contre l’IGFBP2 et CD47 a stimulé l’activité des macrophages, réduit la taille des tumeurs et prolongé la survie, plus efficacement que chaque traitement pris isolément. En interrompant le signal IGFBP2 induit par l’hypoxie et en bloquant directement le signal « ne me mangez pas » de CD47, cette thérapie combinée a attaqué le camouflage immunitaire de la tumeur sur deux fronts. Pour les patients, ces résultats suggèrent que la mesure d’IGFBP2 dans les exosomes circulants pourrait aider à identifier ceux les plus susceptibles de bénéficier d’une immunothérapie ciblant CD47, et que l’association d’inhibiteurs d’IGFBP2 et de CD47 pourrait constituer une stratégie plus puissante contre le glioblastome que chaque médicament utilisé seul.
Citation: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
Mots-clés: glioblastome, exosomes, évasion immunitaire, CD47, hypoxie