Clear Sky Science · fr
HSPA5 favorise la stabilité de YAP/TAZ indépendamment de la voie Hippo et induit une transition proneurale‑vers‑mésenchymateuse dans le glioblastome
Pourquoi cette étude sur le cancer du cerveau est importante
Le glioblastome est l’un des cancers du cerveau les plus meurtriers, en partie parce que de nombreuses tumeurs évoluent au fil du temps vers un état plus résistant aux traitements. Cette étude révèle comment une protéine courante de la réponse au stress, HSPA5, contribue à cette transition et prolonge la survie de molécules favorisant la tumeur. Comprendre cette « astuce de survie » suggère de nouvelles approches pour rendre le glioblastome moins agressif et plus sensible aux thérapies existantes.
Une tumeur qui change de « personnalité »
Les cliniciens et les chercheurs reconnaissent aujourd’hui que le glioblastome n’est pas une maladie unique, mais un mélange de sous‑types moléculaires. Deux grands profils se distinguent : une forme « proneurale », généralement un peu moins agressive, et une forme « mésenchymateuse », plus invasive, résistante aux traitements et associée à des récidives plus précoces. Les tumeurs peuvent évoluer du statut proneurale vers le statut mésenchymateux, un processus que les auteurs appellent transition proneurale‑vers‑mésenchymateuse, ou PMT. L’équipe a cherché quelles protéines de la réponse au stress pourraient pousser les tumeurs le long de cette voie dangereuse.
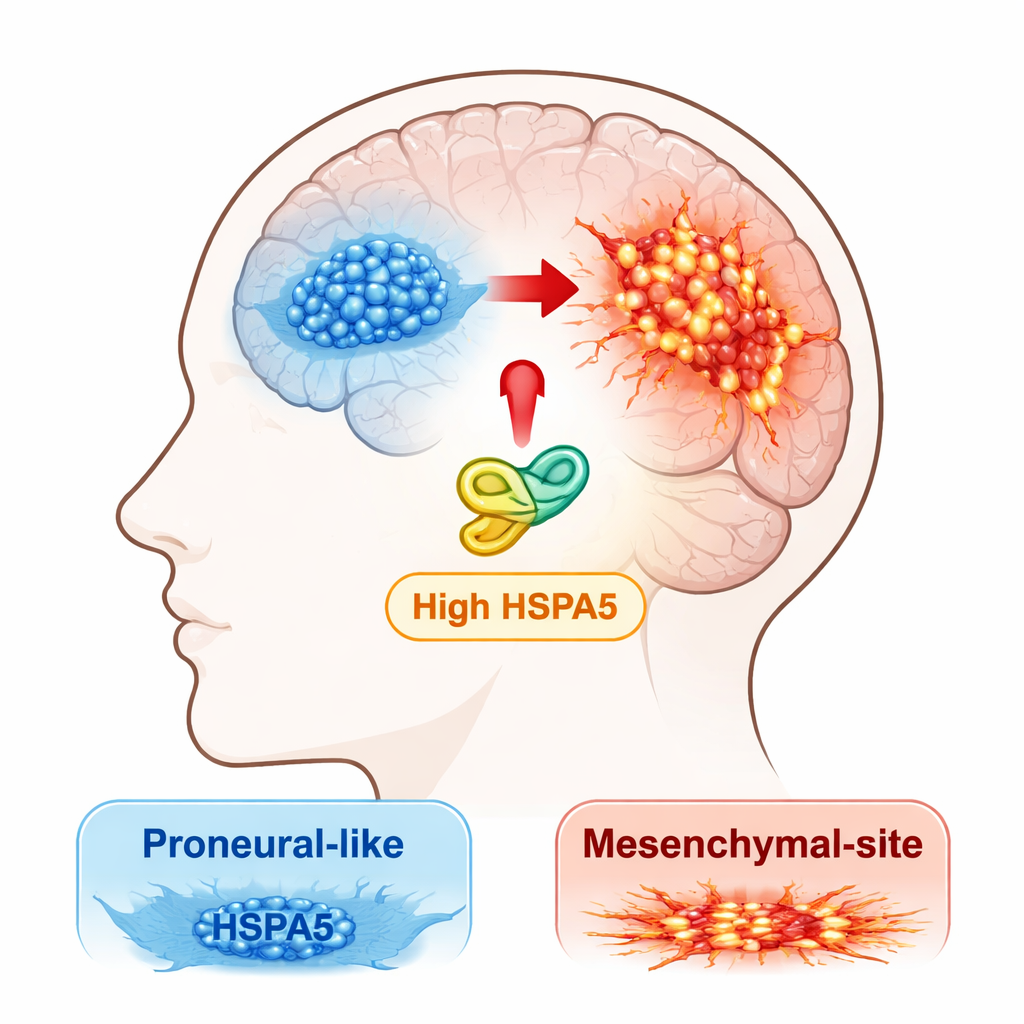
Une protéine aide‑stress au centre de l’attention
Les chercheurs ont commencé par analyser de larges jeux de données publiques sur le cancer et leurs propres échantillons de patients pour repérer les membres de la famille HSP70, un groupe de protéines « chaperonnes » qui aident d’autres protéines à se replier et à survivre sous stress. Une chaperonne, HSPA5, est ressortie. Son activité était maximale dans le sous‑type mésenchymateux du glioblastome et nettement plus élevée dans les tumeurs que dans le tissu cérébral normal. Les patients dont les tumeurs exprimaient davantage HSPA5 avaient tendance à avoir une survie globale plus faible, ce qui en fait un candidat probable pour être un moteur de l’agressivité plutôt qu’un simple passager.
Forcer les cellules à devenir plus agressives
Pour explorer le rôle exact de HSPA5 dans les cellules tumorales, l’équipe a cultivé des cellules primaires de glioblastome prélevées directement chez des patients et les a séparées en groupes à profil proneural et à profil mésenchymateux. Lorsqu’ils ont forcé les cellules proneurales à exprimer davantage de HSPA5, ces cellules ont commencé à se comporter davantage comme des cellules mésenchymateuses : elles proliféraient plus rapidement, migrèrent et envahirent plus facilement, et exprimèrent des marqueurs mésenchymateux caractéristiques tels que CD44 et c‑MET, tout en réduisant l’expression de marqueurs proneuronaux comme SOX2 et OLIG2. L’effet inverse était également vrai : diminuer HSPA5 dans des cellules mésenchymateuses atténuait leur croissance et leur invasivité et les ramenait partiellement vers un profil moins agressif.
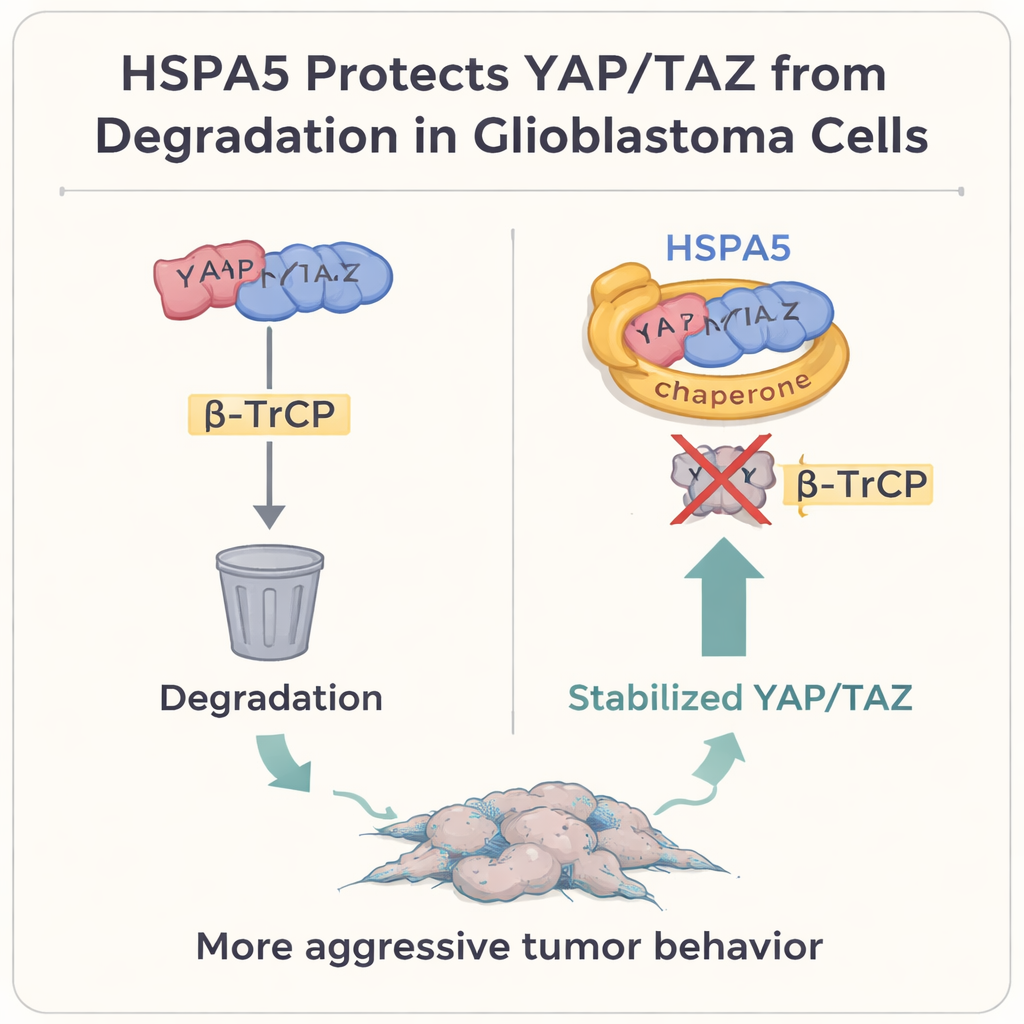
Protéger des commutateurs de croissance clés de la poubelle cellulaire
En approfondissant, les auteurs se sont concentrés sur deux régulateurs puissants de la croissance, YAP et TAZ, qui occupent une place centrale dans la voie de signalisation Hippo. Dans de nombreuses tumeurs solides, y compris le glioblastome, ces protéines agissent comme des interrupteurs maîtres qui favorisent la croissance cellulaire, la plasticité et l’état mésenchymateux. Normalement, quand la cellule veut freiner ce programme, elle marque YAP et TAZ pour destruction via une protéine appelée β‑TrCP, qui les conduit vers la « poubelle » de la cellule, le protéasome. L’étude montre que HSPA5 se lie physiquement à YAP et TAZ, utilisant son domaine de liaison au substrat comme une sorte de gant protecteur. Ce faisant, elle empêche β‑TrCP de s’attacher, bloque l’ubiquitination et la destruction de YAP/TAZ, et permet leur accumulation dans le noyau où ils activent des gènes mésenchymateux, notamment CD44 et c‑MET.
Des boîtes de culture et des souris aux tumeurs de patients
L’équipe a confirmé ce mécanisme de plusieurs manières. Bloquer HSPA5 accélère la disparition des protéines YAP et TAZ, sauf quand le protéasome est chimiquement inhibé, et augmente les signaux d’« étiquetage » pour la mise au rebut. La réactivation de YAP et TAZ compense la perte de croissance et d’invasion observée lors de la réduction de HSPA5, tandis que le silence de YAP/TAZ annule les effets pro‑tumoraux d’une surexpression de HSPA5. Dans des modèles murins où des cellules humaines de glioblastome sont implantées dans le cerveau, les tumeurs exprimant beaucoup de HSPA5 croissaient davantage et tuaient les animaux plus rapidement ; réduire HSPA5, ou interrompre son soutien à YAP/TAZ, ralentissait la croissance et prolongeait la survie. Enfin, dans des échantillons humains appariés prélevés chez les mêmes patients avant et après récidive, les tumeurs récurrentes, plus mésenchymateuses, présentaient des niveaux plus élevés de HSPA5, YAP, TAZ et de marqueurs mésenchymateux que les tumeurs initiales à profil proneural.
Ce que cela signifie pour les traitements futurs du cancer du cerveau
Concrètement, ces travaux suggèrent que les cellules de glioblastome exploitent une chaperonne de la réponse au stress, HSPA5, pour protéger des commutateurs de croissance cruciaux (YAP et TAZ) contre la dégradation. Cette protection aide les tumeurs à basculer vers et à maintenir une identité plus agressive et résistante aux traitements. Comme des inhibiteurs de petite molécule ciblant HSPA5 existent déjà et que les cellules tumorales peuvent dépendre davantage de cette chaperonne que les cellules normales, l’axe HSPA5–YAP/TAZ constitue une cible prometteuse. Des thérapies visant à affaiblir ce bouclier protecteur pourraient rendre les cellules de glioblastome moins adaptables, moins invasives et plus vulnérables aux traitements standards tels que la chimiothérapie et la radiothérapie.
Citation: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Mots-clés: glioblastome, HSPA5, YAP/TAZ, plasticité tumorale, transition mésenchymateuse