Clear Sky Science · fr
l’arrêt du cycle cellulaire en G0/G1 médié par p16 entraîne un phénotype sécrétoire associé à la sénescence (SASP) et une fibrose dans la dystrophie endothéliale de Fuchs
Pourquoi cette maladie oculaire importe
Avec l’âge, l’une des menaces moins connues pour la vision est une affection appelée dystrophie endothéliale de Fuchs (DEF), qui trouble progressivement la fenêtre antérieure normalement transparente de l’œil. Cet article explore pourquoi certaines cellules de la face interne de la cornée s’épuisent et se cicatrisent avec le temps, et pourquoi les femmes sont plus souvent touchées. Comprendre ces changements discrets pourrait ouvrir la voie à des médicaments qui retardent ou même évitent la nécessité de greffes cornéennes.
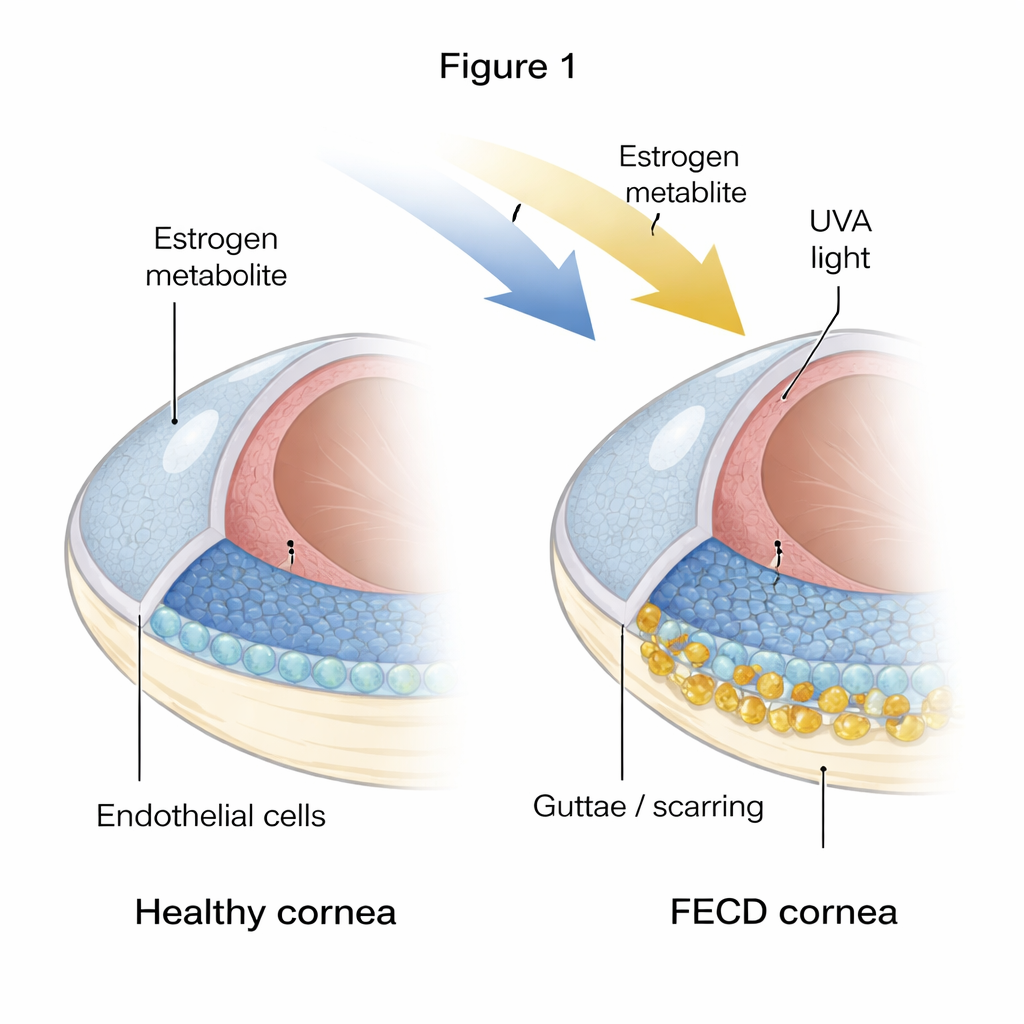
La fragile couche interne de la cornée
La cornée doit rester précisément déshydratée pour rester transparente, tâche assurée par une seule couche de cellules hexagonales appelées cellules endothéliales cornéennes. Dans la DEF, beaucoup de ces cellules meurent et la couche devient inégale et irrégulière. En parallèle, des excroissances et des dépôts épaissis, appelés guttae et matrice extracellulaire en excès, s’accumulent sur la surface interne. Les auteurs ont comparé des cornées de donneurs sains à des cornées de patients atteints de DEF et ont trouvé des signes marqués que le tissu malade est à la fois « âgé » et fibreux : les cellules présentaient des marqueurs de sénescence (un arrêt permanent) et de fibrose (comportement plus proche de cellules productrices de cicatrice et dépôt de tissu supplémentaire).
Le stress chronique lumineux et hormonal pousse les cellules dans une impasse
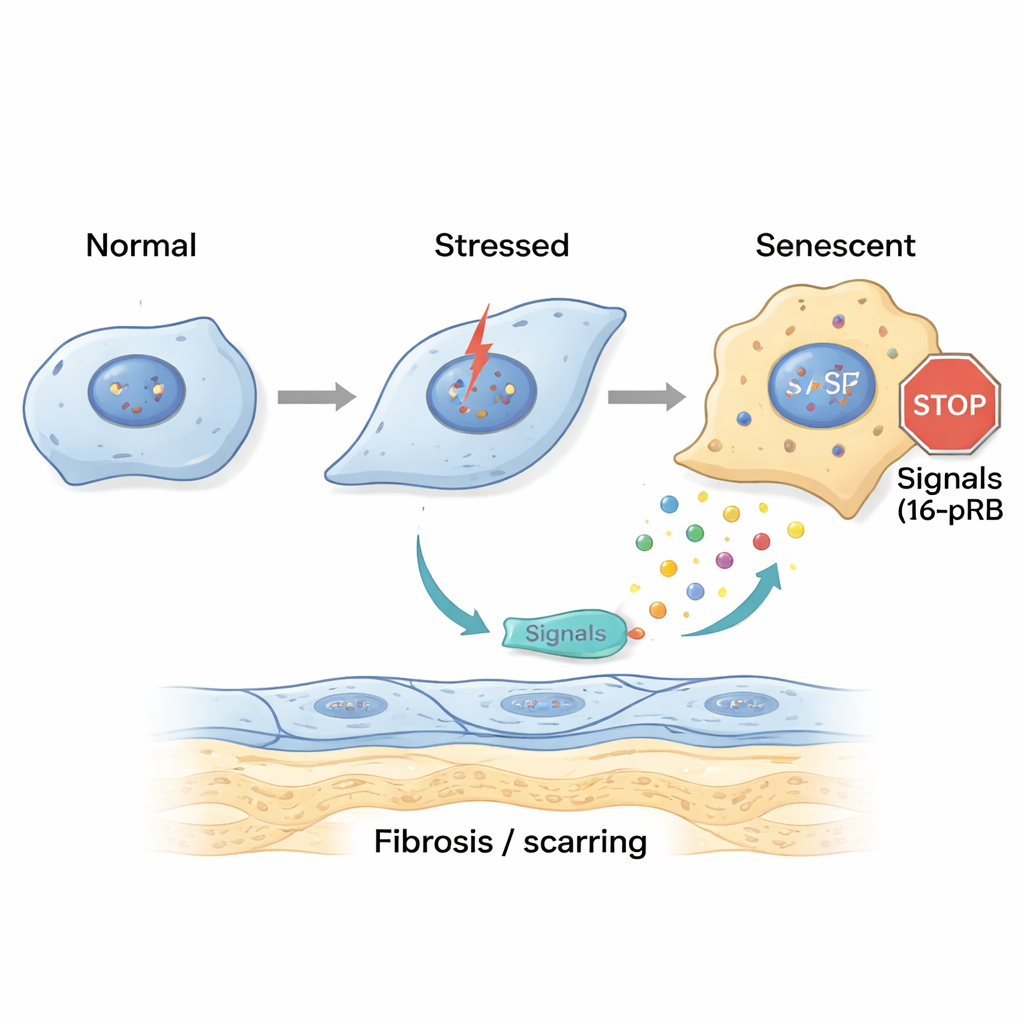
Pour comprendre comment ce dommage commence, les chercheurs ont recréé en laboratoire un stress de type DEF. Ils ont exposé des cellules endothéliales cornéennes saines aux ultraviolets A (UVA) et au 4‑hydroxyœstradiol, un produit oxydé de l’œstradiol lié aux dommages de l’ADN. Un bref coup de stress unique provoquait un arrêt temporel des cellules à un stade tardif du cycle cellulaire et un début de transition vers un état plus fibroblastique, mais une capacité de récupération subsistait. En revanche, des expositions répétées et chroniques conduisaient les cellules dans un autre état : elles s’accumulaient en phase précoce du cycle, appelée G0/G1, et activeaient le gène p16, qui verrouille le cycle cellulaire via sa partenaire pRB. Ces cellules devenaient grandes, plates et indubitablement sénescentes, tout en exprimant fortement des marqueurs de fibrose et des protéines constituant les guttae épaissis de la DEF.
Les cellules sénescentes envoient des signaux nuisibles et propagent la cicatrisation
Les cellules sénescentes ne restent pas passives ; elles sécrètent un mélange de molécules de signalisation connu sous le nom de phénotype sécrétoire associé à la sénescence (SASP). L’équipe a collecté le fluide provenant de cellules cornéennes stressées et l’a appliqué à des cellules fraîches et à des cornées de donneurs sains. Le SASP « aigu » provoquait des signes précoces de modification de la forme cellulaire, tandis que le SASP « chronique » poussait de nombreuses cellules en sénescence et augmentait l’expression de gènes liés à la fibrose et au dépôt de matrice. Des analyses détaillées ont montré que le SASP chronique était riche en médiateurs inflammatoires tels que IL‑8 et IL‑17, connus pour favoriser le vieillissement cellulaire, la cicatrisation fibreuse et le recrutement de cellules immunitaires. Lorsque les chercheurs ont bloqué la voie IL‑17 ou le récepteur CXCR2 d’IL‑8, les cellules exposées au SASP chronique présentaient moins de marqueurs de sénescence et moins de fibrose, suggérant que ces signaux sont des moteurs clés de la maladie.
Éliminer les cellules usées pour protéger la vision
Étant donné que les cellules sénescentes p16‑positives étaient fortement liées à la cicatrisation, les auteurs ont testé si les éliminer pouvait protéger la cornée. Dans un modèle murin où l’exposition aux UVA déclenche des changements similaires à la DEF, ils ont traité les animaux avec une combinaison de médicaments sénolytiques, dasatinib plus quercétine, qui tue sélectivement les cellules sénescentes. Par rapport aux souris non traitées, les souris traitées par sénolytiques conservaient une mosaïque endothéliale plus régulière, préservaient un plus grand nombre de cellules et présentaient moins de marqueurs de sénescence, de fibrose et d’excès de matrice. En d’autres termes, éliminer les cellules les plus endommagées a allégé le fardeau des sécrétions nocives et aidé à maintenir une surface cornéenne plus saine.
Ce que cela signifie pour les personnes atteintes de DEF
Pour les patients, la DEF conduit actuellement souvent à une greffe cornéenne lorsque la vision devient trop trouble. Cette étude suggère une autre voie : la maladie pourrait être entraînée par une accumulation lente de cellules stressées et non divisantes qui non seulement ne remplissent plus leur fonction, mais empoisonnent activement leurs voisines par des signaux inflammatoires et pro‑fibrotiques. Cibler ces signaux avec des médicaments contre les voies IL‑17 ou IL‑8, ou utiliser des thérapies sénolytiques pour éliminer sélectivement les cellules les plus atteintes, pourrait un jour retarder la fibrose, préserver davantage de tissu naturel de l’œil et reporter ou réduire le besoin de chirurgie.
Citation: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
Mots-clés: dystrophie de Fuchs, endothélium cornéen, sénescence cellulaire, fibrose, thérapie sénolytique