Clear Sky Science · fr
L’ADN mitochondrial active l’axe NLRP3-IL-1β dans les microglies en se liant à NLRP3, entraînant une neurodégénérescence dans des modèles de la maladie de Parkinson
Pourquoi c’est important pour la maladie de Parkinson
La maladie de Parkinson est surtout connue pour ses tremblements et la lenteur des mouvements, mais sous ces symptômes se joue une bataille complexe dans le cerveau. Cette étude révèle comment de petits fragments de matériel génétique issus de mitochondries endommagées dans les cellules immunitaires du cerveau peuvent déclencher une inflammation qui, progressivement, tue les neurones producteurs de dopamine nécessaires à la fluidité du mouvement. Comprendre cette réaction en chaîne ouvre la voie à des cibles thérapeutiques très précises susceptibles de ralentir ou prévenir les dommages de type parkinsonien.
Cellules immunitaires du cerveau et centrales énergétiques sous stress
Le cerveau contient non seulement des neurones mais aussi des microglies, ses cellules immunitaires résidentes. Dans la maladie de Parkinson, ces microglies deviennent souvent hyperactives, libérant des molécules toxiques et des signaux inflammatoires qui endommagent les neurones voisins. Les auteurs se sont concentrés sur les mitochondries, les « centrales » cellulaires, qui possèdent leur propre ADN. Lorsque les mitochondries sont lésées — par des toxines, le vieillissement ou d’autres stress — leur ADN peut s’oxyder, une forme de dommage chimique causée par les espèces réactives de l’oxygène. Comme l’ADN mitochondrial ressemble à l’ADN bactérien, ces fragments altérés peuvent agir comme des signaux d’alarme dans le cerveau, alertant le système immunitaire et favorisant potentiellement une inflammation chronique.
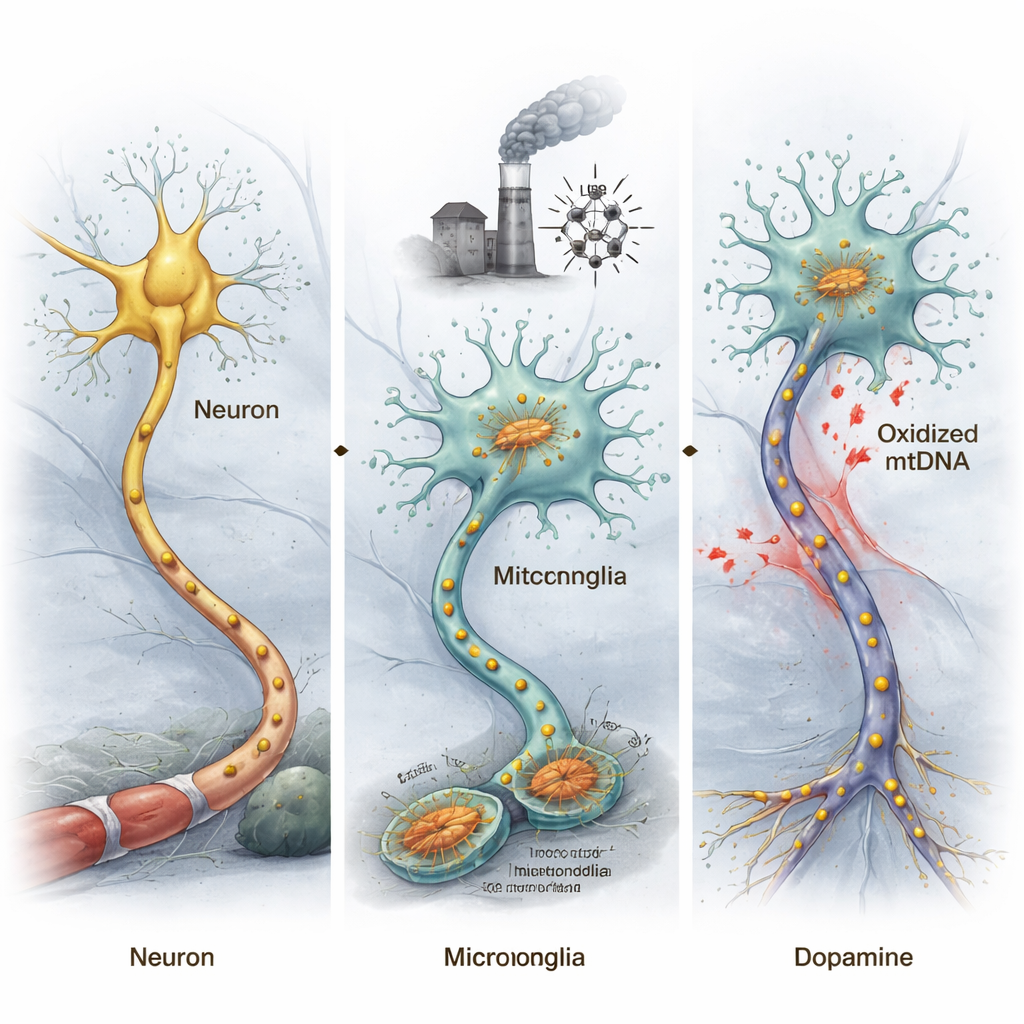
L’ADN mitochondrial endommagé peut pousser les souris vers une maladie de type Parkinson
Pour tester si l’ADN mitochondrial oxydé (ox-mtDNA) peut réellement déclencher des changements de type parkinsonien, les chercheurs ont extrait de l’ox-mtDNA de microglies stressées et l’ont injecté directement dans une région du cerveau qui contient normalement des neurones producteurs de dopamine importants pour le mouvement. Les souris exposées à cet ox-mtDNA ont montré une diminution de l’activité motrice dans des tests comportementaux et une perte de ces neurones dopaminergiques, reproduisant des caractéristiques centrales de la maladie de Parkinson. En triant les neurones et les microglies du mésencéphale et en analysant leur activité génique, l’équipe a constaté que les gènes liés à la maladie de Parkinson devenaient plus anormaux dans les neurones, tandis que les gènes associés à l’inflammation étaient fortement activés dans les microglies.
Un interrupteur d’alarme moléculaire à l’intérieur des microglies
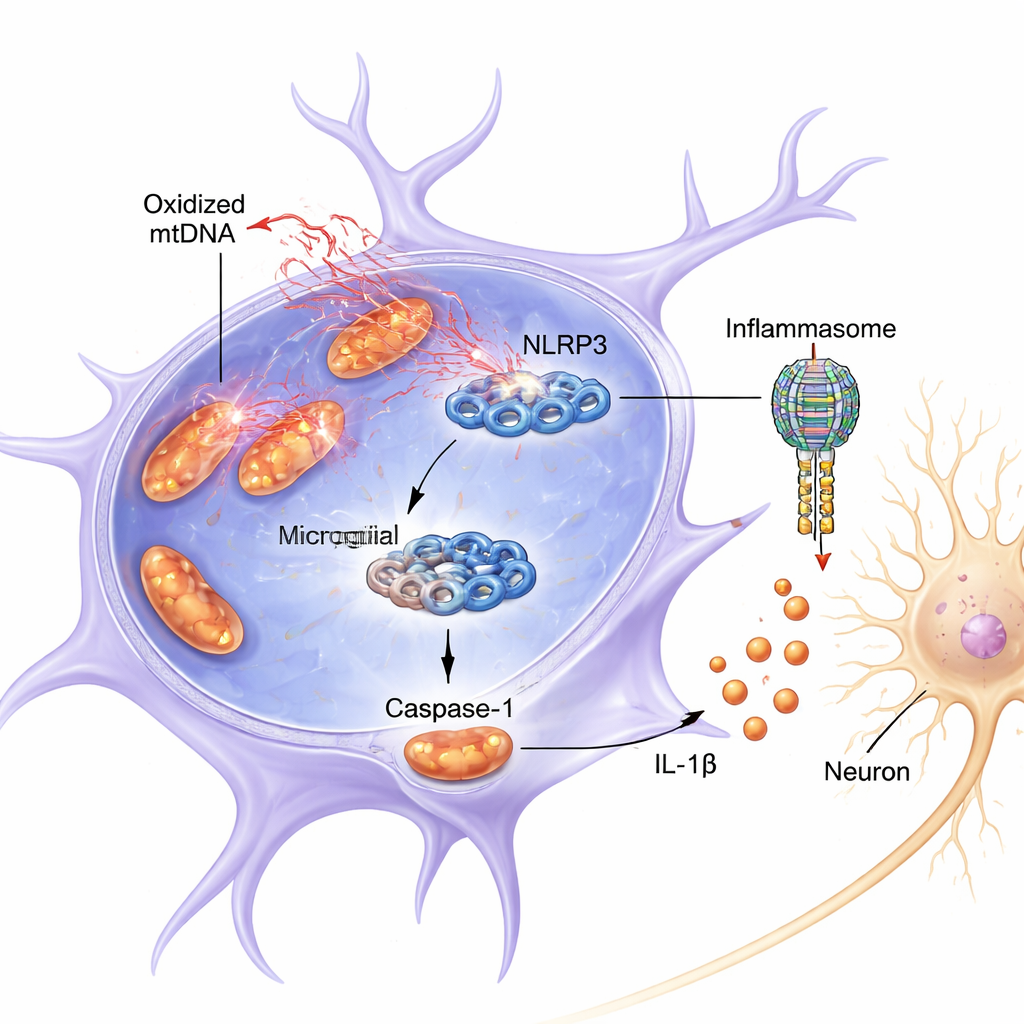
L’étude s’est focalisée sur un complexe protéique des microglies appelé NLRP3, qui fait partie d’un assemblage plus vaste connu sous le nom d’inflammasome. Lorsqu’il est activé, NLRP3 aide à activer la caspase-1, une enzyme qui clive la molécule inflammatoire IL-1β en sa forme active et délétère. Tant chez la souris que dans des cultures cellulaires, la combinaison d’un signal d’amorçage inflammatoire (LPS, un composant bactérien) et de la toxine de type pesticide rotenone a provoqué la libération d’ADN mitochondrial oxydé par les mitochondries des microglies dans le cytosol. Cette libération a coïncidé avec une activation plus forte de NLRP3, davantage de caspase-1 clivée (active) et des taux plus élevés d’IL-1β. Le milieu prélevé sur ces microglies hyperactivées était directement toxique pour des neurones de type dopaminergique cultivés en plaque, réduisant leur survie et le niveau de leur marqueur clé, la tyrosine hydroxylase.
Fixation directe : comment l’ADN oxydé active NLRP3
Au-delà d’une simple corrélation, les auteurs ont montré que l’ox-mtDNA n’est pas seulement présent pendant l’inflammation — il semble se lier physiquement à NLRP3 et l’activer. Lorsqu’ils ont bloqué la libération d’ADN mitochondrial avec un médicament, l’activation de la caspase-1 et d’IL-1β a diminué. À l’inverse, l’introduction directe d’ADN mitochondrial oxydé dans les microglies a fortement renforcé la signalisation NLRP3, davantage que l’ADN mitochondrial non oxydé. Grâce à des expériences biochimiques d’affinity pull-down, ils ont détecté de l’ADN mitochondrial, riche en marqueurs de dommages oxydatifs, associé à NLRP3. La modélisation informatique et la biochimie des protéines ont révélé que l’ox-mtDNA se lie à un segment positivement chargé et flexible de NLRP3 (une « région intrinsèquement désordonnée » couvrant les acides aminés 180–187). Lorsque cette portion critique était supprimée de NLRP3, sa capacité à se lier à l’ox-mtDNA et à activer la caspase-1 était fortement réduite.
Désactiver l’inflammasome épargne les neurones
Les chercheurs ont ensuite demandé si interférer avec NLRP3 pourrait protéger les neurones. Dans des microglies en culture, une réduction génétique de NLRP3 a fortement diminué l’activation de la caspase-1 et d’IL-1β après traitement par LPS et rotenone, et le milieu conditionné de ces cellules était beaucoup moins toxique pour les neurones de type dopaminergique. Chez la souris, un inhibiteur sélectif de NLRP3 (MCC950) a réduit l’activation microgliale, préservé les neurones dopaminergiques et abaissé les protéines liées à l’inflammasome dans des modèles induits soit par LPS plus rotenone, soit par injection d’ADN mitochondrial. Ensemble, ces expériences montrent que la chaîne ox-mtDNA–NLRP3–IL-1β n’est pas seulement associée aux dommages ; elle est nécessaire pour une grande partie de la perte neuronale observée.
Ce que cela signifie pour les futures thérapies de la maladie de Parkinson
Pour les non-spécialistes, le message clé est que l’ADN mitochondrial endommagé fuyant des cellules immunitaires du cerveau peut se fixer directement sur un « interrupteur d’alarme » interne (NLRP3), provoquant une vague d’inflammation qui blesse les neurones dopaminergiques et conduit à une maladie de type Parkinson dans des modèles expérimentaux. Parce que cette interaction dépend d’un court segment défini de la protéine NLRP3 et de la nature oxydée de l’ADN mitochondrial, elle offre des cibles médicamenteuses précises. Des thérapies qui empêchent les dommages ou la fuite de l’ADN mitochondrial, bloquent sa liaison à NLRP3, ou inhibent NLRP3 lui-même pourraient, en théorie, tempérer cette cascade inflammatoire et ralentir la progression de la maladie de Parkinson.
Citation: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
Mots-clés: Maladie de Parkinson, microglie, ADN mitochondrial, inflammasome NLRP3, neuroinflammation