Clear Sky Science · fr
La lactylation de SLC26A3 dans le microenvironnement tumoral acide favorise la progression maligne du carcinome colorectal
Pourquoi l’acidité tumorale compte
Le cancer colorectal reste l’un des cancers les plus meurtriers au monde, en partie parce que les tumeurs récidivent, métastasent ou cessent de répondre aux traitements. Cette étude explore un coupable trop peu considéré de ce comportement : l’environnement intratumoral acide et riche en acide lactique. En montrant comment ce milieu hostile déstabilise une protéine membranaire protectrice, SLC26A3, les auteurs dévoilent une nouvelle chaîne d’événements qui rend les cellules cancéreuses plus semblables à des cellules souches, plus invasives et plus résistantes aux médicaments — ouvrant ainsi de nouvelles pistes thérapeutiques.
Un voisinage hostile autour des cellules cancéreuses
Les tumeurs en croissance rapide consomment de grandes quantités de sucre et d’oxygène, libérant de l’acide lactique et des ions hydrogène qui acidifient leur environnement. À partir de larges jeux de données patient et d’échantillons tissulaires, les chercheurs montrent que cet état acide, repéré par une protéine marqueuse appelée CA9, va de pair avec des tumeurs colorectales agressives. Dans les cancers plus avancés, les taux de CA9 sont élevés, tandis que ceux de SLC26A3 restent systématiquement bas. SLC26A3 se trouve normalement à la surface des cellules coliques et contribue à l’équilibre des sels et du bicarbonate, ce qui aide à réguler le pH. Dans des échantillons tumoraux, des lignées cellulaires et des analyses unicellulaires, l’équipe observe que lorsque l’acidité augmente, les niveaux de SLC26A3 diminuent — en particulier dans les cellules cancéreuses malignes présentant un phénotype de cellules souches. 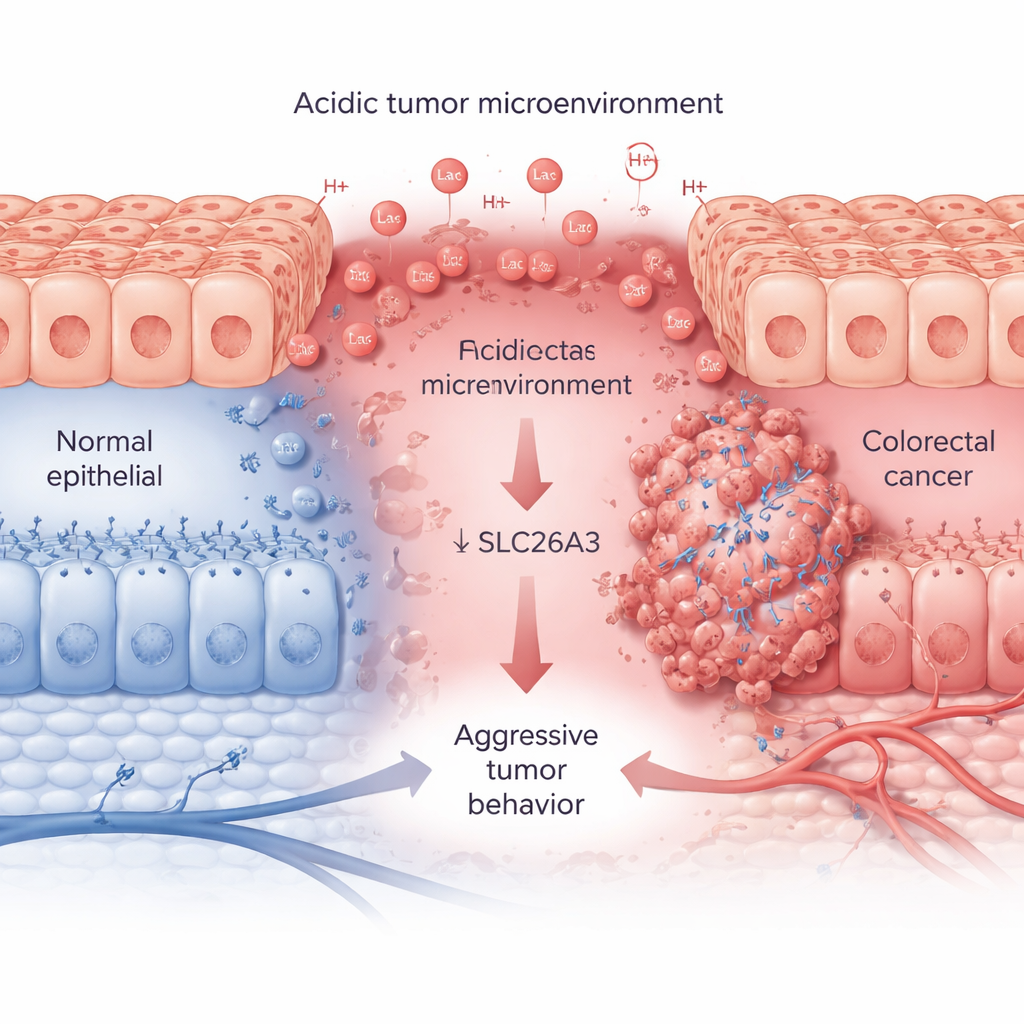
Comment l’acide lactique marque une cible pour la destruction
Les auteurs s’interrogent ensuite sur la raison de la baisse de SLC26A3 dans les tumeurs acides. Ils se concentrent sur la lactylation, un marquage chimique récemment découvert, dérivé de l’acide lactique, qui peut être ajouté aux protéines. Quand des cellules de cancer colorectal sont exposées à l’acide lactique ou cultivées en conditions acides, SLC26A3 est fortement lactylée. Une analyse protéique détaillée identifie un site clé, un acide aminé appelé K536, où cette modification est ajoutée. La lactylation en K536 rend SLC26A3 moins stable : la protéine est plus susceptible d’être ubiquitinée, signal cellulaire d’élimination, et dirigée vers les mécanismes de recyclage cellulaires. Bloquer l’enzyme p300, qui facilite l’ajout des marques de lactylation, protège partiellement SLC26A3 de la dégradation. En conséquence, l’acidité et le lactate établissent une boucle de rétroaction délétère — plus de lactate entraîne plus de lactylation, ce qui réduit SLC26A3, perturbe davantage l’équilibre du pH et favorise un microenvironnement encore plus acide.
Désactivation d’un frein à la stemness et à la dissémination tumorales
Quand SLC26A3 est épuisé, les cellules cancéreuses adoptent un comportement plus agressif. en culture cellulaire, les cellules cancéreuses colo-rectales de type souche expriment naturellement moins de SLC26A3 que leurs homologues non souches. Lorsque les chercheurs réduisent volontairement les niveaux de SLC26A3, les cellules tumorales forment davantage de sphères (un marqueur de stemness), se renouvellent plus efficacement, envahissent des membranes artificielles et migrent plus rapidement dans des tests de cicatrisation. Elles deviennent également moins sensibles à des chimiothérapies courantes comme l’oxaliplatine et le 5‑fluorouracile. À l’inverse, augmenter SLC26A3 diminue les marqueurs de stemness et ralentit l’invasion et la migration — mais cet effet protecteur est atténué lorsqu’on ajoute du lactate, soulignant comment l’acidité peut neutraliser cet avantage.
Un lien caché avec le contrôle des gènes
Au-delà de son rôle dans la régulation du pH, SLC26A3 sert aussi d’échafaudage liant deux protéines ARN‑liantes, HuR et CUGBP1. Ces protéines contrôlent la durée de vie de nombreux ARNm codant des protéines pertinentes pour le cancer. Lorsque SLC26A3 est abondant, il séquestre une partie de HuR et CUGBP1, limitant leur capacité à stabiliser ou déstabiliser certains messages oncogéniques. Lorsque SLC26A3 est perdu par lactylation et dégradation, HuR et CUGBP1 sont plus libres de se lier aux ARNm favorisant la stemness, la transition épithélio‑mésenchymateuse (TEM), l’invasion et la survie. Des expériences montrent que HuR aide à stabiliser les ARNm des marqueurs de stemness et des protéines de jonction cellulaire, tandis que CUGBP1 peut s’opposer à HuR pour certaines cibles, réduisant l’intégrité des jonctions et favorisant la TEM — deux processus qui facilitent la dissémination tumorale.
Recomposer l’environnement pour lutter contre le cancer
Pour tester si ces découvertes peuvent inspirer des stratégies thérapeutiques, les chercheurs utilisent des modèles murins de cancer colorectal. Neutraliser l’acidité tumorale avec du bicarbonate de sodium, bloquer le transport du lactate avec un inhibiteur de MCT1, ou surexprimer SLC26A3 ralentissent tous la croissance tumorale. Combiner la restauration de SLC26A3 avec la chimiothérapie réduit encore davantage les tumeurs. Dans les données patient, des niveaux plus élevés de SLC26A3 corrèlent avec une meilleure survie, moins de récidives, moins de métastases et de meilleures réponses à la chimiothérapie, ce qui suggère que cette protéine pourrait servir à la fois de biomarqueur et de cible thérapeutique. 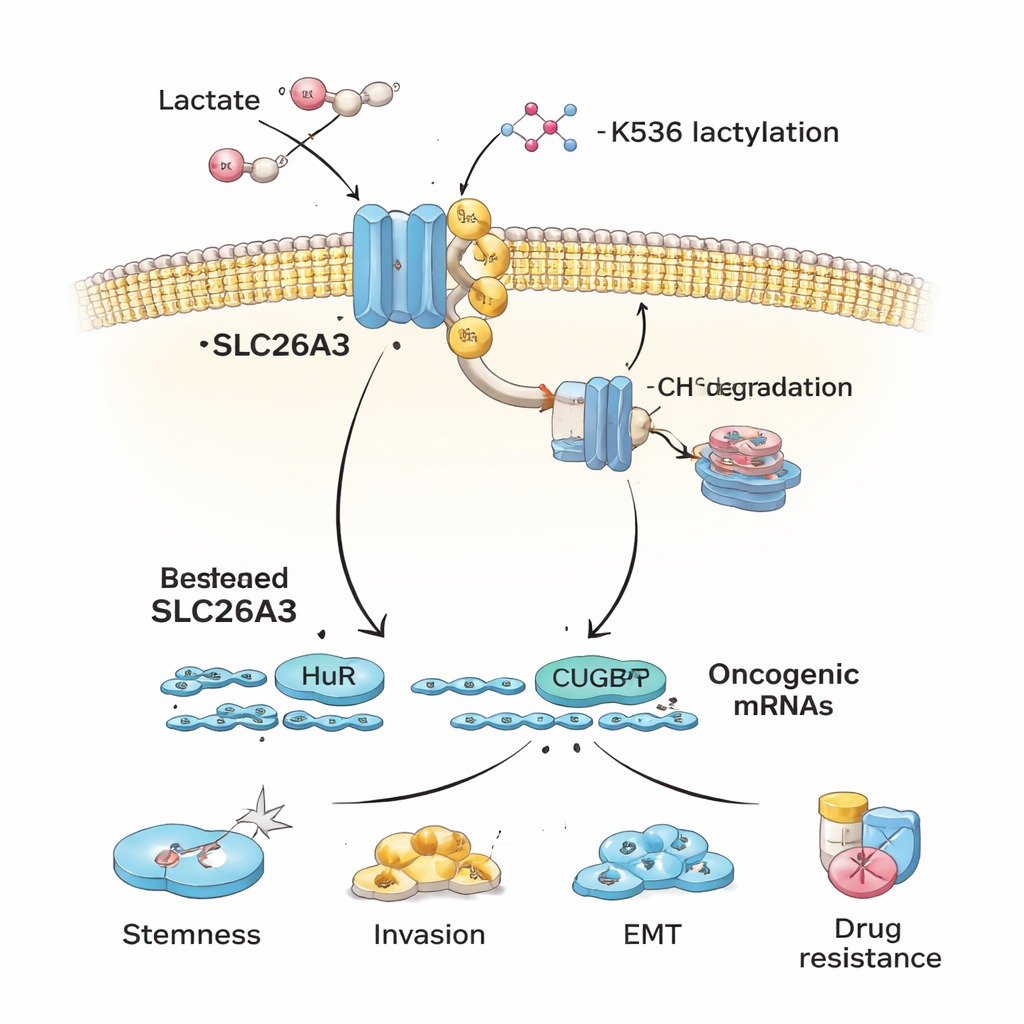
Ce que cela signifie pour les patients
Concrètement, cette étude montre que les tumeurs colorectales prospèrent dans un bain acide riche en acide lactique qui « étiquette » chimiquement et détruit un gardien protecteur, SLC26A3. Une fois ce gardien disparu, les cellules cancéreuses adoptent plus facilement des traits de cellules souches, se propagent et résistent aux traitements, aidées par de puissants régulateurs d’ARN à l’intérieur de la cellule. En tamponnant l’acidité tumorale, en bloquant le métabolisme du lactate ou en restaurant SLC26A3, il pourrait être possible d’affaiblir cette boucle maligne et d’améliorer l’efficacité des thérapies standards. Bien que ces approches nécessitent encore des essais cliniques rigoureux, elles ouvrent une voie prometteuse pour contrôler le cancer colorectal en modulant le milieu chimique tumoral.
Citation: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
Mots-clés: cancer colorectal, microenvironnement tumoral, lactylation, cellules souches cancéreuses, résistance à la chimiothérapie