Clear Sky Science · fr
Cibler GNG4 inhibe la progression tumorale et restaure la sensibilité à l’enzalutamide dans le cancer de la prostate en supprimant l’autophagie
Pourquoi cette recherche compte
Pour de nombreux hommes atteints d’un cancer de la prostate avancé, des médicaments anti-hormonaux puissants comme l’enzalutamide fonctionnent bien au départ, mais perdent progressivement leur efficacité. Cette étude révèle une astuce de survie utilisée par les cellules tumorales et met en lumière une protéine spécifique, appelée GNG4, qui aide les cancers à continuer de croître et à résister au traitement. Comprendre ce mécanisme pourrait conduire à des thérapies combinées rendant les médicaments actuels plus efficaces et durables.
Un interrupteur protéique à découvert
Les cellules du cancer de la prostate sont fortement dépendantes des hormones masculines, si bien que la prise en charge standard des formes avancées vise à supprimer ces signaux. Pourtant, la plupart des tumeurs deviennent finalement « résistantes à la castration » et recommencent à croître. Les auteurs ont cherché des gènes beaucoup plus actifs dans le tissu tumoral que dans la prostate saine adjacente des mêmes patients. Parmi plusieurs candidats, GNG4 s’est distingué : lorsqu’ils ont réduit son niveau dans des cellules de cancer de la prostate, la croissance tumorale a chuté nettement. Des analyses de centaines d’échantillons de patients ont confirmé que GNG4 est plus élevé dans les cancers prostatiques primaires que dans le tissu normal et qu’il est particulièrement augmenté dans les tumeurs plus agressives et de grade élevé.
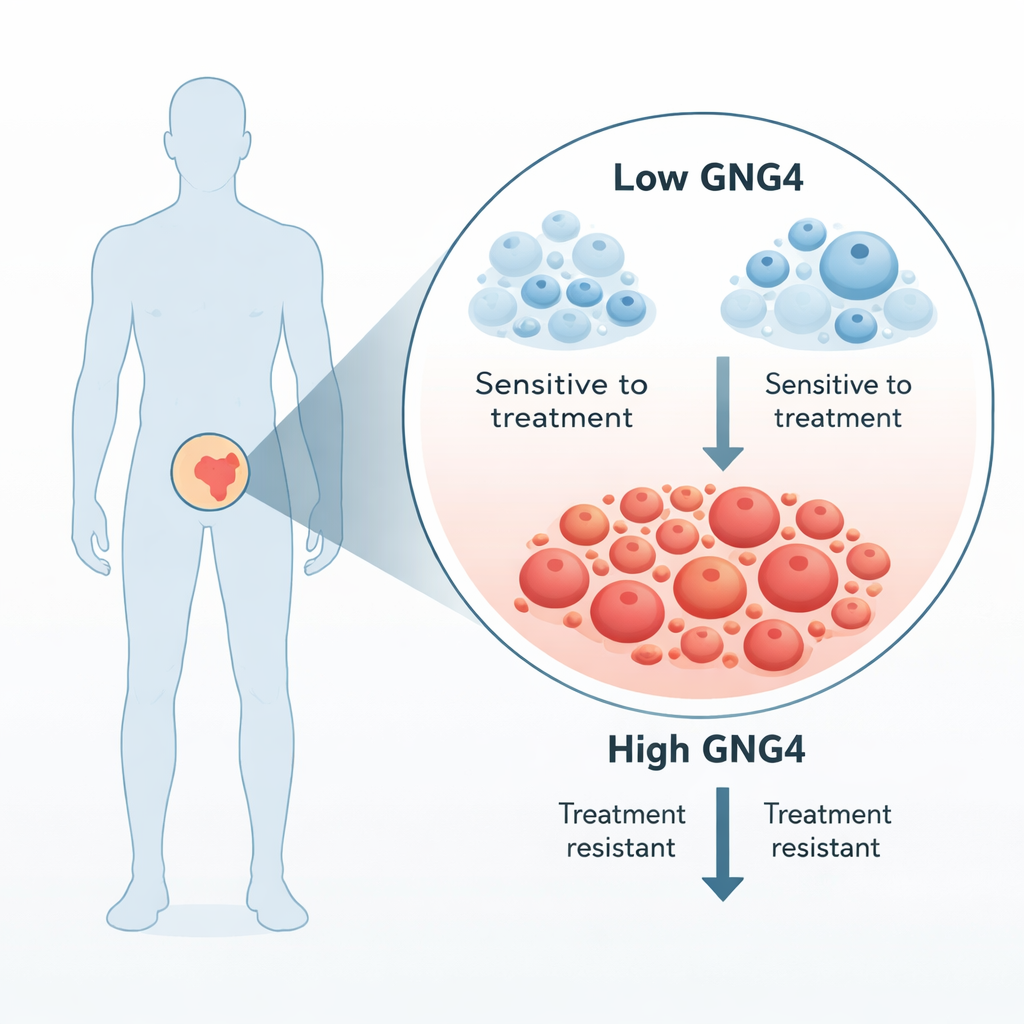
Comment GNG4 aide les tumeurs à prospérer
GNG4 fait partie d’une grande famille de signalisation connue sous le nom de protéines G, qui siègent à la membrane cellulaire et transmettent des signaux de l’extérieur vers l’intérieur de la cellule. L’équipe a montré que la diminution de GNG4 dans des lignées cellulaires de cancer de la prostate ralentissait la division cellulaire, bloquait les cellules à une étape de contrôle du cycle, et augmentait la mort cellulaire programmée. Ces changements réduisaient aussi la capacité des cellules cancéreuses à migrer et à refermer des lésions dans des tests en laboratoire, et les tumeurs formées par des cellules déficientes en GNG4 croissaient plus lentement chez la souris. Ensemble, ces résultats suggèrent que GNG4 joue le rôle d’accélérateur pour la croissance et la dissémination du cancer de la prostate.
Autophagie : le garde-manger d’urgence de la cellule cancéreuse
Les chercheurs se sont ensuite concentrés sur un processus appelé autophagie, par lequel les cellules décomposent et recyclent leurs propres composants pour survivre au stress, comme la privation de nutriments ou le traitement médicamenteux. Dans de nombreux cancers avancés, l’autophagie sert de garde-manger d’urgence qui aide les cellules tumorales à faire face à des conditions défavorables. Dans cette étude, les cellules de cancer de la prostate à forte activité de GNG4 présentaient davantage de signes d’autophagie active, tandis que les cellules avec GNG4 réduit avaient moins de structures de recyclage et des niveaux plus bas de marqueurs clés de l’autophagie. Quand GNG4 était surexprimé, les cellules toléraient mieux l’enzalutamide et subissaient moins de mort cellulaire. Le blocage de l’autophagie par un inhibiteur chimique annulait une grande partie de cette protection, indiquant que GNG4 aide les tumeurs à supporter le traitement principalement en renforçant ce système de recyclage.
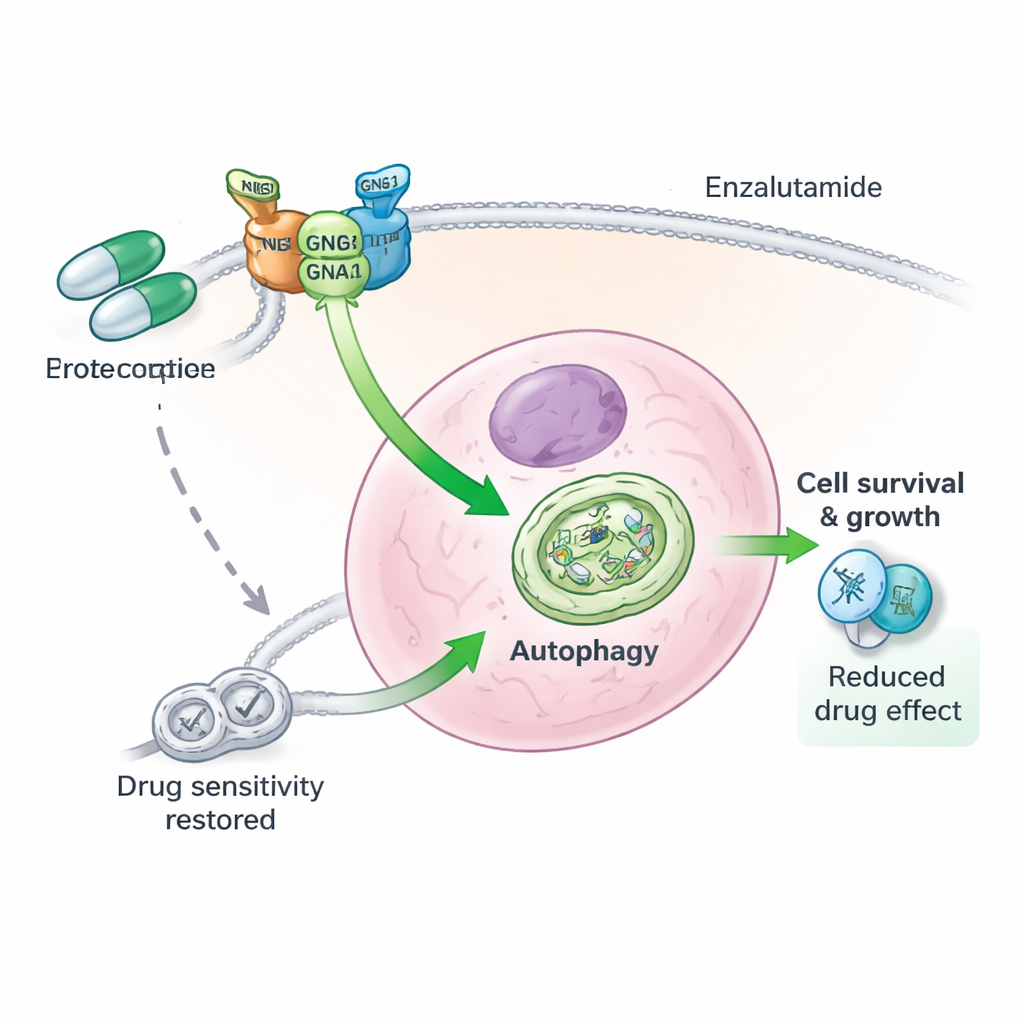
Une équipe de trois protéines derrière la résistance aux médicaments
En approfondissant, les auteurs ont découvert que GNG4 n’agit pas seul. Il s’associe physiquement à un autre composant des protéines G, GNB1, pour stabiliser une troisième protéine, GNAI3. Ensemble, ces trois sous-unités forment un complexe fonctionnel qui stimule l’autophagie dans les cellules de cancer de la prostate. Lorsque GNG4 était réduit, la protéine GNAI3 était plus rapidement marquée pour la destruction et dégradée par le système d’élimination cellulaire, éteignant le signal d’autophagie. La suppression directe de GNAI3 annulait les avantages de croissance et de survie conférés par un excès de GNG4, tant dans les cellules en culture que dans les tumeurs de souris. En d’autres termes, GNG4 favorise la malignité et la résistance au stress en grande partie via cet axe GNG4–GNB1–GNAI3.
Renforcer l’efficacité des traitements actuels
Enfin, l’équipe a testé ce qui se passe lorsque le ciblage de GNG4 est combiné à l’enzalutamide, un médicament de référence pour le cancer de la prostate avancé. En laboratoire, la réduction de GNG4 rendait les cellules cancéreuses nettement plus sensibles à l’enzalutamide et diminuait leur capacité à former des colonies après traitement. Chez la souris, les tumeurs avec un GNG4 abaissé régressaient davantage sous l’enzalutamide que les tumeurs avec des niveaux normaux de GNG4, sans toxicité ajoutée évidente. Le blocage direct de l’autophagie produisait des améliorations similaires. Ces résultats suggèrent que perturber l’autophagie pilotée par GNG4 peut priver les cellules tumorales d’un mécanisme de défense vital, permettant aux thérapies anti-hormonales existantes d’infliger un coup plus fort et plus durable.
Ce que cela signifie pour les patients
Pour un non-spécialiste, le message essentiel est que certains cancers de la prostate survivent au traitement en activant un système interne de recyclage qui agit comme un groupe électrogène de secours. Cette étude identifie GNG4 comme l’interrupteur principal qui active ce système, en collaboration avec des protéines partenaires pour protéger les cellules cancéreuses de l’enzalutamide. En éteignant cet interrupteur — soit en ciblant directement GNG4, soit en atténuant en toute sécurité l’autophagie — des thérapies futures pourraient ralentir la croissance tumorale et restaurer la sensibilité aux médicaments chez des hommes dont les cancers sont devenus difficiles à traiter.
Citation: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
Mots-clés: cancer de la prostate, résistance aux médicaments, autophagie, protéines G, enzalutamide