Clear Sky Science · fr
Profil préclinique des conjugués anticorps-médicaments ciblant le chondroïtine sulfate oncofœtal
Pourquoi cette recherche est importante pour les traitements anticancéreux futurs
Les médicaments contre le cancer fonctionnent souvent comme un bombardement généralisé : ils touchent les cellules à forte prolifération dans tout l’organisme, pas seulement dans les tumeurs, provoquant des effets indésirables sévères et parfois échouant à atteindre toutes les cellules cancéreuses. Cette étude explore une approche plus intelligente qui combine la précision des anticorps avec la puissance des agents chimiothérapeutiques, et cible une structure largement présente dans les tumeurs mais quasiment absente des tissus sains. Pour un lecteur non spécialiste, elle donne un aperçu de la manière dont les thérapies anticancéreuses futures pourraient être à la fois plus efficaces et moins dommageables.
Un « drapeau » spécifique au cancer sur le tissu tumoral
Les chercheurs se concentrent sur une molécule appelée chondroïtine sulfate oncofœtal, ou ofCS. Il s’agit d’un enrobage de type sucre qui apparaît pendant le développement fœtal, disparaît dans la plupart des tissus adultes sains, puis réapparaît dans de nombreux cancers. On le trouve non seulement sur les cellules cancéreuses elles‑mêmes, mais aussi dans l’échafaudage tumoral et les cellules de soutien environnantes. Cela en fait une cible particulièrement intéressante : frapper l’ofCS pourrait signifier atteindre à la fois la tumeur et son « sol » tout en épargnant majoritairement les organes normaux. L’équipe a précédemment identifié un fragment d’anticorps, nommé Vartumab, qui reconnaît l’ofCS sur une grande variété de tumeurs solides avec très peu de liaison aux tissus normaux.
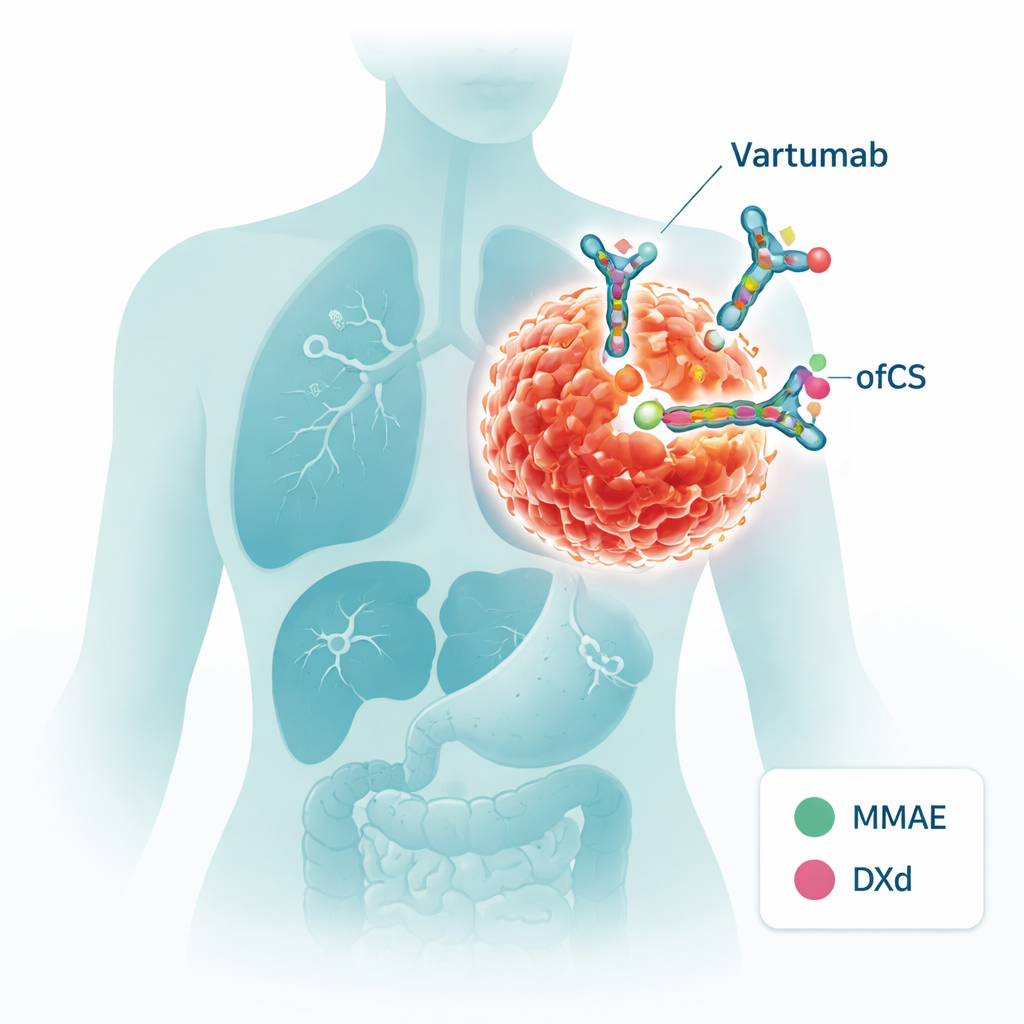
Concevoir un missile guidé contre les tumeurs
Dans ce travail, Vartumab est transformé en un conjugué anticorps‑médicament (ADC) — essentiellement un missile guidé portant une tête toxique. Les scientifiques ont attaché deux charges chimiothérapeutiques différentes, MMAE et DXd, chacune via un « linker » chimique qui peut être coupé par des enzymes couramment présentes dans l’environnement tumoral. Lorsque Vartumab se lie à l’ofCS, ces linkers peuvent être clivés, libérant le médicament exactement là où il est nécessaire. L’équipe a vérifié avec soin que les anticorps modifiés restaient stables dans des conditions proches du sang, libéraient la charge lorsqu’ils étaient exposés aux enzymes liées à la tumeur et, surtout, reconnaissaient toujours l’ofCS aussi bien que le Vartumab d’origine.
Toucher les cellules cancéreuses et leurs voisines
Une caractéristique clé des charges choisies est l’« effet voisin ». Une fois libérés, MMAE et DXd peuvent diffuser hors de la première cellule qu’ils tuent et pénétrer dans les cellules voisines, même si ces dernières n’expriment pas la cible ofCS. Les chercheurs ont testé cela en mélangeant des cellules de mélanome ofCS‑positives avec des cellules génétiquement modifiées ofCS‑négatives. Les ADC portant MMAE ou DXd ont tué non seulement les cellules ciblées, mais aussi les voisines dépourvues de cible, d’une manière dépendante de la proportion de cellules ofCS‑positives présentes. En revanche, un ADC témoin avec une charge moins perméable (MMAF) n’a tué que les cellules directement ciblées et n’a pas produit un fort effet voisin.
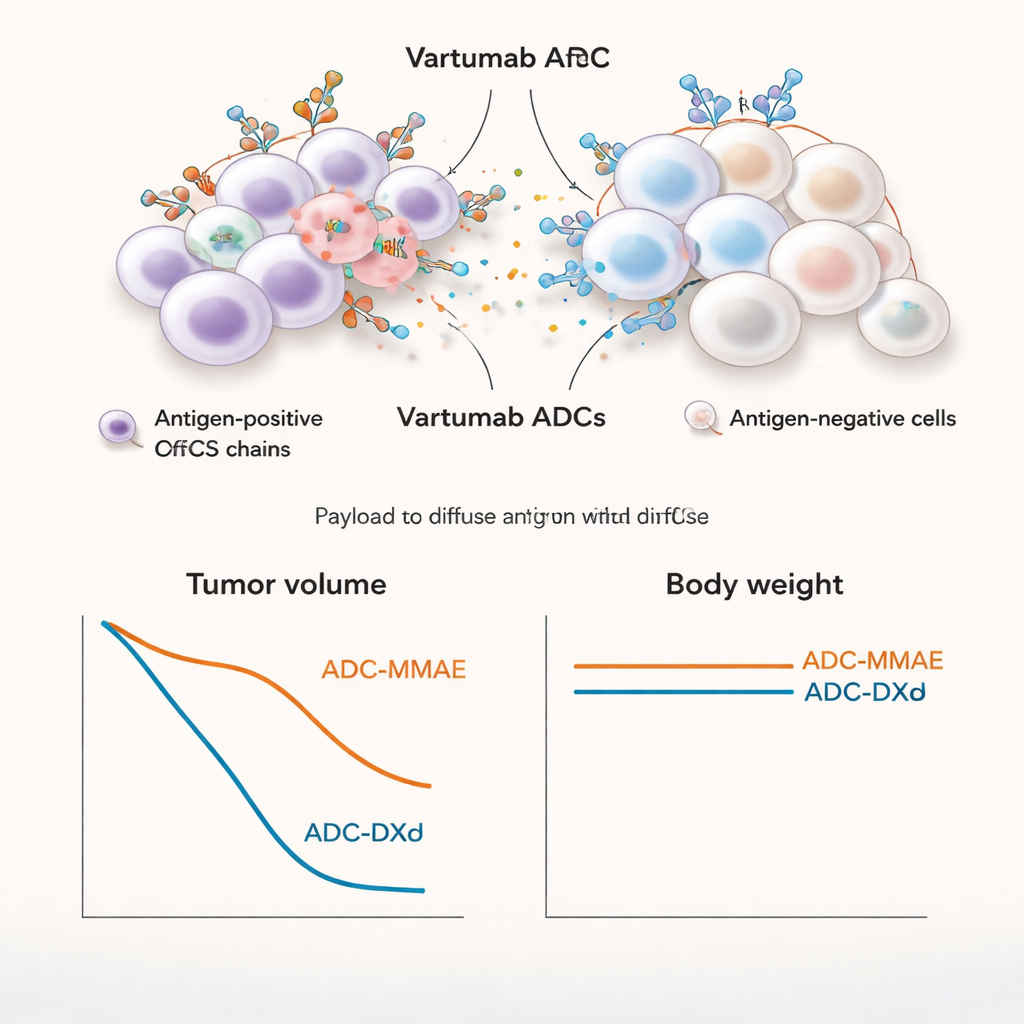
Forte réduction tumorale avec dommages hors cible limités
En avançant vers des modèles murins de mélanome et de cancer du poumon, les ADCs Vartumab se sont accumulés fortement dans les tumeurs tout en présentant des niveaux beaucoup plus faibles dans les autres organes. La version MMAE s’est montrée particulièrement puissante : à des doses relativement faibles, elle a complètement fait régresser des tumeurs établies, y compris dans un modèle de cancer du poumon avec des niveaux d’ofCS plus faibles. La version DXd a également entraîné une forte régression tumorale, bien qu’elle ait généralement nécessité des doses plus élevées. Lorsque l’équipe a comparé MMAE au MMAF non‑voisin chez la souris, seul l’ADC capable de produire un effet voisin (MMAE) a permis une élimination tumorale complète et durable, soulignant l’importance de tuer à la fois les cellules cancéreuses et les cellules stromales de soutien. Chez le rat, des administrations répétées de l’ADC MMAE jusqu’à 5 mg/kg ont été bien tolérées, la poids, les analyses sanguines et les examens tissulaires montrant seulement des modifications légères et réversibles, similaires aux effets connus de médicaments apparentés approuvés.
Ce que cela pourrait signifier pour les patients
Pour les non‑spécialistes, le message est que cette étude affine une stratégie prometteuse de « chercher‑et‑détruire » contre le cancer. En ciblant l’ofCS — un marqueur largement présent dans les tumeurs mais rare dans les tissus normaux — et en utilisant des charges capables de se répandre vers les cellules voisines, les ADCs Vartumab attaquent non seulement la masse tumorale visible, mais aussi son microenvironnement de soutien et les cellules cancéreuses cachées qui pourraient autrement échapper au traitement. Les travaux restent précliniques, mais ils suggèrent une voie vers des médicaments futurs plus centrés sur la tumeur, actifs sur de nombreux types de cancer, et susceptibles d’éviter certains des effets secondaires les plus graves de la chimiothérapie conventionnelle.
Citation: Skafte, A., Vidal-Calvo, E.E., Choudhary, S. et al. Preclinical profiling of antibody drug conjugates targeting oncofetal chondroitin sulfate. Cell Death Dis 17, 162 (2026). https://doi.org/10.1038/s41419-026-08420-x
Mots-clés: conjugués anticorps-médicaments, chondroïtine sulfate oncofœtal, effet voisin, thérapie ciblée du cancer, microenvironnement tumoral