Clear Sky Science · fr
DNA-PKcs orchestre la sénescence induite par l’élimination de CTLA-4 dans les cellules cancéreuses
Transformer l’interrupteur de croissance du cancer en signal d’arrêt
Les médicaments anticancéreux à base d’immunothérapie ciblent souvent une molécule appelée CTLA-4, présente sur les cellules immunitaires, pour aider l’organisme à attaquer les tumeurs. Cette étude révèle une surprise : CTLA-4 se trouve aussi à l’intérieur des cellules cancéreuses et peut agir comme un aide-croissance caché. Lorsque les chercheurs ont délibérément supprimé ce CTLA-4 intracellulaire dans des cellules de mélanome, les cellules cancéreuses ont cessé de se multiplier et sont entrées dans un état de « retraite » durable appelé sénescence cellulaire. Comprendre ce rôle inattendu ouvre de nouvelles voies pour ralentir ou même réduire les tumeurs en ciblant CTLA-4 à l’intérieur des cellules cancéreuses, et pas seulement sur les cellules immunitaires.
Quand les cellules choisissent la retraite plutôt que la croissance incontrôlée
Les cellules se divisent normalement, se réparent et—lorsqu’elles sont endommagées au-delà de toute réparation—meurent ou entrent en sénescence, un arrêt permanent de leur croissance. Les cellules sénescentes grossissent en général, changent de forme et produisent des marqueurs spécifiques détectables en laboratoire. Les chercheurs ont constaté que, lorsqu’ils réduisaient CTLA-4 à l’intérieur de cellules de mélanome murines et humaines, les cellules augmentaient de taille, leur prolifération chutait fortement et les signes classiques de sénescence montaient, y compris des enzymes détectables par des colorations spécifiques et des protéines comme p16 et p21 qui bloquent le cycle cellulaire. Ces changements ont été observés aussi bien lorsque CTLA-4 était temporairement silencé que lorsqu’il était définitivement supprimé par des outils d’édition génétique.
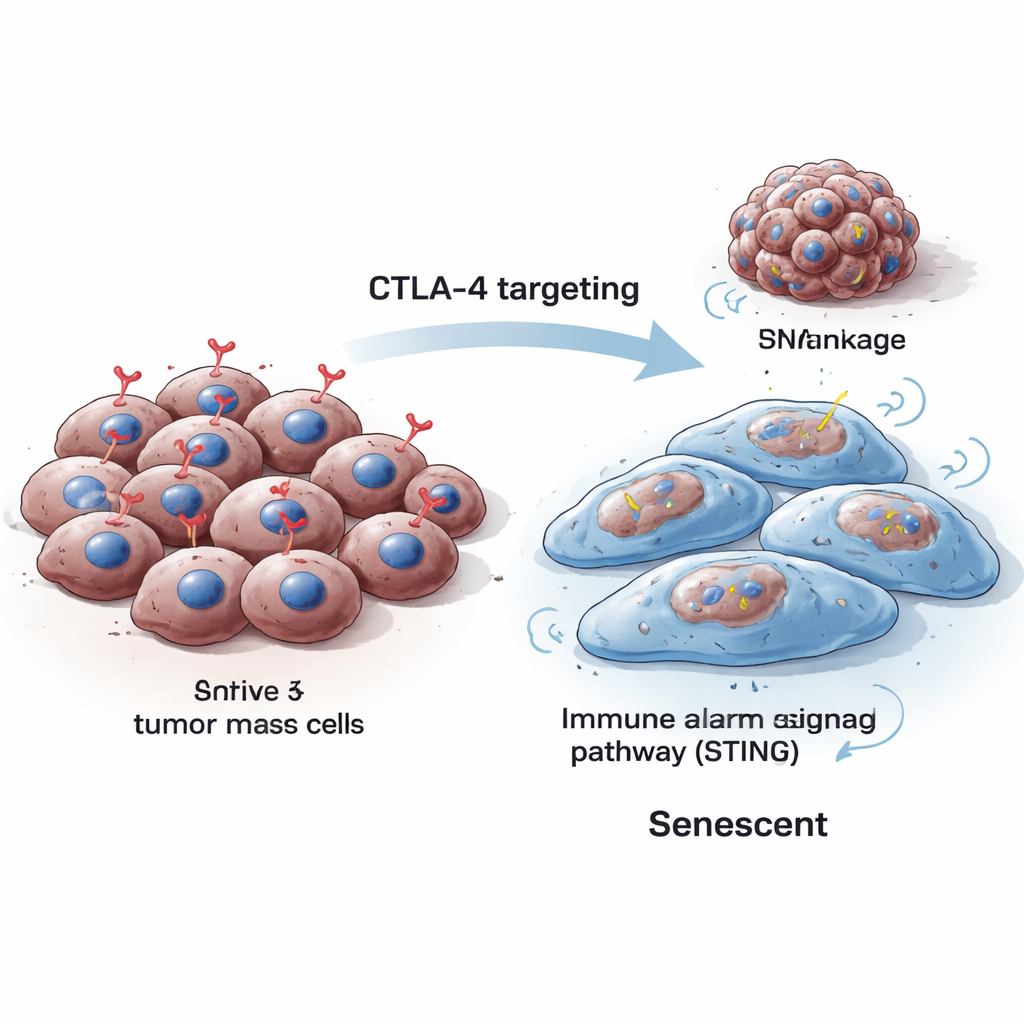
Des fissures dans le plan génétique provoquent un arrêt
Pour comprendre pourquoi la perte de CTLA-4 pousse les cellules cancéreuses vers la sénescence, l’équipe a examiné la manière dont ces cellules gèrent leur ADN lors de la division. Ils ont découvert que la déplétion de CTLA-4 réduisait les niveaux d’Aurora B, une protéine qui aide à séparer proprement les chromosomes pendant la division cellulaire. Quand Aurora B diminuait, les cellules développaient une instabilité génomique : de petits corps micronucléaires contenant de l’ADN apparaissaient et les marqueurs de dommages à l’ADN augmentaient. Ce type de stress de l’ADN est connu pour pousser les cellules vers la sénescence plutôt que vers une croissance incontrôlée. Fait important, la restauration d’Aurora B a permis de réduire ces micronoyaux, reliant directement la perte de CTLA-4 à une mauvaise gestion des chromosomes et aux dommages de l’ADN.
Les dommages à l’ADN déclenchent un réseau d’alarme interne
L’ADN fragmenté et déplacé dans les cellules appauvries en CTLA-4 n’est pas resté ignoré. Il a activé DNA-PKcs, un senseur des dommages à l’ADN, qui a à son tour déclenché la voie STING, un système d’alarme interne qui répond à la présence d’ADN errant dans la cellule. Une fois STING activé, il a signalé des molécules en aval, y compris TBK1 et IRF3, et a aussi renforcé une autre voie clé de contrôle de la croissance, la voie AKT. Plutôt que de promouvoir la croissance, cette signalisation combinée a finalement augmenté p21, un puissant frein du cycle cellulaire, consolidant l’état de sénescence. Lorsque les chercheurs ont bloqué DNA-PKcs, l’activation de STING et les caractéristiques de sénescence ont été fortement réduites, montrant que DNA-PKcs occupe une place centrale dans cette chaîne d’alarme.
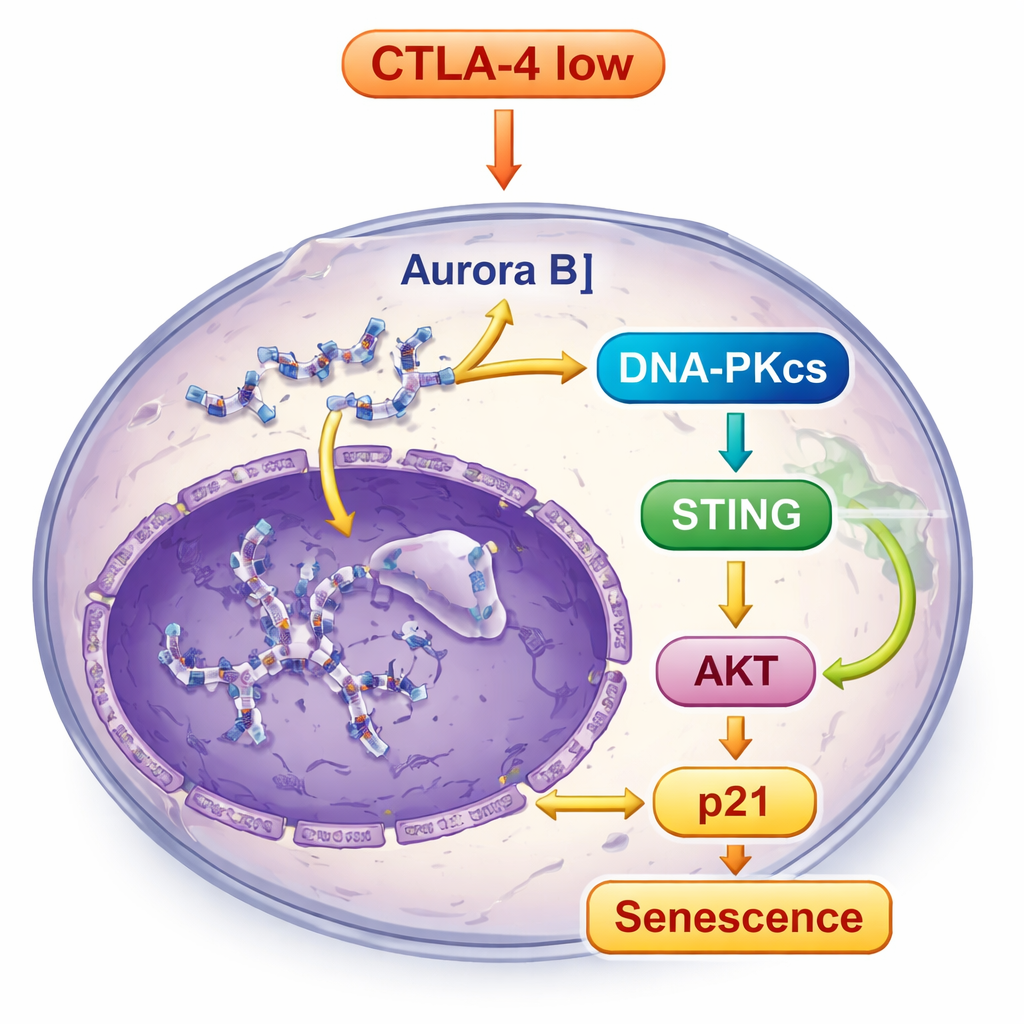
De la culture cellulaire aux tumeurs chez l’animal
Les boîtes de laboratoire ne racontent qu’une partie de l’histoire, aussi les chercheurs ont testé si la perte de CTLA-4 affecterait de vraies tumeurs chez des souris. Ils ont implanté des cellules de mélanome avec ou sans CTLA-4 de part et d’autre des mêmes animaux. Les tumeurs dépourvues de CTLA-4 ont crû plus lentement, pesé moins et avaient un volume moindre que leurs homologues contenant CTLA-4. Ces tumeurs déficientes en CTLA-4 présentaient aussi des colorations de sénescence plus marquées et des niveaux plus élevés de dommages à l’ADN et d’activation de la voie STING. L’analyse de données de patients issues de grandes bases publiques a en outre soutenu ce lien : à travers plusieurs types de cancer, l’expression de CTLA-4 tendait à être inversement corrélée à DNA-PKcs et à d’autres composants de la réparation de l’ADN, faisant écho aux observations de laboratoire sur la maladie humaine.
Ce que cela signifie pour les traitements anticancéreux futurs
Dans l’ensemble, l’étude montre que CTLA-4 intracellulaire aide les cellules cancéreuses à maintenir la stabilité génétique et à continuer de se diviser. Lorsque CTLA-4 est éliminé, les chromosomes deviennent instables, les cassures d’ADN s’accumulent et une voie d’alarme interne—centrée sur DNA-PKcs et STING—pousse les cellules vers un arrêt de croissance permanent. Pour le grand public, cela signifie que désactiver CTLA-4 dans les cellules tumorales incite les cancers à s’éloigner d’un comportement dangereux et rapidement proliférant pour tendre vers un état « retraité » plus sûr. Ces découvertes suggèrent que de futures thérapies anticancéreuses pourraient être conçues non seulement pour libérer le système immunitaire en bloquant CTLA-4 sur les cellules immunitaires, mais aussi pour désarmer directement les tumeurs en ciblant CTLA-4 à l’intérieur des cellules cancéreuses et en exploitant la sénescence comme frein intrinsèque à la croissance tumorale.
Citation: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Mots-clés: sénescence cellulaire, mélanome, CTLA-4, dégâts de l’ADN, voie STING