Clear Sky Science · fr
Navette cytoplasme‑noyau de TET2 : un frein intrinsèque dans la progression du cancer colorectal
Comment les cellules cancéreuses transportent leur propre frein
Le cancer colorectal est l’un des cancers les plus fréquents au monde et devient souvent mortel lorsque les cellules tumorales apprennent à envahir les tissus voisins et à se propager vers d’autres organes. Cette étude révèle que bon nombre de ces cellules cancéreuses possèdent en réalité un « système de freinage » interne — une protéine appelée TET2 — capable de ralentir leur avance lorsqu’elle se situe dans le noyau de la cellule. Comprendre comment ce frein intégré s’active ou se désactive pourrait ouvrir de nouvelles voies pour contenir la croissance tumorale plutôt que de se limiter à tenter d’éliminer les cellules cancéreuses.
Observer le déplacement d’une protéine clé à l’intérieur des cellules tumorales
Les chercheurs se sont intéressés à TET2, une protéine qui contribue à contrôler l’activation des gènes en supprimant certaines marques chimiques sur l’ADN. Dans des prélèvements tissulaires issus de centaines de patients atteints de cancer colorectal, ils ont localisé TET2 dans les cellules tumorales. Quatre grands profils sont apparus : principalement nucléaire, principalement cytoplasmique, ou fortement biaisé vers l’un ou l’autre compartiment. Les patients dont les tumeurs présentaient davantage de TET2 dans le noyau avaient tendance à vivre plus longtemps, tandis que ceux dont les tumeurs retenaient TET2 dans le cytoplasme avaient un pronostic plus défavorable. À mesure que les cancers progressaient vers des stades cliniques plus avancés, la présence de TET2 nucléaire diminuait, ce qui suggère que la perte de cette protection nucléaire fait partie du processus rendant les tumeurs plus agressives.
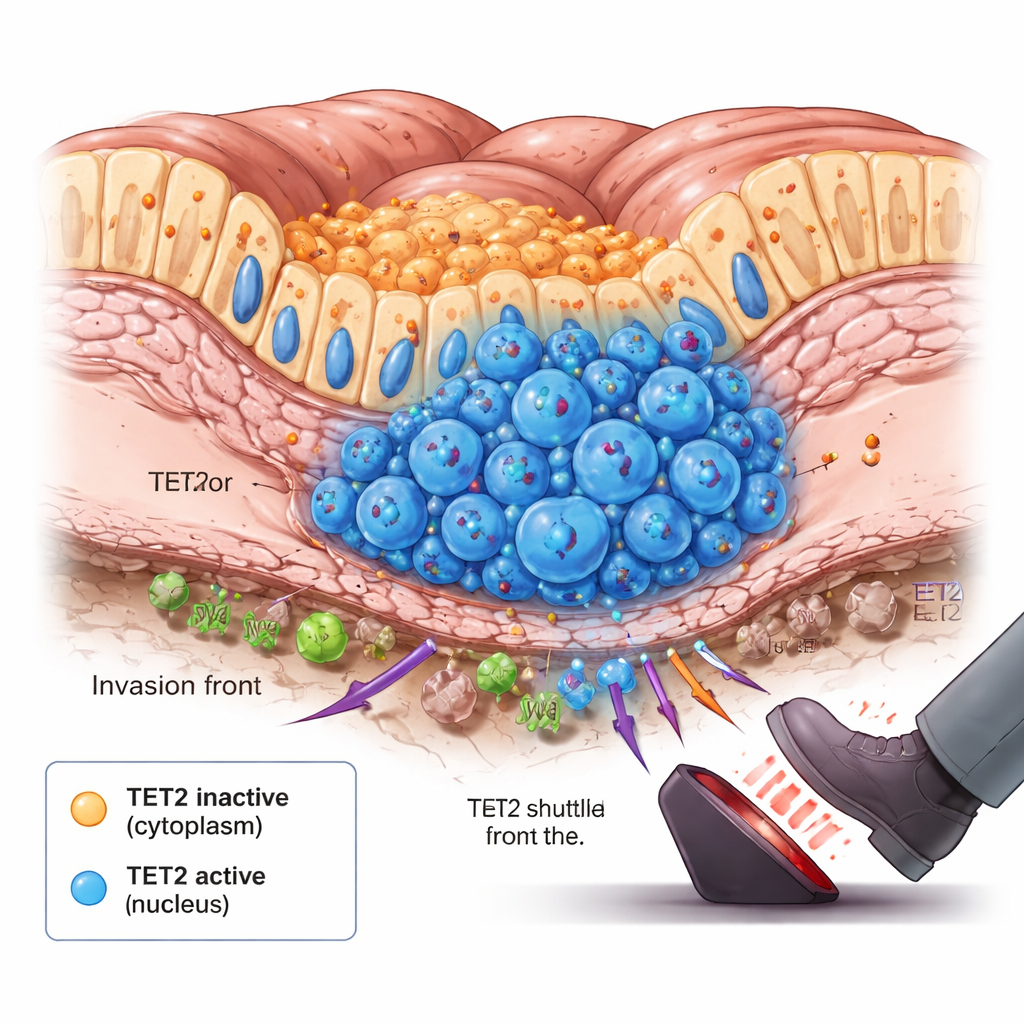
La ligne de front tumorale et le moment du basculement
En creusant davantage, l’équipe a constaté quelque chose de surprenant : dans les tumeurs qui commençaient tout juste à se propager, on observait une légère augmentation des cellules où TET2 s’était déplacée vers le noyau. Ces cellules se concentraient à la base de l’épithélium intestinal, au front d’invasion où les cellules cancéreuses commencent à pénétrer les tissus profonds. Des expériences animales et des modèles de culture cellulaire à long terme reproduisant la croissance tumorale ont montré un schéma comparable au fil du temps. Au début, TET2 restait dans le cytoplasme et était en grande partie inactive. À mesure que les tumeurs grandissaient et que des régions internes devenaient en manque d’oxygène et de nutriments, des signaux intracellulaires déclenchaient le transport de TET2 vers le noyau dans des sous‑populations spécifiques. Une fois dans le noyau, TET2 commençait à enlever des marques de méthylation de l’ADN et à freiner la croissance tumorale, agissant comme un frein d’urgence lorsque le cancer franchissait un seuil dangereux.
Quand les signaux « avance » déclenchent aussi un frein
Les tumeurs colorectales s’appuient souvent sur deux programmes puissants d’« avance » : un processus de changement de forme appelé transition épithélio‑mésenchymateuse (EMT), qui rend les cellules plus mobiles et invasives, et la voie de signalisation WNT, qui stimule la croissance et la survie. Ces voies sont généralement considérées comme purement délétères dans le cancer. Cependant, cette étude montre que lorsque EMT et WNT s’activent fortement, elles favorisent aussi le déplacement de TET2 vers le noyau. À l’aide de drogues et d’outils génétiques en culture cellulaire, les scientifiques ont montré que l’activation d’EMT ou de WNT augmentait le nombre de cellules transférant TET2 dans leur noyau, tandis que le blocage de ces voies produisait l’effet inverse. Une fois nucléaire, TET2 actif réprimait ensuite les gènes liés à EMT et à WNT, réduisant la migration cellulaire et ralentissant la prolifération. Autrement dit, les mêmes signaux qui facilitent la croissance tumorale réveillent aussi une force interne de contrepoids.
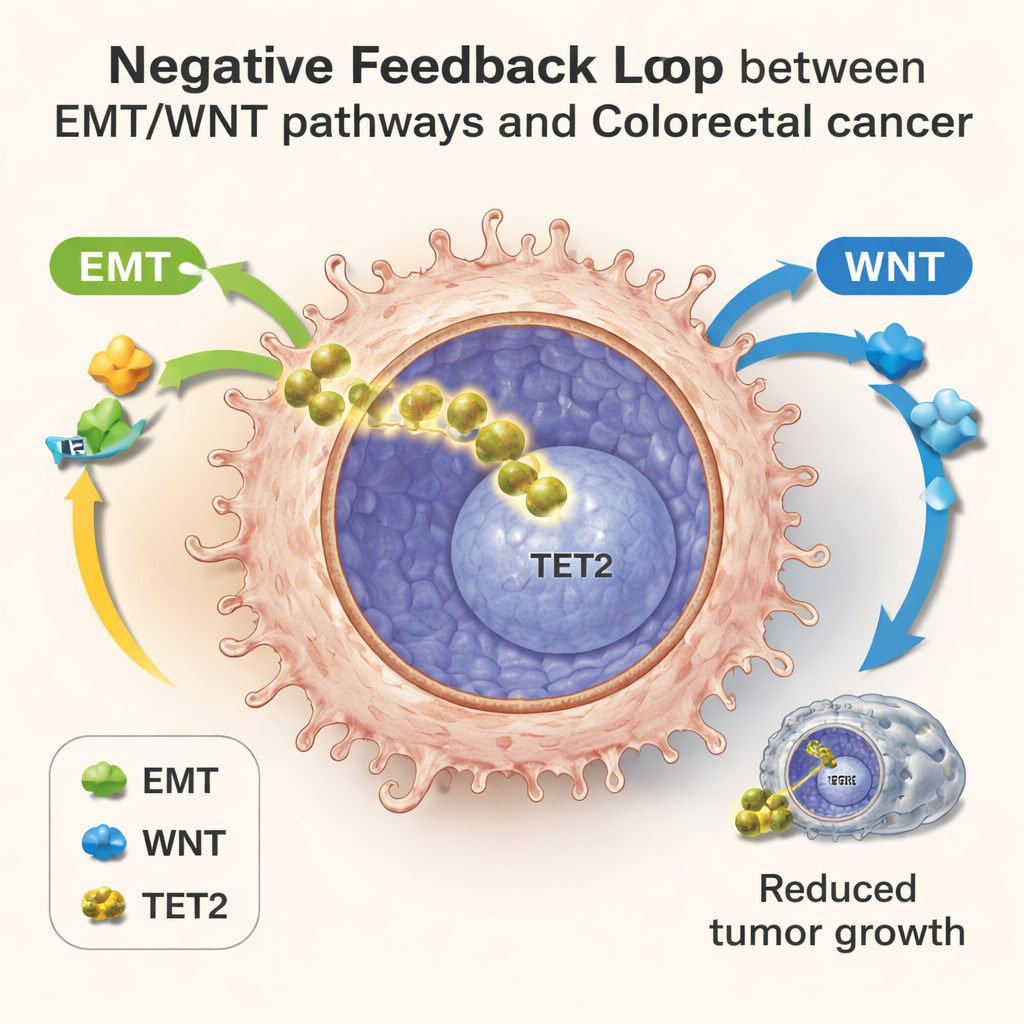
Les cellules individuelles révèlent une boucle de rétroaction cachée
Pour cartographier ce bras de fer en détail, l’équipe a utilisé le séquençage ARN monocellulaire, qui indique quels gènes sont actifs dans des milliers de cellules individuelles simultanément. Dans des colonies cultivées en laboratoire, dans des tumeurs de souris et dans des échantillons de patients atteints de cancer colorectal, ils ont observé des cellules réparties le long d’une chronologie de progression. Les cellules précoces présentaient un métabolisme normal et une faible activité EMT/WNT ; les cellules plus avancées montraient une réorganisation métabolique, une forte activation d’EMT/WNT, puis une hausse des gènes cibles de TET2. À ces stades tardifs, les cellules présentant une activité TET2 plus élevée affichaient des niveaux réduits de gènes liés à l’invasion et étaient associées à de meilleurs résultats pour les patients, même parmi les tumeurs ayant déjà commencé à se propager. Ce schéma soutient l’idée d’une boucle de rétroaction négative : le stress métabolique et l’activation EMT/WNT poussent TET2 dans le noyau, et TET2 nucléaire restreint à son tour ces programmes agressifs.
Ce que cela signifie pour les traitements futurs du cancer
Pour les non‑spécialistes, le message clé est que la progression du cancer colorectal n’est pas un simple interrupteur « marche/arrêt » entre comportements bons et mauvais. Il existe plutôt un mécanisme de sécurité intégré et différé : à mesure que les cellules tumorales deviennent plus invasives, elles activent aussi TET2 dans leur noyau, ce qui les freine partiellement. Avec le temps, de nombreuses tumeurs échappent à ce contrôle en perdant TET2 nucléaire ou en surpassant ses effets. En trouvant des moyens de maintenir TET2 dans le noyau ou d’en renforcer l’activité — éventuellement en combinaison avec des médicaments modulant EMT ou WNT — les cliniciens pourraient consolider ce frein naturel et ralentir la propagation du cancer. Plutôt que de s’attaquer uniquement aux cellules cancéreuses de l’extérieur, les thérapies futures pourraient viser à restaurer et amplifier ce système de contrôle interne.
Citation: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
Mots-clés: cancer colorectal, TET2, épigénétique, EMT signalisation WNT, progression du cancer