Clear Sky Science · fr
Cibler ENO1 reprogramme la polarisation des macrophages pour déclencher l’immunité antitumorale et améliore l’effet thérapeutique de la radiothérapie
Transformer les boucliers tumoraux en cibles
Le cancer survit souvent non seulement en croissant rapidement, mais aussi en neutralisant discrètement les défenses de l’organisme. Cette étude explore une molécule cachée à la surface des cellules cancéreuses, appelée ENO1, qui aide les tumeurs à échapper au système immunitaire et à résister à la radiothérapie. En développant un nouvel anticorps thérapeutique ciblant ENO1, les chercheurs montrent qu’il est possible d’assécher la tumeur de ses composés protecteurs, de réveiller les cellules immunitaires et d’améliorer l’efficacité de la radiothérapie dans des modèles de cancer colorectal et de cancer du sein triple négatif. 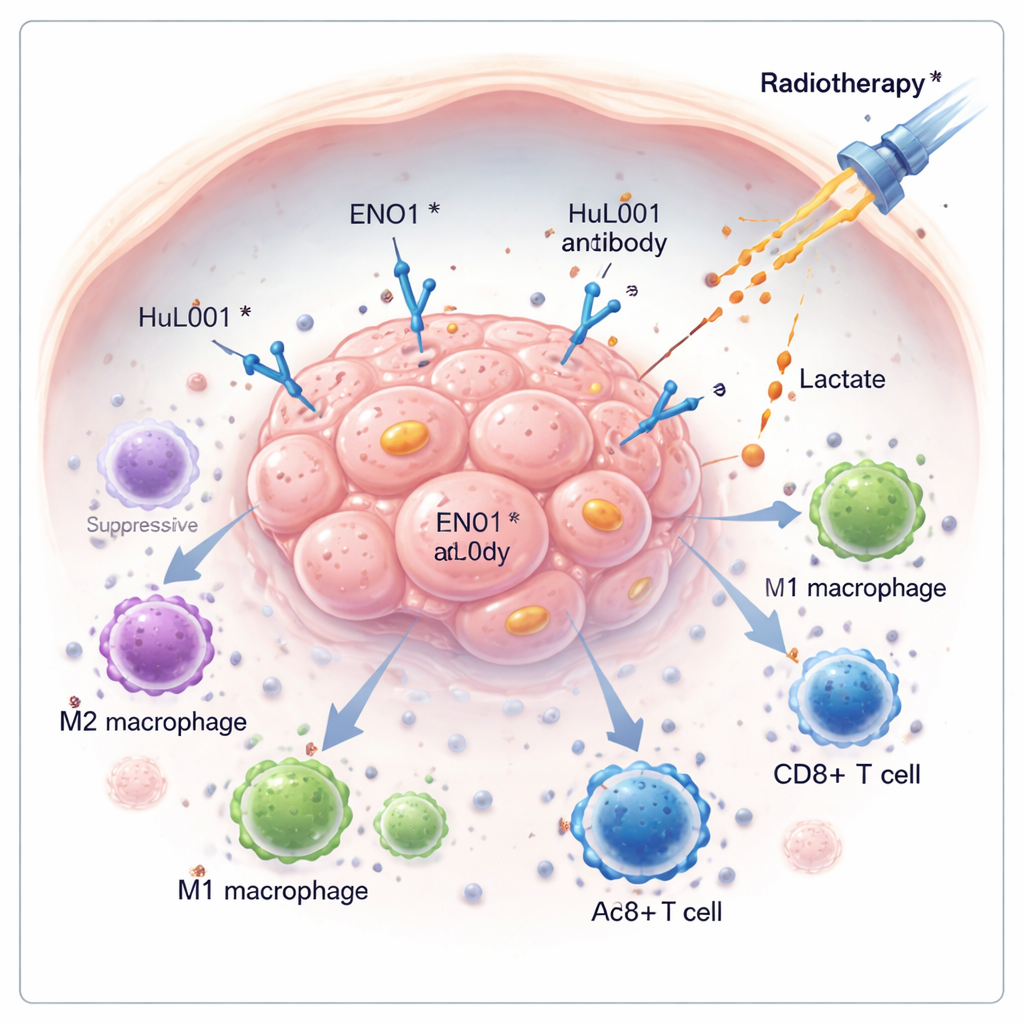
Une astuce métabolique qui fait taire l’immunité
De nombreuses tumeurs réorganisent leur utilisation de l’énergie en dégradant le sucre d’une manière qui produit de grandes quantités d’acide lactique, même en présence d’oxygène. Cet acide lactique est expulsé des cellules cancéreuses et s’accumule autour de la tumeur, transformant le microenvironnement en une niche acide et hostile qui affaiblit l’attaque immunitaire. Dans ce travail, les auteurs se concentrent sur ENO1, une enzyme impliquée dans la dégradation du sucre qui peut également apparaître à la surface des cellules cancéreuses. Lorsqu’elle est localisée en surface, ENO1 s’associe à une autre protéine, un transporteur appelé MCT4, pour aider à exporter le lactate — alimentant ainsi un environnement qui favorise la croissance tumorale et supprime les cellules immunitaires.
Comment la radiothérapie peut se retourner contre nous
La radiothérapie vise à endommager l’ADN tumoral et à déclencher des réponses immunitaires, mais elle a aussi des effets secondaires dans le microenvironnement tumoral. L’équipe a découvert que des signaux induits par une molécule appelée TGFβ1, qui sont amplifiés par la radiothérapie, activent une enzyme (PRMT5) qui modifie chimiquement ENO1 et le déplace à la surface des cellules cancéreuses. Une fois en surface, ENO1 interagit physiquement avec MCT4 pour le stabiliser et favoriser l’export du lactate. Des niveaux plus élevés d’ENO1 de surface ont été observés chez des patients atteints de cancers colorectaux et de cancers du sein triple négatif avancés et étaient associés à davantage de métastases et à une survie plus faible, suggérant que la radiothérapie peut involontairement renforcer un bouclier immunosuppresseur axé sur le lactate autour des tumeurs.
Reprogrammer cellules immunitaires amies et ennemies
Dans le halo acide entourant les tumeurs, des cellules immunitaires appelées macrophages sont poussées vers un état « réparateur » (souvent qualifié de M2) qui aide en réalité les tumeurs en atténuant l’inflammation et en favorisant la réparation, plutôt qu’en éliminant les cellules cancéreuses. Les chercheurs ont créé un anticorps humanisé, HuL001, qui reconnaît ENO1 sur les cellules cancéreuses de souris et d’humain. En culture cellulaire et dans des modèles murins, HuL001 a perturbé le soutien d’ENO1 à MCT4, réduit la libération de lactate et déplacé les macrophages hors de l’état M2 promoteur de tumeur vers un état M1, plus agressif contre le cancer et plus apte à phagocyter les cellules tumorales. Il est important de noter que HuL001 ne tuait pas simplement les macrophages ; il les a rééduqués tout en augmentant directement la mort des cellules cancéreuses.
Renforcer l’efficacité de la radiothérapie
Lorsque HuL001 a été combiné à la radiothérapie dans des modèles murins de cancer colorectal et de cancer du sein triple négatif, les tumeurs ont diminué davantage, repoussé plus lentement et, chez de nombreux animaux, ont totalement disparu. 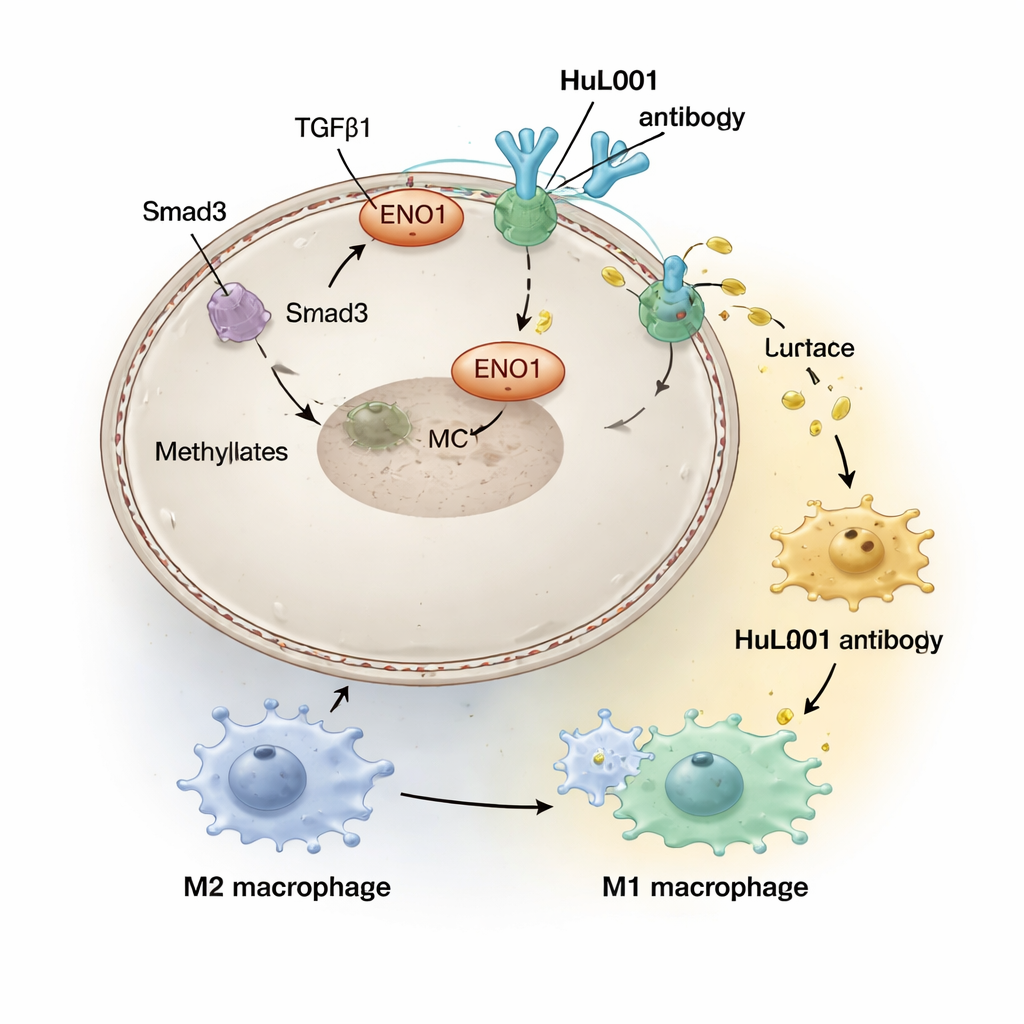
Des voies complexes à une promesse pratique
Pour les non-spécialistes, le message de cette étude est que la chimie d’une tumeur et son voisinage de cellules immunitaires sont profondément imbriqués. ENO1 se trouve à un carrefour : il aide les tumeurs à brûler le sucre, à exporter l’acide lactique et à recruter le mauvais type d’aide immunitaire. En bloquant ENO1 de surface avec un anticorps ciblé, les chercheurs ont pu réduire l’accumulation nocive de lactate, faire basculer les macrophages d’aidants de la tumeur en combattants de la tumeur et rendre la radiothérapie plus efficace dans des modèles de cancers difficiles à traiter. Bien que HuL001 ne soit pas encore un médicament clinique, ce travail suggère que viser des gardiens métaboliques comme ENO1 pourrait devenir un moyen puissant de retourner les défenses d’une tumeur contre elle-même et d’améliorer des traitements existants tels que la radiothérapie.
Citation: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
Mots-clés: métabolisme tumoral, polarisation des macrophages, radiothérapie, immunothérapie, lactate