Clear Sky Science · fr
Sec8 : un nouveau régulateur positif de RIG‑I dans la défense antivirale contre les virus à ARN
Comment nos cellules repèrent des virus furtifs
Beaucoup de virus dangereux, y compris la grippe et des virus animaux émergents, transportent leur matériel génétique sous forme d’ARN. Nos cellules s’appuient sur des systèmes d’alarme internes pour détecter rapidement ces intrus et déclencher une réponse antivirale. Cet article explore une protéine cellulaire peu connue appelée Sec8 et montre qu’elle joue discrètement un rôle central pour maintenir l’un de nos senseurs viraux clés, RIG‑I, suffisamment longtemps en vie et actif pour nous protéger.
Une alarme cellulaire menacée
RIG‑I est une « alarme » moléculaire qui patrouille l’intérieur des cellules à la recherche de fragments d’ARN viral. Lorsqu’il détecte un ARN suspect, il change de conformation, s’active et envoie des signaux qui aboutissent à la production d’interférons de type I — des molécules d’alerte puissantes qui aident les cellules voisines à résister à l’infection et activent les défenses immunitaires. Parce qu’une alarme hyperactive peut provoquer une inflammation nuisible ou des maladies auto‑immunes, les cellules contrôlent strictement les niveaux de RIG‑I. Plusieurs autres protéines peuvent marquer RIG‑I pour destruction en lui ajoutant de petites chaînes d’ubiquitine, le conduisant vers le « broyeur » cellulaire appelé protéasome. Jusqu’à présent, on ne savait pas quels facteurs cellulaires supplémentaires protègent RIG‑I d’une élimination prématurée, notamment durant une infection active par un virus à ARN.
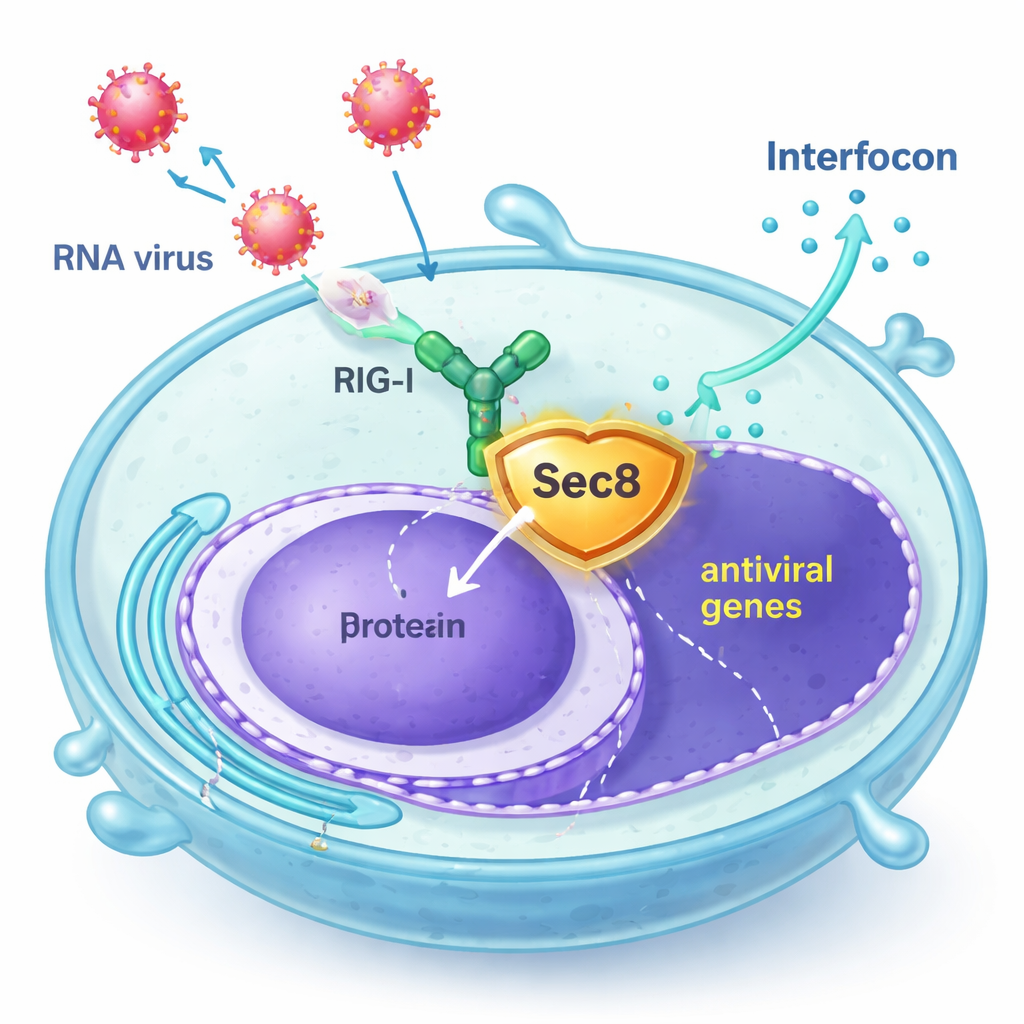
Sec8 intervient en tant que garde du corps
Les auteurs ont découvert que Sec8, surtout connu comme composant d’un complexe de huit protéines qui aide les vésicules sécrétoires à fusionner avec la membrane cellulaire, renforce en réalité la signalisation antivirale. Dans des lignées cellulaires humaines et dans des cellules immunitaires primaires de souris, une augmentation des niveaux de Sec8 a conduit à une activation plus forte des gènes liés aux interférons après infection par des virus à ARN tels que le virus de la stomatite vésiculaire (VSV) et le virus de Sendai, ou après exposition à de l’ARN viral synthétique. À l’inverse, la réduction de Sec8 diminuait la production d’interférons et des gènes stimulés par l’interféron, laissant les cellules moins capables de résister à la réplication virale. Ces résultats suggèrent que Sec8 agit non seulement dans la sécrétion, mais aussi comme un régulateur positif au sein de la voie d’alarme antivirale.
Bloquer le broyeur cellulaire
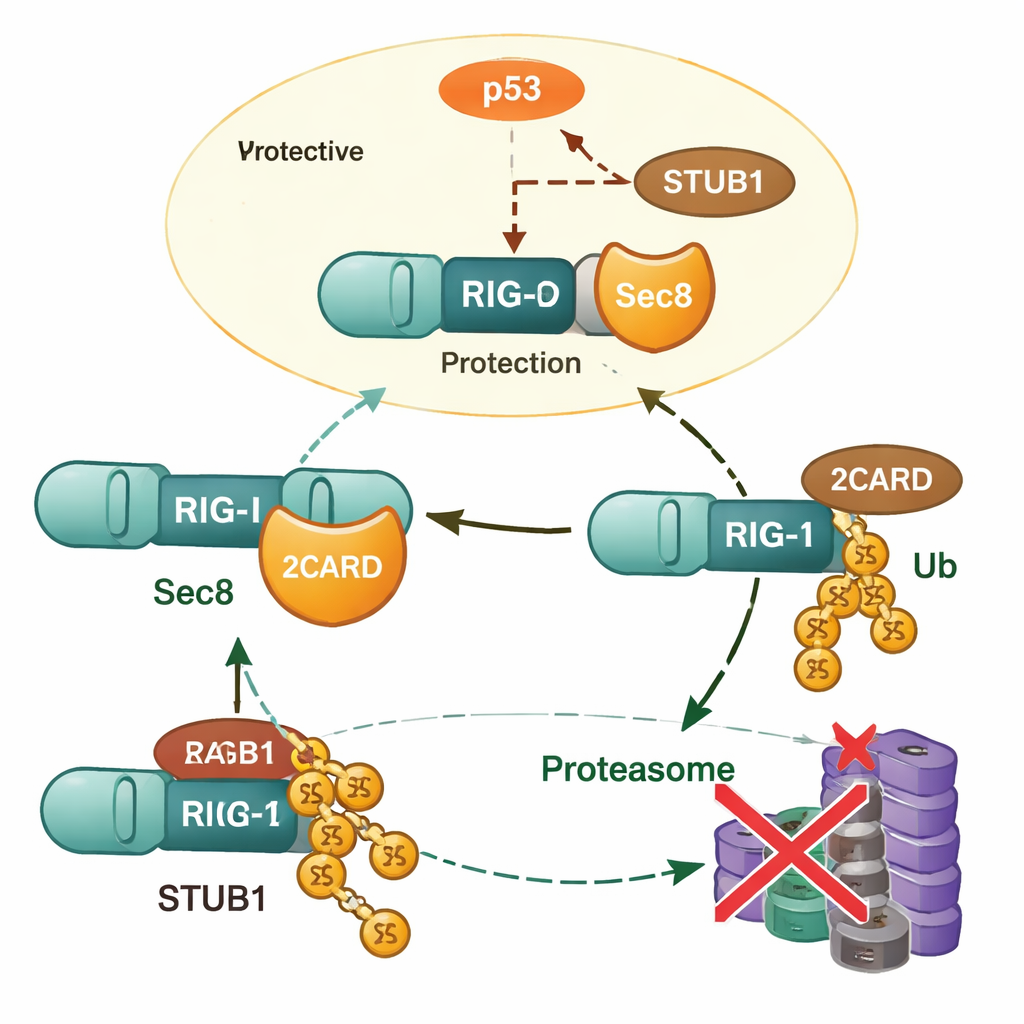
En creusant davantage, les chercheurs ont constaté que Sec8 n’augmente pas l’expression du gène RIG‑I ; au lieu de cela, il empêche la dégradation de la protéine RIG‑I. Lorsque Sec8 était supprimé, les niveaux de RIG‑I chutaient plus rapidement, et cette perte pouvait être prévenue par des médicaments bloquant le protéasome, impliquant ainsi la machinerie de recyclage protéique de la cellule. L’équipe a identifié une autre protéine, STUB1, comme étant un « étiqueteur » clé qui attache un type spécifique de chaîne d’ubiquitine (liée en K48) à RIG‑I sur un acide aminé appelé lysine 190. Cette marque dirige RIG‑I vers la destruction. Sec8 interfère avec ce processus de deux manières : il entre en compétition physique avec STUB1 pour se lier à la même région d’activation de RIG‑I, et il réduit la quantité de STUB1 produite par la cellule.
Sec8, p53 et le contrôle de l’étiqueteur
Pour expliquer comment Sec8 réduit la production de STUB1, les auteurs se sont intéressés à la régulation génique. Ils ont identifié un court segment d’ADN qui agit comme le noyau de l’interrupteur d’activation (promoteur) du gène STUB1 et ont montré que la célèbre protéine suppresseur de tumeur p53 se lie à cette région et augmente les niveaux de STUB1. Sec8 atténue à la fois la quantité et la phosphorylation activatrice de p53, de sorte que p53 ne peut plus stimuler efficacement la production de STUB1. Lorsque p53 était bloqué ou que STUB1 était silencé, les effets néfastes de la perte de Sec8 sur la production d’interférons et la croissance virale étaient en grande partie inversés. Cela place Sec8 au sommet d’une chaîne de régulation qui va de p53 à STUB1 et enfin à la stabilité de RIG‑I.
De la boîte de Pétri aux animaux vivants
L’équipe a ensuite testé l’importance de Sec8 chez des souris génétiquement modifiées pour manquer du gène Sec8 spécifiquement dans certains types cellulaires immunitaires. Après infection par le VSV, ces animaux produisaient moins d’interféron, portaient des quantités plus élevées de virus dans des organes tels que la rate, le foie et les poumons, et présentaient des lésions pulmonaires plus sévères, une perte de poids plus importante et une survie réduite par rapport aux souris témoins. Ces résultats in vivo confirment que Sec8 n’est pas un acteur mineur mais un protecteur significatif contre l’infection par des virus à ARN au niveau de l’organisme entier.
Pourquoi cela compte pour de futures thérapies
En termes simples, cette étude montre que Sec8 agit comme un garde du corps pour le senseur antiviral RIG‑I. En maintenant l’étiqueteur STUB1 sous contrôle et en protégeant directement RIG‑I contre l’envoi au broyeur cellulaire, Sec8 permet aux cellules de déclencher une réponse en interféron en temps utile et de mieux contrôler les virus à ARN. Comprendre ce nouvel axe p53–STUB1–RIG‑I ouvre la voie à des stratégies antivirales futures visant à stabiliser RIG‑I ou à imiter les actions protectrices de Sec8, renforçant potentiellement nos défenses contre un large éventail d’infections virales à base d’ARN.
Citation: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Mots-clés: immunité innée, virus à ARN, RIG‑I, ubiquitination, signalisation de l'interféron