Clear Sky Science · fr
Les fibroblastes associés au cancer (CAF) dérivés de MFAP2 favorisent la prolifération et les métastases du CCR tout en supprimant l’immunité antitumorale médiée par les cellules CD8+ T
Pourquoi le voisinage de la tumeur compte
Le cancer colorectal est l’un des cancers les plus fréquents et les plus meurtriers au monde, et les cliniciens peinent encore à empêcher sa propagation et à prédire quels patients auront un mauvais pronostic. Cette étude n’examine pas seulement les cellules cancéreuses elles‑mêmes, mais leurs « voisins » : les cellules de soutien et les cellules immunitaires qui partagent le même milieu. Les chercheurs dévoilent comment un type particulier de cellules auxiliaires, les fibroblastes associés au cancer, peut discrètement stimuler la croissance tumorale et réduire l’efficacité des lymphocytes T tueurs du corps. Comprendre cette conversation cachée pourrait ouvrir la voie à de nouveaux traitements rendant les thérapies actuelles plus efficaces.
Aides cachés à l’intérieur des tumeurs du côlon
Les tumeurs du côlon ne sont pas de simples amas de cellules malignes ; ce sont des écosystèmes en miniature. Parmi les habitants les plus importants figurent les fibroblastes associés au cancer, ou CAF. Ces cellules déposent la matrice conjonctive, remodèlent l’environnement tumoral et libèrent des signaux. En analysant des échantillons de patients et de larges bases de données génomiques, les auteurs ont constaté qu’une protéine nommée MFAP2 est beaucoup plus abondante dans les tumeurs colorectales que dans le tissu colique normal, et que les patients présentant davantage de MFAP2 ont tendance à avoir une survie moindre. Ils ont montré que ce sont les CAF, et non les cellules cancéreuses elles‑mêmes, qui produisent principalement MFAP2 dans ces tumeurs. En cultures cellulaires et dans des modèles murins, des CAF riches en MFAP2 étaient étroitement associés à une croissance tumorale plus rapide et à un comportement plus agressif.
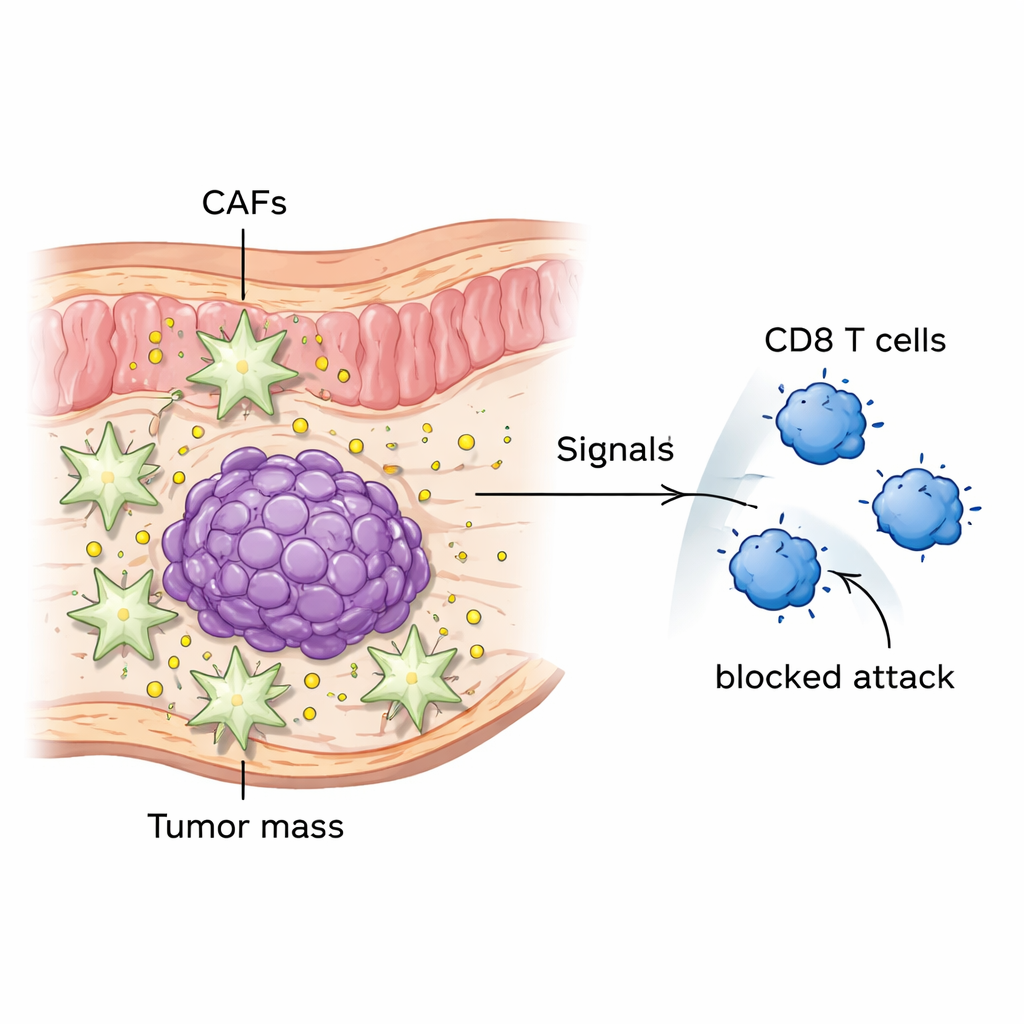
Un commutateur de croissance sur les cellules cancéreuses
L’équipe s’est ensuite demandé comment MFAP2 poussait effectivement les cellules cancéreuses à croître et à se disséminer. Ils ont découvert que MFAP2 libéré par les CAF se fixe à un récepteur appelé intégrine β8 (ITGB8) à la surface des cellules du cancer colorectal. Ce contact active une chaîne de signalisation interne connue sous le nom de voie FAK–ERK1/2, bien reconnue pour favoriser la multiplication et la mobilité cellulaires. L’un des régulateurs géniques activés par cette voie est un facteur nommé ETS2. Quand ETS2 augmente, les cellules du cancer du côlon deviennent plus invasives et mieux à même de survivre, même face aux cellules immunitaires qui tentent de les éliminer. Lorsque les chercheurs ont bloqué MFAP2 ou ITGB8, ou réduit ETS2, les tumeurs chez la souris ont diminué et formé moins de métastases hépatiques.
Comment les tumeurs empêchent l’attaque immunitaire
Les tumeurs du côlon sont souvent infiltrées par des lymphocytes T CD8 — des cellules immunitaires spécialisées dans la reconnaissance et l’élimination des cellules cancéreuses. Les patients dont les tumeurs contiennent davantage de ces cellules vivent généralement plus longtemps. Pour autant, dans les tumeurs riches en MFAP2, les chercheurs ont trouvé moins de lymphocytes CD8 et des signes indiquant que ceux présents étaient épuisés et moins efficaces. Ils ont attribué cet effet à une modification du traitement du cholestérol par les cellules tumorales. ETS2 stimule la production d’une enzyme appelée CYP27A1, qui convertit le cholestérol en une molécule nommée 27‑hydroxycholestérol (27‑HC). Cette molécule lipidique agit ensuite sur un senseur des lymphocytes T appelé LXRβ, qui atténue leur activité. En cultures cellulaires comme chez la souris, plus de MFAP2 signifiait plus de 27‑HC dans le microenvironnement tumoral, plus de mort et de dysfonction des T, et une croissance tumorale accrue.
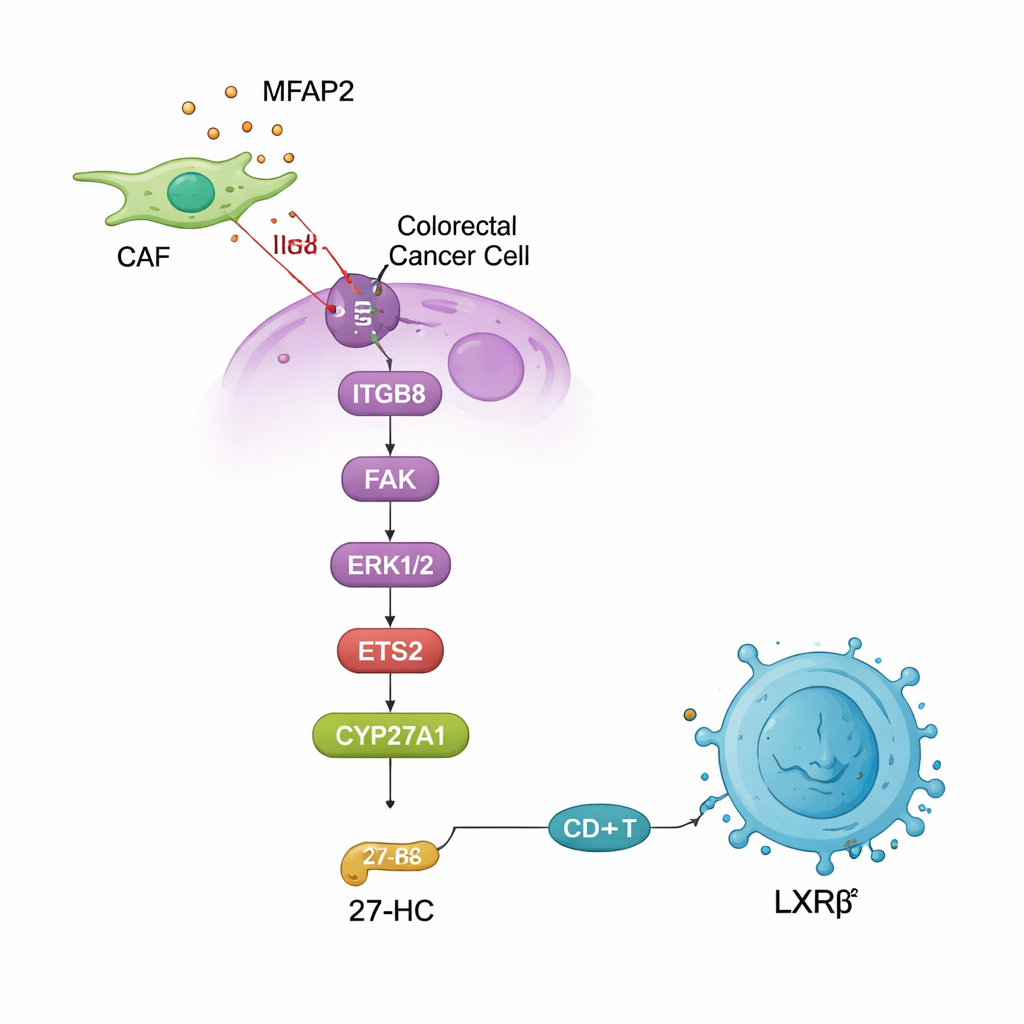
Relier métabolisme, fibroblastes et évasion immunitaire
Ce travail relie plusieurs aspects apparemment distincts de la biologie du cancer : les cellules de soutien autour de la tumeur, la signalisation interne des cellules tumorales, et la manière dont la tumeur reprogramme le métabolisme lipidique pour neutraliser les défenses immunitaires. En plaçant MFAP2 au sommet d’une chaîne passant par ITGB8, FAK, ERK1/2, ETS2 et CYP27A1, et se terminant par le 27‑HC désactivant les lymphocytes CD8 via LXRβ, les chercheurs décrivent une voie complète allant du signal des fibroblastes à l’évasion immunitaire. Fait important, bloquer MFAP2 ou ETS2 a non seulement ralenti la croissance tumorale mais aussi restauré l’infiltration et la fonction des T chez la souris, suggérant que cette voie pourrait être ciblée pour améliorer l’efficacité de l’immunothérapie et des traitements standards.
Ce que cela signifie pour les traitements futurs
Pour un public non spécialiste, le message essentiel est que certains des acteurs les plus néfastes dans le cancer du côlon ne sont pas uniquement les cellules tumorales, mais leurs complices et les signaux chimiques qu’ils envoient. MFAP2, produit par les fibroblastes du microenvironnement tumoral, aide les cellules cancéreuses à croître et les protège contre l’attaque en affaiblissant les lymphocytes T tueurs via un signal basé sur le cholestérol. Parce que cette chaîne pilotée par MFAP2 comporte plusieurs étapes — au niveau du fibroblaste, de la surface des cellules cancéreuses, de la signalisation intracellulaire et de la cellule T — elle offre plusieurs cibles potentielles pour de nouveaux médicaments. Des thérapies interrompant cette voie pourraient à la fois ralentir la dissémination tumorale et « réveiller » les T épuisés, améliorant le pronostic des patients atteints de cancer colorectal.
Citation: Zhang, X., Fei, Y., Xie, C. et al. Cancer-associated fibroblasts (CAFs) derived from MFAP2 promote CRC proliferation and metastasis while suppressing CD8+ T cell-mediated antitumor immunity. Cell Death Dis 17, 159 (2026). https://doi.org/10.1038/s41419-026-08413-w
Mots-clés: cancer colorectal, microenvironnement tumoral, fibroblastes associés au cancer, évasion immunitaire, métabolisme du cholestérol