Clear Sky Science · fr
La transmission du lactate par les cellules tumorales hypoxiques favorise la sénescence des macrophages et leur polarisation M2 via l’axe DNMT1‑NHE7, accélérant la progression du cancer de l’endomètre
Pourquoi priver les tumeurs d’oxygène a de l’importance
Le cancer de l’endomètre, qui prend naissance dans la muqueuse utérine, devient plus fréquent dans le monde. De nombreuses tumeurs avancées sont difficiles à traiter parce qu’elles récidivent, se disséminent ou résistent aux thérapies standard. Cette étude examine ce qui se passe à l’intérieur de ces tumeurs lorsqu’elles manquent d’oxygène — une caractéristique courante des cancers à croissance rapide — et montre comment un simple déchet métabolique, le lactate, peut reprogrammer les cellules immunitaires voisines pour favoriser la croissance tumorale plutôt que de la combattre.
Le manque d’oxygène transforme les tumeurs en usines à lactate
À mesure que les cellules du cancer de l’endomètre se multiplient, leur apport sanguin devient insuffisant, créant des poches d’hypoxie. Les cellules répondent en activant un régulateur maître appelé HIF1A qui reconfigure leur métabolisme énergétique. Plutôt que de s’appuyer principalement sur une production d’énergie efficace, elles augmentent la glycolyse, un processus rapide mais peu économe qui génère de grandes quantités de lactate. Les chercheurs ont analysé des données tumorales de centaines de patients et ont constaté que des niveaux plus élevés de HIF1A s’accompagnaient d’une activité accrue de nombreux gènes liés à la glycolyse et des transporteurs qui expulsent le lactate des cellules cancéreuses. Les patients dont les tumeurs présentaient davantage de HIF1A avaient tendance à avoir un pronostic plus défavorable, ce qui suggère que ce basculement métabolique est étroitement lié à une maladie agressive.
Comment les déchets tumoraux reconfigurent des cellules immunitaires utiles
Les macrophages sont des cellules immunitaires qui peuvent soit attaquer les tumeurs, soit les soutenir, selon leur état. Dans ce travail, l’équipe montre que, en hypoxie, les cellules du cancer de l’endomètre libèrent beaucoup plus de lactate dans leur environnement. Ce lactate est exporté via un transporteur appelé MCT3 sur les cellules tumorales puis importé dans les macrophages par un autre transporteur, MCT1. Une fois à l’intérieur, le lactate pousse les macrophages hors d’un mode défensif vers l’état dit M2, associé à la réparation tissulaire, à la suppression de l’inflammation et, malheureusement, au soutien de la croissance tumorale. En laboratoire, des macrophages exposés à un liquide tumoral riche en lactate présentaient davantage de marqueurs de type M2, et le fluide qu’ils sécrétaient favorisait à son tour la prolifération, la migration et l’invasion des cellules cancéreuses. 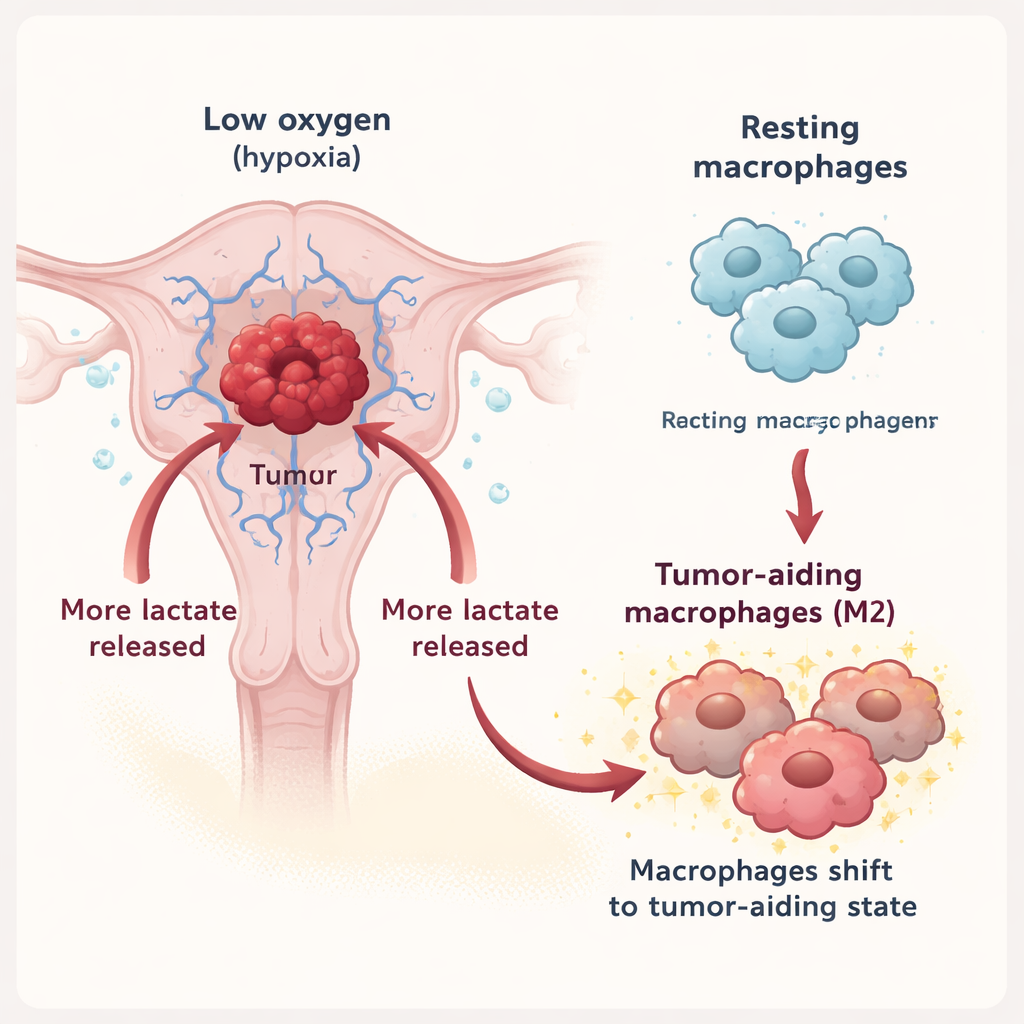
Un interrupteur épigénétique qui éteint une « soupape » de pH cellulaire
L’étude va plus loin en dévoilant l’interrupteur moléculaire à l’intérieur des macrophages qui relie le lactate tumoral à ce comportement nocif. Le lactate ne se contente pas de circuler ; il peut modifier les histones dans le noyau — une marque chimique connue sous le nom de lactylation — qui influence l’expression des gènes. Les chercheurs ont observé que le lactate augmente une marque histone spécifique sur la région de contrôle du gène DNMT1, en augmentant son activité. DNMT1 est une enzyme qui ajoute des groupes méthyle à l’ADN et peut silencier des gènes. L’une de ses cibles ici est NHE7, une protéine qui contribue à réguler l’acidité à l’intérieur de certains compartiments cellulaires. Lorsque DNMT1 est stimulée, elle accroît la méthylation du gène NHE7, le réprimant. La réduction de NHE7 perturbe l’équilibre du pH interne et active une voie de signalisation connue sous le nom de voie MAPK. Cette voie, à son tour, oriente les macrophages vers l’état pro‑tumoral M2 et vers une forme de vieillissement cellulaire dite sénescence, qui les enferme dans un mode chronique favorable à la tumeur.
De la réaction en chaîne moléculaire à des tumeurs à croissance accélérée
Pour vérifier si cette cascade a un impact in vivo, les scientifiques ont créé des modèles murins dans lesquels des cellules de cancer de l’endomètre humaines étaient cultivées avec des macrophages de type humain. Lorsqu’un excès de lactate était fourni, les tumeurs étaient plus volumineuses, comportaient davantage de cellules en division et contenaient plus de macrophages de type M2 et sénescents, avec un DNMT1 élevé et un NHE7 faible. Fait marquant, lorsque les macrophages étaient modifiés pour surexprimer NHE7, l’effet stimulant du lactate sur la tumeur était atténué : les tumeurs étaient plus petites, présentaient plus de cellules en apoptose et contenaient moins de macrophages M2 et sénescents. Le blocage de l’enzyme DNMT1 ou de la voie MAPK affaiblissait aussi la capacité du lactate à reprogrammer les macrophages, renforçant l’idée que ces molécules forment un axe connecté. 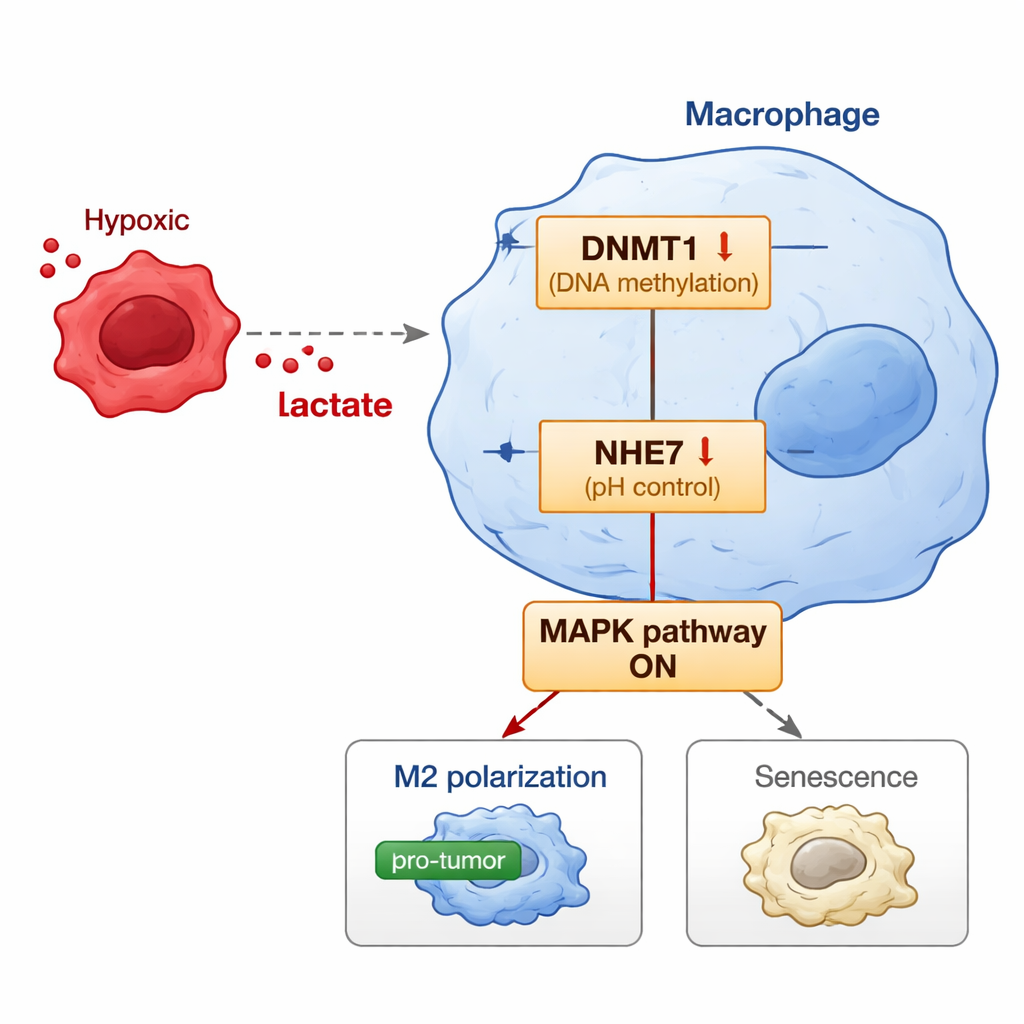
Transformer les ruses de la tumeur en cibles thérapeutiques
Pour le grand public, le message clé est que les tumeurs de l’endomètre peuvent exploiter l’hypoxie et le lactate — autrefois perçu comme de simples déchets cellulaires — pour « laver le cerveau » des cellules immunitaires voisines et les amener à aider le cancer. Elles le font via un relais épigénétique : le lactate stimule DNMT1, qui silencie NHE7, ce qui active ensuite une signalisation qui fige les macrophages dans un état sénescent et pro‑tumoral. En interférant avec n’importe quelle étape de cette chaîne lactate–DNMT1–NHE7–MAPK, il pourrait être possible de restaurer une activité immunitaire plus anti‑tumorale et de ralentir la croissance du cancer. Ce travail ouvre la voie à des thérapies futures qui ne ciblent pas seulement les cellules cancéreuses, mais qui rééduquent aussi les cellules immunitaires environnantes que la tumeur a retournées à son avantage.
Citation: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
Mots-clés: cancer de l’endomètre, microenvironnement tumoral, métabolisme du lactate, polarisation des macrophages, régulation épigénétique