Clear Sky Science · fr
Au‑delà du métabolisme : explorer les implications régulatrices et thérapeutiques du lactate et de la lactylation dans la mort cellulaire régulée par le cancer
Pourquoi un « déchet » du sucre compte en cancérologie
Pendant des décennies, le lactate — la substance qui fait brûler les muscles surmenés — a été considéré comme un déchet cellulaire. Cet article de synthèse montre qu’en cancérologie, le lactate est tout sauf un rebut. Il sert de carburant, de signal chimique et même d’interrupteur pouvant déterminer la survie ou la mort des cellules tumorales. Comprendre ce rôle caché pourrait ouvrir de nouvelles voies pour pousser les cellules cancéreuses à s’autodétruire tout en épargnant les tissus sains.
Le raccourci sucré qui reprogramme les cellules cancéreuses
Les cellules cancéreuses sont célèbres pour leur « dent sucrée ». Même quand l’oxygène est abondant, elles préfèrent dégrader rapidement le glucose en lactate plutôt que de l’oxyder complètement dans leurs mitochondries, un basculement connu sous le nom d’effet Warburg. Cette stratégie permet aux tumeurs de produire énergie et éléments de construction à grande vitesse. L’afflux de lactate ainsi généré est expulsé via des transporteurs spécifiques, façonnant un microenvironnement tumoral acide et riche en nutriments qui favorise la croissance et aide les tumeurs à s’adapter au stress, comme l’hypoxie ou la chimiothérapie.
Le lactate comme réglage pour différents types de mort cellulaire
La mort cellulaire dans notre organisme est généralement strictement contrôlée, aidant à éliminer les cellules endommagées ou dangereuses. Les cellules cancéreuses échappent souvent à ces programmes. Les auteurs décrivent comment le lactate peut à la fois bloquer et déclencher plusieurs voies de mort régulée — l’apoptose (le « suicide » cellulaire), l’autophagie (l’autodigestion), la ferroptose (dégâts membranaires liés au fer), la pyroptose (éclatement inflammatoire) et la cuproptose (effondrement lié au cuivre). Lorsque les cellules cancéreuses produisent ou importent des quantités modérées de lactate, elles l’utilisent comme carburant et signal de survie, activant des voies qui les protègent contre la chimiothérapie, la pénurie de nutriments ou les traitements ciblés. Mais quand le lactate s’accumule à l’intérieur des cellules, par exemple si son export est bloqué, le stress acide et les lésions mitochondriales qui en résultent peuvent inverser la tendance et pousser les cellules vers l’apoptose ou la ferroptose.
Lactylation : quand le lactate marque les protéines
Une découverte frappante récente est que le lactate peut être converti en une petite étiquette chimique et attaché aux résidus lysine des protéines, une modification appelée lactylation. Des enzymes agissent comme « rédacteurs » et « effaceurs » de ces marques, décorant aussi bien les histones associés à l’ADN que de nombreuses autres protéines. Ces marques modifient les gènes qui sont activés, le comportement des enzymes et la stabilité des régulateurs clés. En cancérologie, la lactylation ajuste finement l’équilibre entre survie et autodestruction. Elle peut, par exemple, augmenter des protéines qui bloquent l’apoptose, stimuler le recyclage via l’autophagie, protéger les cellules de la ferroptose en resserrant le contrôle du fer et en renforçant les antioxydants, ou modifier de nouvelles formes de mort comme la cuproptose en altérant la gestion des protéines sensibles au cuivre.
Une conversation bidirectionnelle entre métabolisme et programmes de mort
La relation n’est pas unilatérale : les voies de mort cellulaire reconfigurent aussi la manière dont les tumeurs utilisent le glucose et produisent du lactate. Quand les mitochondries sont endommagées lors d’une apoptose précoce ou d’une mitophagie (élimination sélective des mitochondries), les cellules retombent souvent sur une glycolyse rapide, augmentant la production de lactate. Les cellules de soutien environnantes, comme les fibroblastes associés à la tumeur, peuvent subir une reprogrammation similaire et devenir des usines à lactate qui nourrissent les cellules tumorales voisines. D’autres types de mort, comme la ferroptose, tendent à supprimer la glycolyse et donc à faire baisser les niveaux de lactate. Le résultat est une boucle de rétroaction dynamique dans laquelle métabolisme et mécanismes de mort s’ajustent continuellement à mesure que la tumeur évolue et répond au traitement.
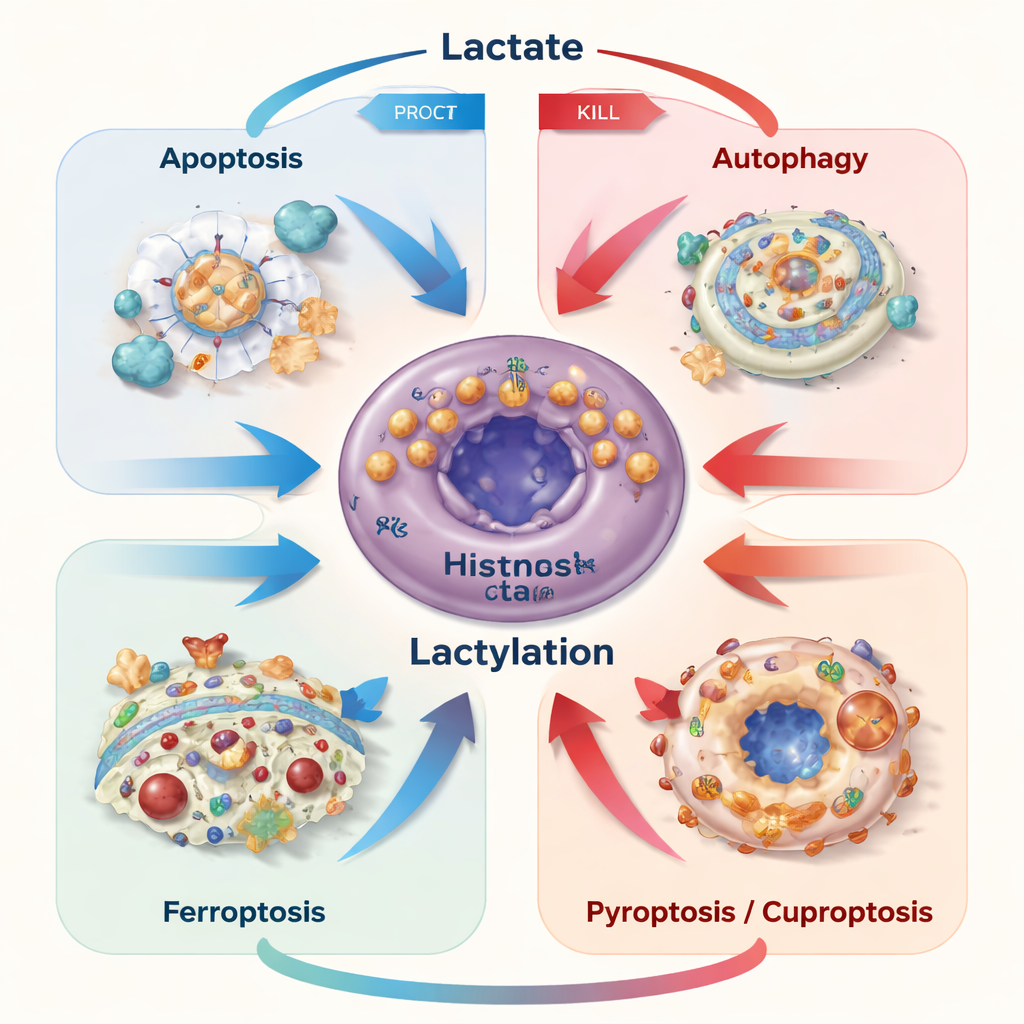
Transformer une faiblesse en stratégie thérapeutique
Parce que le lactate et la lactylation peuvent soit protéger soit tuer les cellules cancéreuses selon le contexte, les auteurs soutiennent que les thérapies doivent faire plus que simplement bloquer la production de lactate. À la place, les traitements futurs pourraient rediriger sélectivement les flux de lactate, ajuster ses transporteurs ou cibler des marques de lactylation spécifiques pour faire basculer les cellules cancéreuses tout en réénergisant les cellules immunitaires anti‑tumorales actuellement paralysées par l’environnement acide. Des systèmes intelligents d’administration de médicaments et des nanomédicaments qui répondent aux niveaux locaux de lactate ou de pH émergent comme des moyens pour appliquer cette précision. En termes simples, le message de l’article est que ce qui paraissait jadis être des détritus métaboliques est en réalité un puissant bouton de commande du destin des cellules cancéreuses — et apprendre à tourner ce bouton correctement pourrait rendre les thérapies existantes bien plus efficaces.
Citation: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
Mots-clés: lactate, lactylation, mort cellulaire cancéreuse, métabolisme tumoral, ferroptose