Clear Sky Science · fr
Empreintes fonctionnelles de l’insuffisance de recombinaison homologue dans le cancer de la prostate révélées par la fragmentation de l’ADNc circulant et l’accessibilité des facteurs de transcription
Pourquoi cela compte pour les patients atteints de cancer
De nombreux hommes atteints d’un cancer de la prostate avancé pourraient bénéficier de médicaments qui exploitent des fragilités dans la réparation de l’ADN de leurs tumeurs. Pourtant, aujourd’hui, les médecins manquent souvent d’identifier qui répondra, car les tests exigent généralement des biopsies tissulaires difficiles et se concentrent sur seulement quelques gènes. Cette étude montre comment une simple prise de sang peut être transformée en un compte rendu riche et multi-couches de ces faiblesses de réparation de l’ADN, orientant potentiellement des choix thérapeutiques plus précis et plus doux.
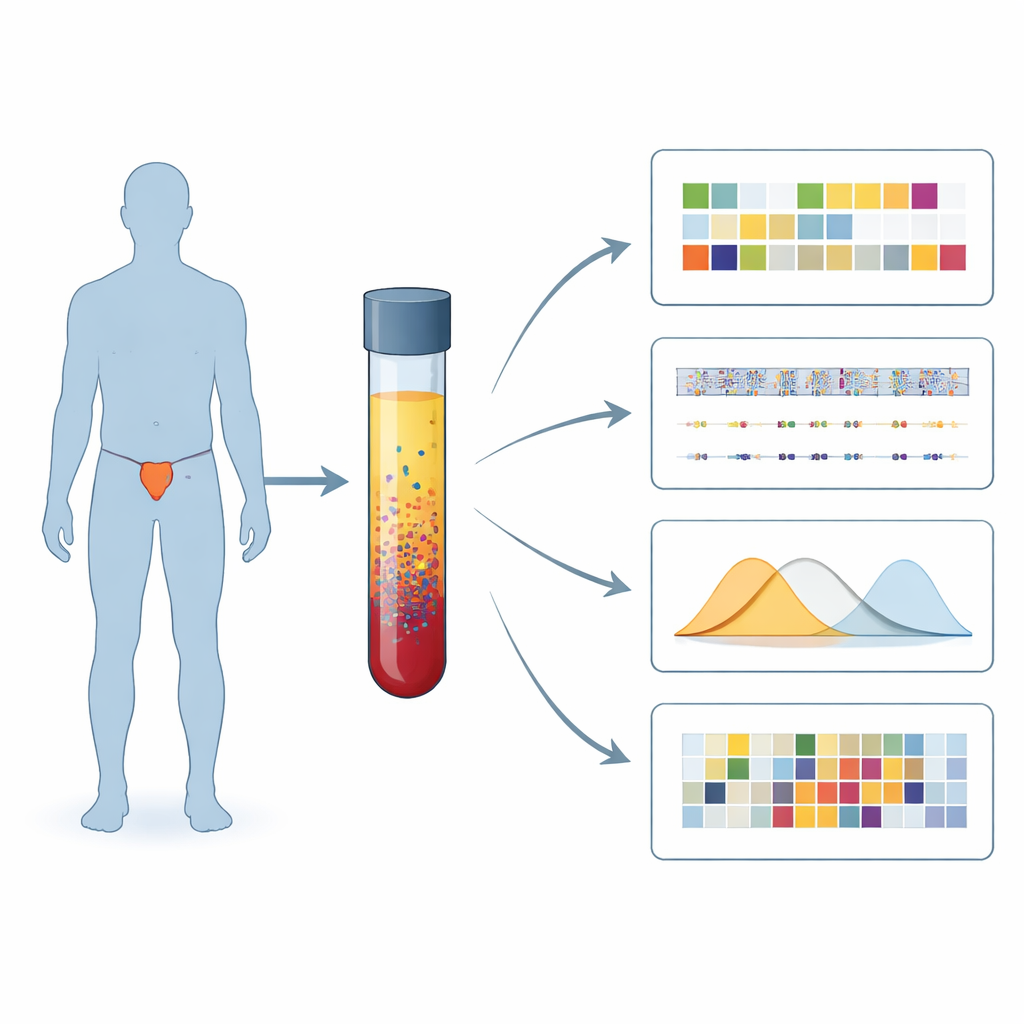
Une nouvelle façon de lire les signaux du cancer dans le sang
Les chercheurs se sont concentrés sur un problème de réparation particulier appelé déficience de recombinaison homologue, ou HRD, qui rend les tumeurs particulièrement vulnérables aux médicaments tels que les inhibiteurs de PARP et à certaines chimiothérapies. Au lieu de s’appuyer sur des échantillons tumoraux prélevés sur l’os ou la prostate, ils ont analysé des fragments d’ADN tumoral flottant dans la circulation sanguine, appelés ADN tumoral circulant. Sur 375 hommes atteints d’un cancer de la prostate métastatique, ils ont sélectionné 106 dont le sang portait suffisamment d’ADN tumoral pour être étudié en profondeur, puis ont appliqué plusieurs tests complémentaires aux mêmes échantillons de plasma.
Au-delà des mutations d’un seul gène
Tout d’abord, ils ont séquencé un panel de gènes clés de réparation de l’ADN, incluant des acteurs bien connus tels que BRCA2, BRCA1 et PALB2, ainsi que d’autres gènes qui déterminent l’agressivité des tumeurs prostatiques. BRCA2 est apparu comme le gène de réparation le plus fréquemment altéré et s’est souvent retrouvé associé à la perte d’autres garde-fous importants tels que PTEN et RB1. Mais l’équipe a également examiné des modifications à grande échelle de la structure chromosomique sur l’ensemble du génome, en utilisant un séquençage du génome entier à faible profondeur pour calculer un score d’instabilité génomique. Les tumeurs avec des gènes BRCA endommagés, ou avec des scores élevés, présentaient des génomes fortement réarrangés et étaient liées à une survie globale plus mauvaise, soulignant que les grandes altérations structurelles peuvent être tout aussi informatives que des mutations spécifiques.
Empreintes de l’échec de réparation dans les motifs de mutation
Dans un sous-ensemble de patients, les scientifiques sont allés plus loin en séquençant toutes les régions codantes pour lire le motif détaillé des mutations accumulées au fil du temps. Certaines combinaisons de substitutions de bases et de petites insertions ou délétions agissent comme des empreintes digitales des processus qui les ont générées. Ils ont constaté que des signatures classiques associées à la HRD, telles qu’une appelée SBS3 et un autre motif d’indels connu sous le nom d’ID6, étaient enrichies dans les tumeurs présentant des défauts des gènes de réparation et une instabilité génomique élevée. D’autres signatures indiquaient des problèmes distincts, comme une défaillance du système de réparation des mésappariements ou un sous-type spécifique entraîné par CDK12, montrant que différentes ruptures des mécanismes de réparation laissent des cicatrices reconnaissables dans le génome.
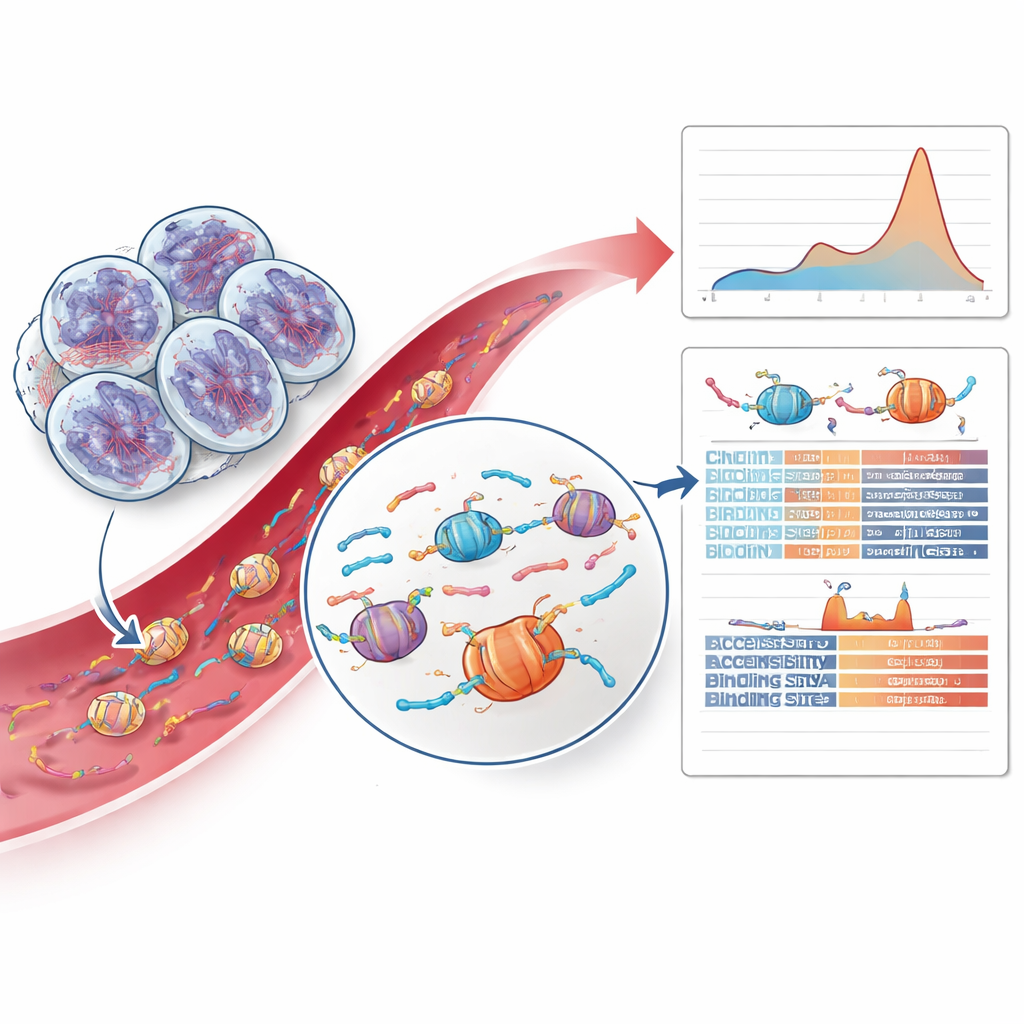
Décoder les motifs de fragments d’ADN et les indices chromatinien
La partie la plus novatrice du travail dépassait entièrement l’analyse des mutations et examinait comment l’ADN tumoral était fragmenté. Lorsque les cellules meurent, leur ADN est découpé autour de structures protéiques appelées nucléosomes, créant des fragments avec des longueurs et des extrémités caractéristiques. L’équipe a découvert que les tumeurs avec HRD montraient un excès relatif de fragments légèrement plus longs correspondant à deux nucléosomes, un décalage non observé dans d’autres cancers de la prostate ou chez des témoins sains. En entraînant un modèle d’apprentissage automatique prudent sur les longueurs de fragments et les caractéristiques des extrémités des fragments, ils ont pu identifier les cas positifs pour la HRD à partir du sang seul avec une précision encourageante. Ils ont également sondé l’accessibilité de différentes régions du génome autour des sites de liaison des facteurs de transcription — des protéines qui contrôlent l’activité des gènes — et ont trouvé que certains sites de liaison de doigts de zinc étaient moins accessibles dans les tumeurs HRD, suggérant des changements plus profonds liés à la réparation dans l’organisation de la chromatine.
Ce que cela pourrait signifier pour les patients
Ensemble, ces couches d’information — depuis des mutations de gènes spécifiques et le réarrangement massif des chromosomes jusqu’à des décalages subtils dans la taille des fragments d’ADN et l’accessibilité de la chromatine — forment une image plus complète de la faiblesse de réparation de l’ADN dans le cancer de la prostate. Pour un non-spécialiste, le message clé est qu’un prélèvement sanguin analysé avec soin peut révéler non seulement si un gène familier comme BRCA2 est muté, mais si une tumeur se comporte comme si elle avait un défaut sérieux de réparation, même lorsque les tests habituels paraissent normaux. Si cette approche multimodale basée sur le sang est validée dans des cohortes plus larges et plus diverses, elle pourrait aider les médecins à identifier de manière plus fiable qui est susceptible de bénéficier d’inhibiteurs de PARP ou de médicaments à base de platine, à surveiller les évolutions au fil du temps et, en définitive, à personnaliser les traitements avec un test simple et répétable.
Citation: Vlachos, G., Moser, T., Lazzeri, I. et al. Functional footprints of homologous recombination deficiency in prostate cancer revealed by ctDNA fragmentation and transcription factor accessibility. Br J Cancer 134, 949–960 (2026). https://doi.org/10.1038/s41416-025-03301-0
Mots-clés: cancer de la prostate, biopsie liquide, réparation de l’ADN, ADN tumoral circulant, inhibiteurs de PARP