Clear Sky Science · fr
Paysages d’un microenvironnement immunosuppresseur dans le cancer gastrique à forte expression de VISTA
Pourquoi les défenses de l’organisme échouent parfois contre le cancer de l’estomac
Les traitements anticancéreux modernes reposent de plus en plus sur la réactivation du système immunitaire pour qu’il attaque les tumeurs. Pourtant, chez de nombreux patients atteints d’un cancer gastrique avancé, ces médicaments puissants fonctionnent mal ou cessent d’être efficaces. Cette étude explore une raison importante : une molécule de frein appelée VISTA qui reconfigure l’environnement local autour de la tumeur, transformant les cellules immunitaires de combattantes en spectatrices voire en auxiliaires du cancer. Comprendre cet interrupteur caché pourrait ouvrir la voie à des immunothérapies plus précises et plus efficaces.
Un frein caché dans le voisinage tumoral
Les auteurs se sont concentrés sur VISTA, une protéine principalement présente sur certains globules blancs au sein et autour des tumeurs. VISTA agit comme un signal d’arrêt pour les réponses immunitaires. Alors que d’autres freins tels que PD-1 et PD-L1 sont déjà ciblés par des médicaments approuvés, le rôle de VISTA dans le cancer gastrique restait flou. Pour l’examiner, l’équipe a analysé des tissus provenant de 172 patients en utilisant un marquage multicolore avancé pour cartographier de nombreux types cellulaires à la fois. Ils ont aussi utilisé le séquençage ARN unicellulaire et la transcriptomique spatiale sur des séries d’échantillons plus petites pour déterminer quelles cellules portent VISTA, ce que font ces cellules et où elles se situent précisément dans le paysage tumoral. 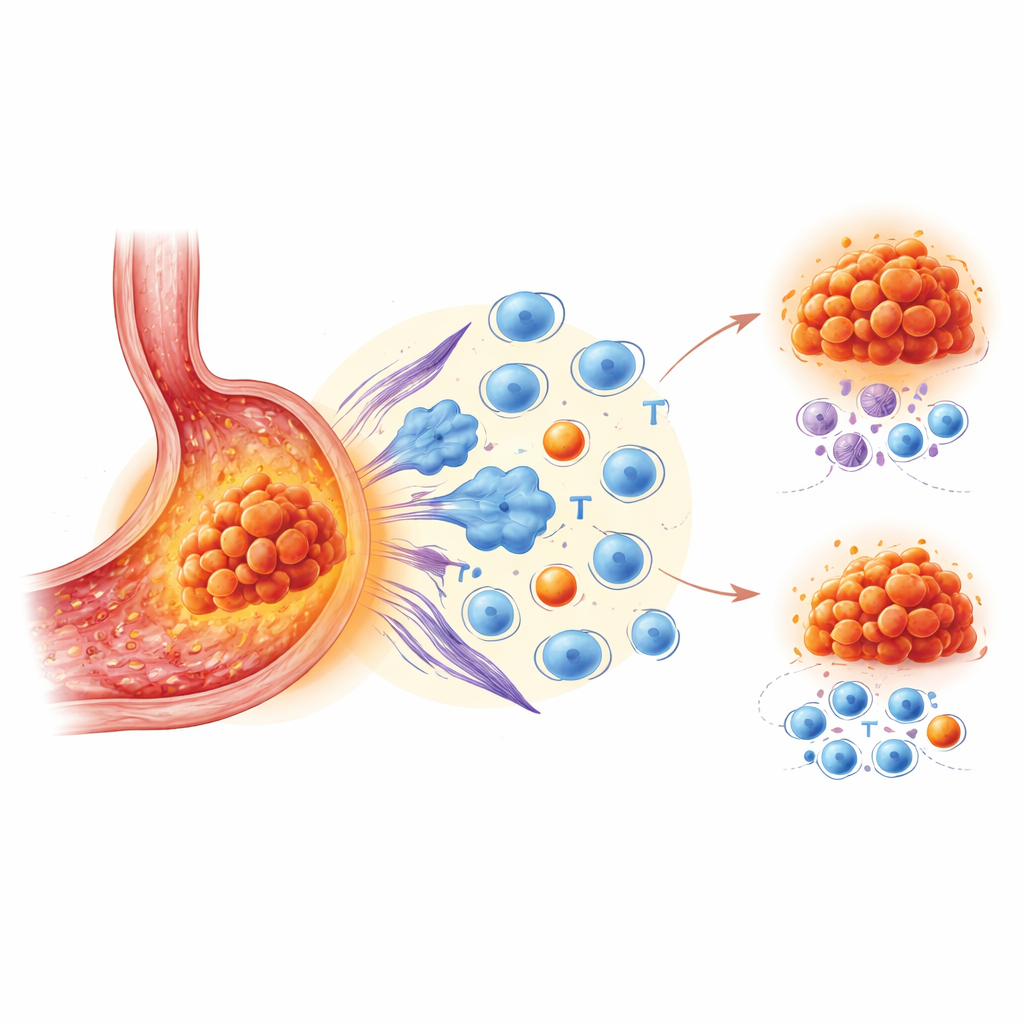
Lorsque VISTA est élevée, le système immunitaire est étouffé
En comparant des tumeurs à niveaux élevés ou faibles de VISTA, les chercheurs ont observé un schéma constant. Les cancers riches en VISTA étaient entourés de cellules immunitaires, mais pas celles qui montent une attaque vigoureuse. On trouvait plutôt une accumulation de lymphocytes T cytotoxiques « épuisés » ayant perdu leur efficacité, de lymphocytes T régulateurs qui atténuent les réponses immunitaires, de cellules de soutien cicatricielles appelées fibroblastes, et de macrophages orientés vers un état favorable à la tumeur. Les patients dont les régions tumorales contenaient davantage de VISTA ont connu des périodes plus courtes avant la progression de la maladie après immunothérapie, même en tenant compte d’autres facteurs cliniques. Autrement dit, un voisinage riche en VISTA semblait actif au microscope mais fonctionnait comme une zone « immuno-silencieuse » ou suppressive.
Les macrophages comme intermédiaires clés
En approfondissant l’analyse, les scientifiques ont examiné les monocytes et les macrophages — des cellules immunitaires qui peuvent soit dévorer le cancer, soit le protéger. Au niveau unicellulaire, le gène codant VISTA (appelé VSIR) était particulièrement actif dans plusieurs sous-groupes de macrophages, en particulier ceux qui présentent efficacement des fragments de protéines tumorales à leur surface et ceux présentant des caractéristiques de macrophages dits M2, ou de réparation tissulaire. En utilisant une chronologie computationnelle du développement cellulaire, l’équipe a observé l’activation de VISTA lorsque les cellules évoluaient de monocytes précoces vers des macrophages plus matures qui se regroupaient autour des cellules tumorales. La cartographie spatiale a confirmé que les macrophages VISTA-positifs avaient tendance à se situer à proximité des cellules cancéreuses, et les patients dont les tumeurs comprenaient davantage de ces cellules à ces emplacements précis ont eu un pronostic pire après un traitement par inhibiteur de point de contrôle immunitaire. 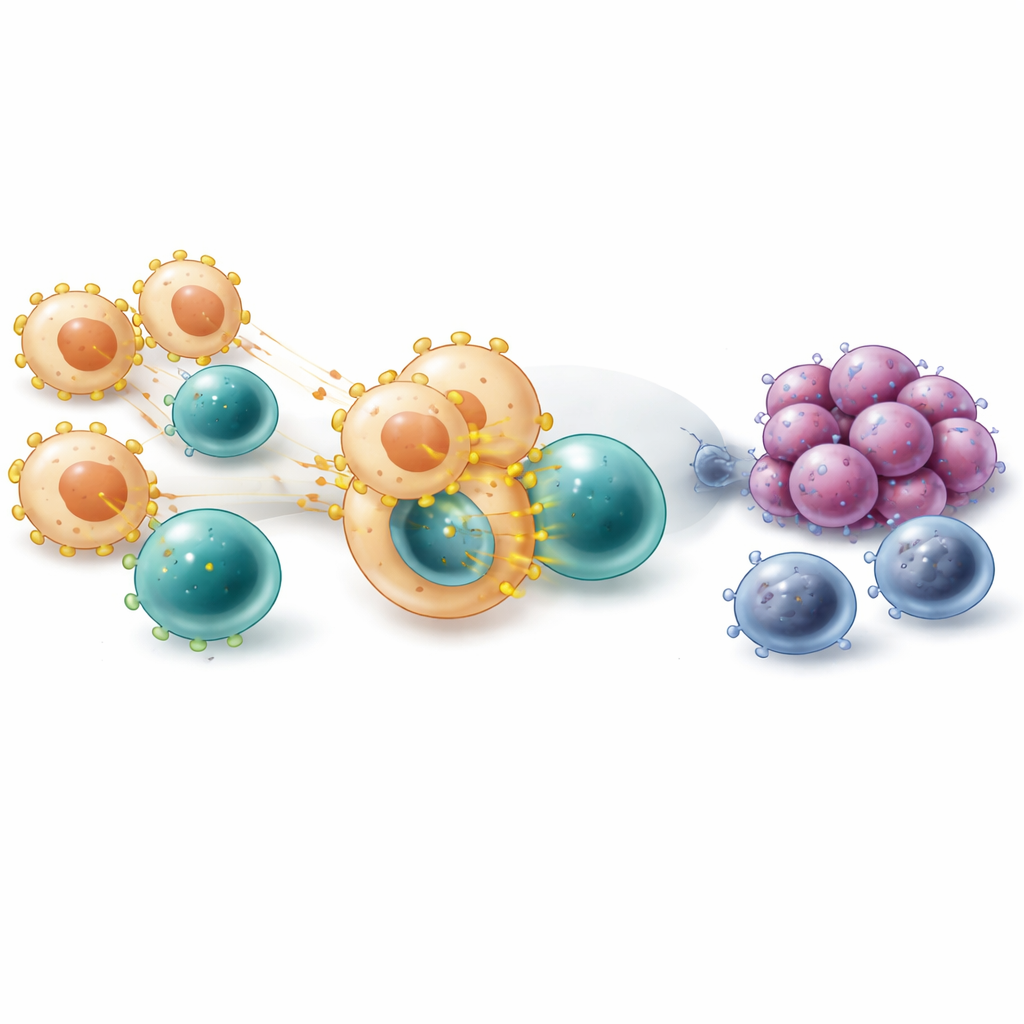
Comment les cellules VISTA-positives épuisent les lymphocytes T
L’étude a également exploré la façon dont les macrophages portant VISTA interagissent avec les lymphocytes T. Des cartes de communication construites à partir de données d’expression génique suggèrent que ces macrophages contactent fréquemment les lymphocytes T via des paires moléculaires telles que LGALS9 et PTPRC, ainsi que par des molécules impliquées dans la présentation de fragments tumoraux aux lymphocytes T. Cette présentation constante peut, avec le temps, pousser les lymphocytes T d’un état précoce et actif vers un état de stimulation chronique et d’épuisement, caractérisé par de multiples signaux inhibiteurs à leur surface. Dans les échantillons où les macrophages exprimaient davantage VSIR, on observait plus de lymphocytes T régulateurs et plus de lymphocytes T cytotoxiques épuisés, renforçant l’idée que les macrophages VISTA-positifs favorisent l’épuisement immunitaire plutôt qu’une attaque nette et efficace.
Ce que cela pourrait signifier pour les traitements futurs
Dans l’ensemble, ce travail présente VISTA comme un interrupteur central qui aide les tumeurs gastriques à construire une niche immunosuppressive, notamment via des macrophages spécialisés qui présentent du matériel tumoral tout en envoyant des signaux inhibiteurs aux lymphocytes T. Pour les patients, cela suggère qu’une forte expression de VISTA est un marqueur de résistance aux traitements actuels ciblant uniquement PD‑1 ou PD‑L1. Bloquer VISTA — éventuellement en association avec les inhibiteurs de points de contrôle existants — pourrait revitaliser les lymphocytes T et rééquilibrer la réponse en faveur du contrôle tumoral. Bien que des études précliniques et cliniques supplémentaires soient nécessaires, cette recherche offre une feuille de route pour concevoir de nouvelles combinaisons thérapeutiques et pour identifier les patients les plus susceptibles de bénéficier de telles approches.
Citation: Luo, Y., Peng, H., Yao, Q. et al. Immunosuppressive immune microenvironment landscapes in VISTA-high gastric cancer. Br J Cancer 134, 1066–1079 (2026). https://doi.org/10.1038/s41416-025-03290-0
Mots-clés: cancer gastrique, microenvironnement tumoral, point de contrôle immunitaire, macrophages, épuisement des lymphocytes T