Clear Sky Science · fr
Spectre et fonctions des canaux ioniques et des transporteurs dans les ostéoclastes
Pourquoi nos os ont besoin de petits gardiens
Notre squelette semble solide et immuable, mais il est constamment détruit et reconstruit. Des cellules spécialisées appelées ostéoclastes jouent le rôle d’équipe de démolition, dissolvant l’os ancien pour permettre la formation d’os neuf. Cet article de synthèse explore une distribution cachée de protéines microscopiques « gardiennes » — canaux ioniques et transporteurs — qui laissent passer des ions chargés et des nutriments à l’intérieur et à l’extérieur des ostéoclastes. En comprenant comment ces petites portes régulent la dégradation osseuse, les chercheurs espèrent concevoir de meilleurs traitements pour l’ostéoporose et d’autres maladies osseuses.
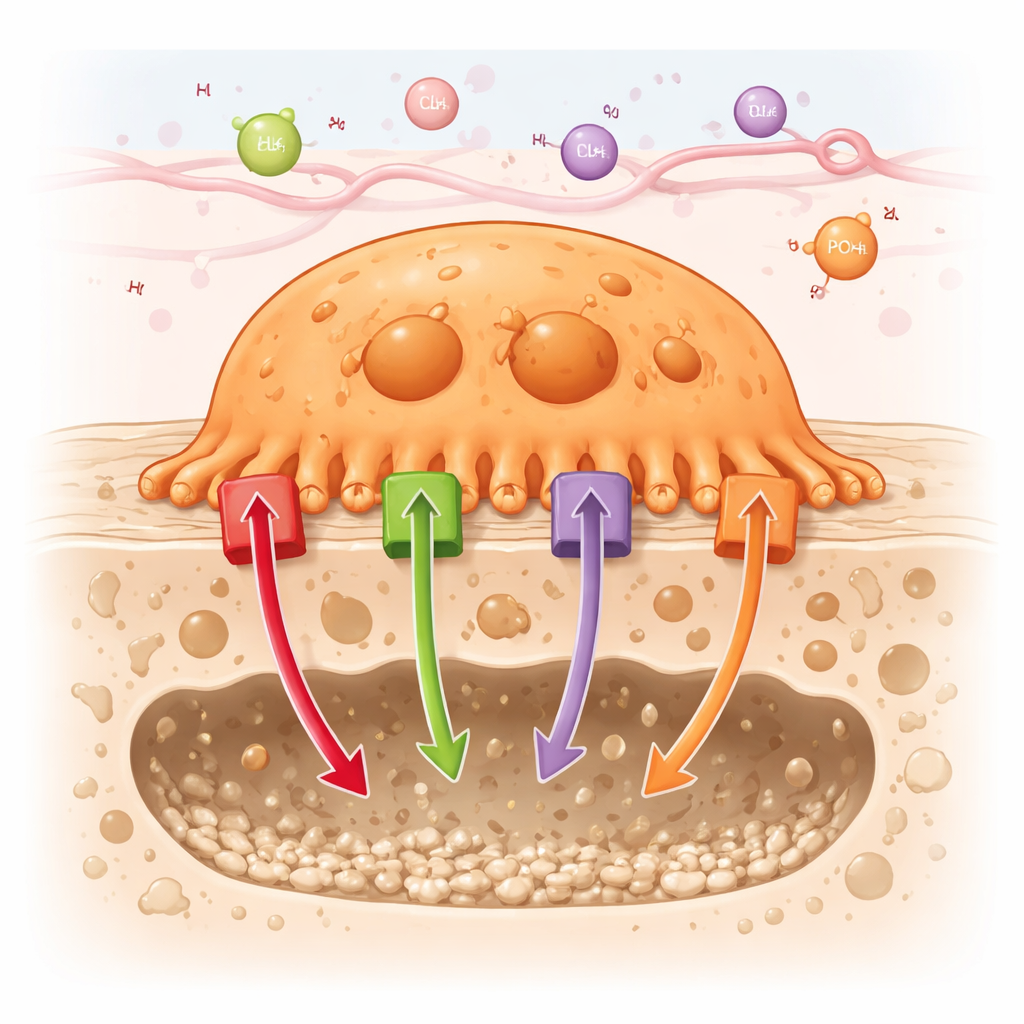
Comment les cellules qui mangent l’os accomplissent leur tâche
Les ostéoclastes agissent en s’attachant fermement à la surface osseuse et en créant une poche scellée où ils peuvent dissoudre les minéraux et digérer les protéines en toute sécurité. Pour rendre cette « chambre de digestion » miniature très acide, les ostéoclastes pompant un grand nombre de protons (ions hydrogène) dans la poche. Simultanément, ils transportent d’autres ions — tels que le chlorure, le calcium et le phosphate — à travers leurs membranes et compartiments internes. L’article passe en revue environ 90 canaux et transporteurs différents trouvés dans les ostéoclastes et les classe en six familles, incluant des pompes entraînées par l’énergie (ATPases), des canaux cationiques et anioniques, des transporteurs couplés, des transporteurs de nutriments et des transporteurs de la famille des protéines à cassette liant l’ATP (ABC).
Acide, sel et énergie : la machinerie centrale
Deux systèmes protéiques se distinguent comme centraux pour la résorption osseuse. D’abord, des pompes à protons vacuolaires connues sous le nom de V‑ATPases poussent activement des protons dans la poche de résorption, la rendant suffisamment acide pour dissoudre le minéral osseux et activer les enzymes protéolytiques. Des sous-unités spécifiques de la V‑ATPase, telles que a3, d2 et plusieurs composants V1, sont enrichies à la bordure en franges de l’ostéoclaste et dans les lysosomes, et des défauts génétiques de ces sous‑unités peuvent soit fragiliser l’os soit provoquer un épaississement osseux anormal. Ensuite, un échangeur chlorure–proton appelé ClC‑7, qui fonctionne en partenariat avec une protéine nommée OSTM1, introduit des ions chlorure dans la même zone. Cela équilibre la charge électrique et permet un pompage continu de protons. Lorsque ClC‑7 est muté, les humains et les souris développent une ostéopétrose, une affection caractérisée par des os trop denses mais fragiles, illustrant à quel point un flux ionique correct est essentiel à la santé squelettique normale.
Calcium, phosphate et autres acteurs de soutien
Au‑delà de la production d’acide, les ostéoclastes dépendent d’une gestion précise du calcium et du phosphate. Un réseau de canaux et de pompes calciques dans la membrane cellulaire, le réticulum endoplasmique, les lysosomes et les mitochondries génère des « oscillations » calciques rythmiques qui activent les gènes clés impliqués dans la formation et la fusion des ostéoclastes. Des transporteurs à la bordure en franges et du côté opposé de la cellule déplacent calcium et phosphate issus de l’os dissous, soit pour les recycler à l’intérieur de la cellule, soit pour les renvoyer dans la circulation sanguine. D’autres métaux et minéraux — tels que le manganèse, le magnésium, le zinc, le cuivre et le fer — sont également contrôlés par des transporteurs spécialisés et influencent l’agressivité de la résorption. Par exemple, le fer et certaines formes de mort cellulaire liées au fer peuvent augmenter ou diminuer l’activité des ostéoclastes, tandis que les transporteurs du zinc tendent à limiter la perte osseuse excessive.
Contrôle du trafic à l’intérieur de la cellule
Les canaux ioniques ne se limitent pas à la membrane externe. Nombre d’entre eux siègent sur des compartiments internes tels que lysosomes, endosomes, l’appareil de Golgi et les mitochondries, créant un réseau de transport en couches. Ces portes internes aident à régler le pH des vésicules digestives, la production d’énergie dans les mitochondries et le mouvement des enzymes et des débris. La revue met en avant la coopération de multiples systèmes de canaux : les échangeurs sodium–hydrogène régulent l’acidité interne, les cotransporteurs potassium–chlorure contribuent au maintien du potentiel de membrane et de l’équilibre en chlorure, et les canaux purinergiques et mécanosensibles traduisent les signaux chimiques ou mécaniques en modifications de la résorption osseuse. Des transporteurs de nutriments pour le glucose, les acides aminés, les nucléosides et la vitamine C soutiennent en outre les fortes demandes énergétiques et biosynthétiques des ostéoclastes en activité.
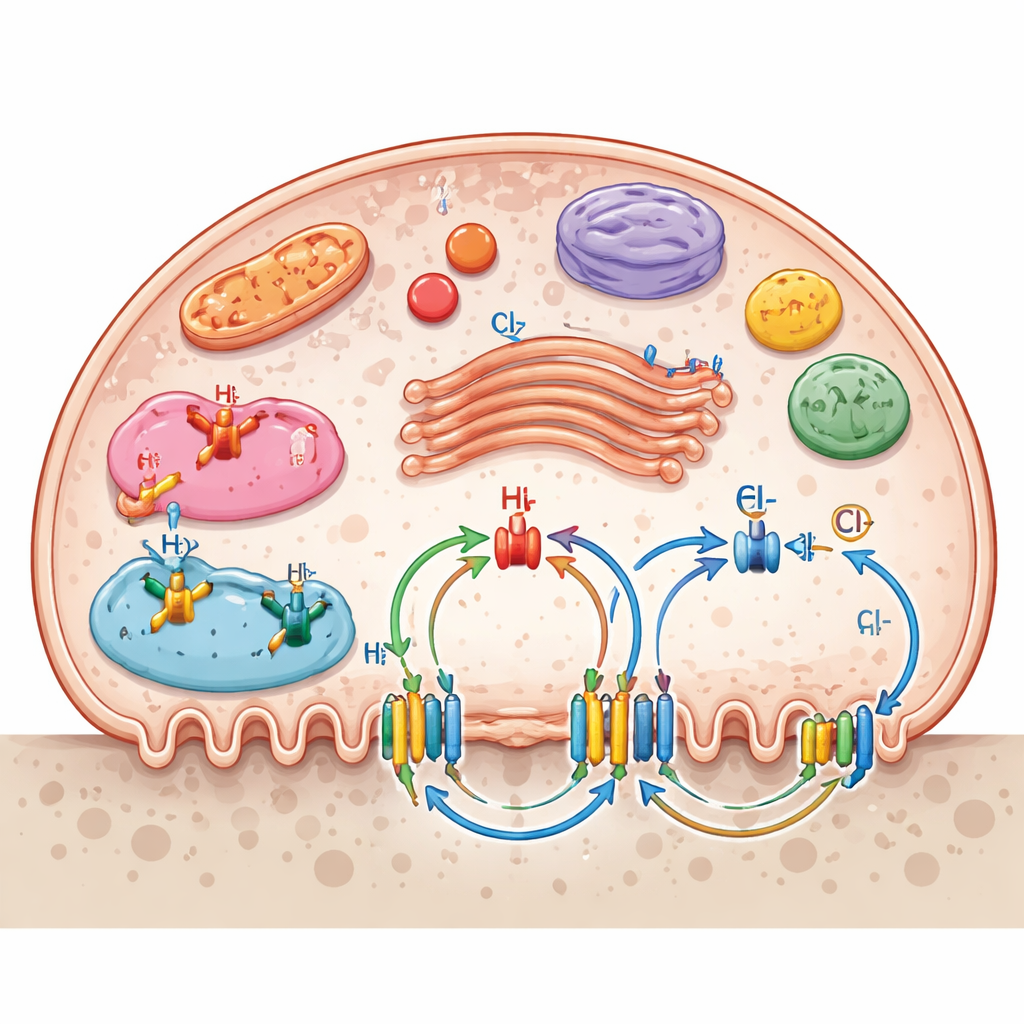
De la biologie fondamentale aux nouveaux traitements
Parce que de nombreux troubles osseux surviennent lorsque les ostéoclastes sont soit hyperactifs soit hypoactifs, les canaux et transporteurs qui dirigent leur comportement constituent des cibles pharmacologiques attrayantes. Les auteurs passent en revue des composés existants et expérimentaux qui bloquent les V‑ATPases, les canaux calciques TRP, les échangeurs de chlorure, les récepteurs purinergiques et d’autres transporteurs, ainsi que des idées plus récentes comme perturber des interactions entre sous‑unités spécifiques ou utiliser des nanoparticules ciblées pour délivrer les médicaments directement à l’os. Ils soulignent que beaucoup de ces protéines se retrouvent aussi dans d’autres tissus, de sorte qu’obtenir une véritable spécificité pour les ostéoclastes reste un défi. Néanmoins, à mesure que les outils génomiques et d’imagerie révèlent mieux où se situent ces canaux et comment ils interagissent, la carte ionique en expansion des ostéoclastes devrait permettre de concevoir des thérapies plus précises pour l’ostéoporose, la perte osseuse inflammatoire et les rares maladies osseuses génétiques.
Citation: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
Mots-clés: ostéoclastes, canaux ioniques, résorption osseuse, V-ATPase, ostéoporose