Clear Sky Science · fr
La PRMT6 est nécessaire pour initier et amplifier l’inflammation induite par les macrophages dans l’ossification hétérotopique en augmentant l’expression de CCL2
Quand la cicatrisation va trop loin
Parfois, après une blessure grave ou une intervention chirurgicale, le corps tente tellement de réparer qu’il crée en réalité du nouvel os là où il ne devrait pas en exister. Cette affection douloureuse, qui correspond à une croissance osseuse indésirable dans les tissus mous, peut bloquer les articulations, compliquer les amputations et rendre les mouvements quotidiens difficiles. Les traitements actuels sont limités et échouent souvent à empêcher la récidive. Cette étude met au jour un interrupteur précoce clé du système immunitaire qui relie le traumatisme à cette formation osseuse anormale — et indique une fenêtre critique, brève, durant laquelle un traitement ciblé pourrait arrêter le processus avant qu’il ne démarre. 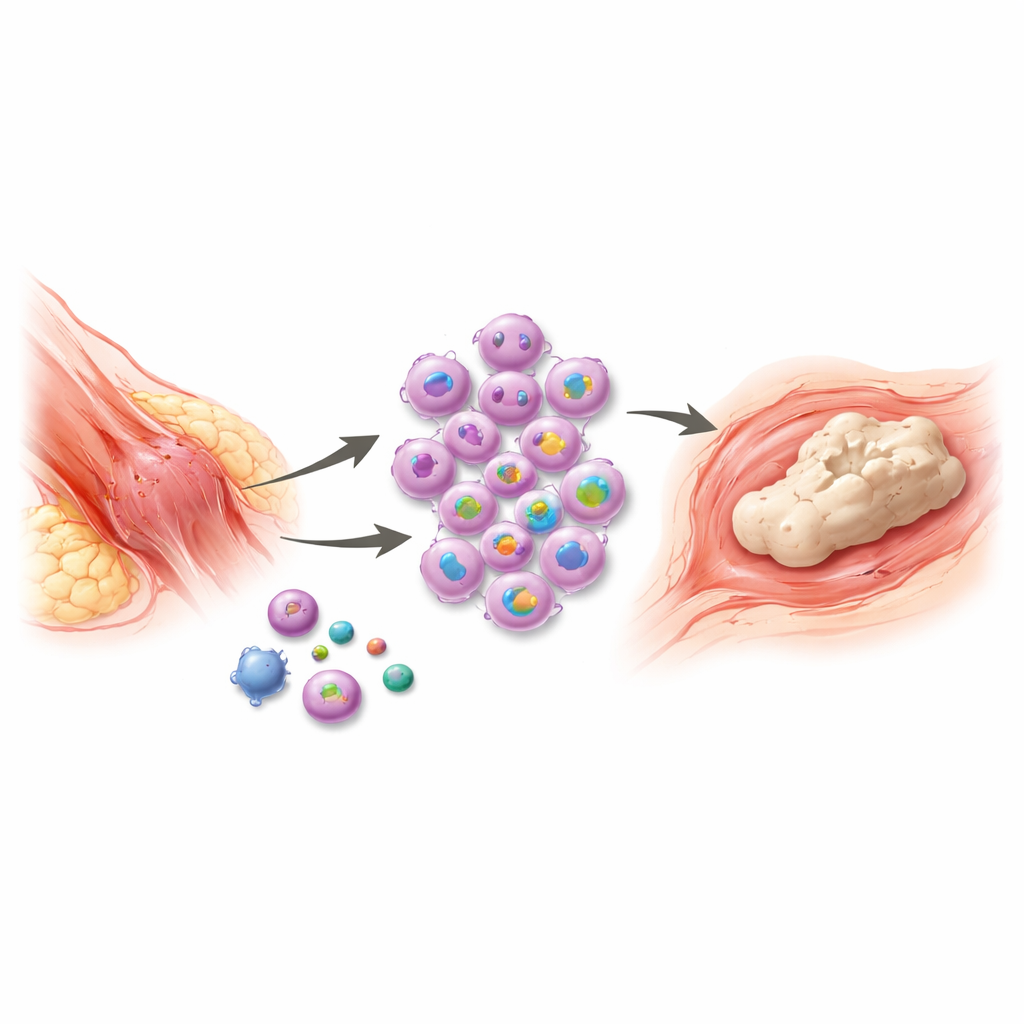
Le problème de l’os au mauvais endroit
Après un traumatisme majeur, comme des brûlures, des fractures ou une chirurgie orthopédique, certains patients développent des îlots d’os à l’intérieur des muscles, des tendons et d’autres tissus mous. Ce nouvel os se forme par un processus similaire au développement osseux normal, débutant par une inflammation et se terminant par un tissu mature et minéralisé. Bien que les cliniciens sachent que des cellules immunitaires appelées macrophages sont centrales dans cette réponse, le contrôle étape par étape de la façon dont elles déclenchent et entretiennent l’inflammation restait flou. Sans cette connaissance, des thérapies comme les anti-inflammatoires, la radiothérapie ou l’ablation chirurgicale tardive traitent principalement les conséquences et non la cause, et la récidive est fréquente.
Le médiateur clé de l’inflammation
À l’aide d’un modèle murin combinant une lésion tendineuse et une brûlure — mimant de près un traumatisme sévère chez l’humain — les chercheurs ont suivi ce qui se passe sur le site de la blessure au fil du temps. Ils ont observé une accumulation rapide de macrophages durant les premiers jours après la lésion, qui a ensuite persisté au fur et à mesure que l’os anormal se formait. Lorsque ces cellules ont été éliminées, l’os surnuméraire a presque disparu, et les tissus environnants présentaient beaucoup moins de perturbations des vaisseaux sanguins et des cellules de soutien. Une analyse génétique approfondie des tissus lésés a mis en évidence une molécule dans ces macrophages qui se détachait du lot : la PRMT6, une enzyme qui modifie les protéines et aide à contrôler l’activation de certains gènes.
Un bouton de volume moléculaire pour l’inflammation
L’équipe a constaté que les niveaux de PRMT6 dans les macrophages augmentaient rapidement après la lésion et en réponse à des signaux de danger et à des composants bactériens en laboratoire. Les souris dépourvues de PRMT6, ou celles chez lesquelles la PRMT6 avait été réduite sélectivement uniquement dans les macrophages, présentaient beaucoup moins de macrophages sur le site de la blessure et développaient nettement moins d’os anormal. Fait important, les tendons lésés chez ces animaux guérissaient en réalité mieux, avec des tissus plus ordonnés et moins de cicatrisation maladroite. Cela indique que la PRMT6 n’est pas nécessaire à la réparation saine, mais qu’elle agit plutôt comme un bouton de volume qui amplifie une inflammation dommageable. Lorsque les chercheurs ont bloqué la PRMT6 avec un médicament, cela n’a été efficace que si l’administration intervenait tôt — durant les premières semaines après la lésion. Commencer le traitement plus tard avait peu d’effet, révélant une fenêtre thérapeutique étroite mais puissante. 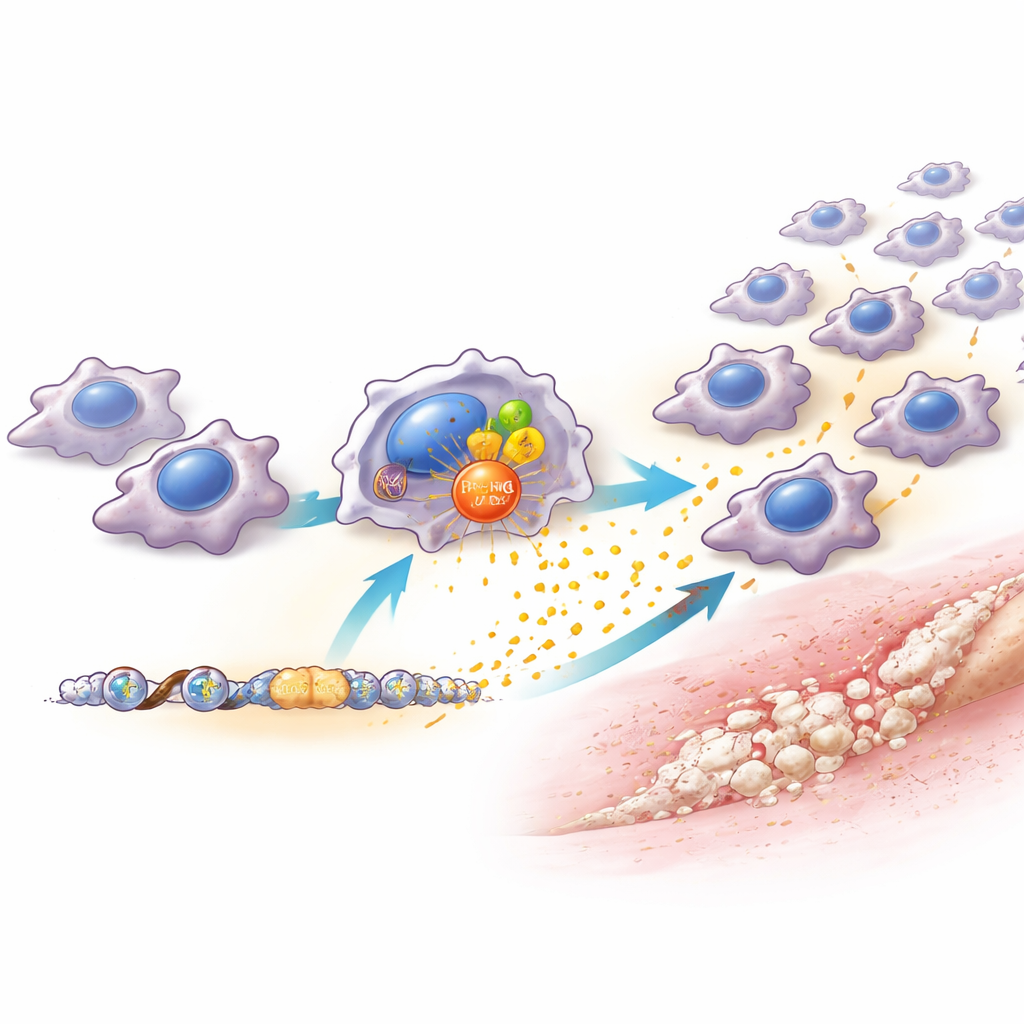
Comment un signal attire de nombreuses cellules immunitaires
Pour comprendre comment la PRMT6 produit cet effet, les scientifiques ont étudié les macrophages en détail. Sans PRMT6, ces cellules produisaient des quantités bien plus faibles de plusieurs attractifs chimiques, en particulier une molécule appelée CCL2, qui attire normalement davantage de monocytes et de macrophages depuis la circulation sanguine vers le tissu lésé. La PRMT6 aide à activer le gène CCL2 de deux manières : elle s’associe au régulateur inflammatoire bien connu NF-κB, et elle marque chimiquement les protéines d’emballage de l’ADN à proximité pour rendre ce gène plus accessible à la lecture. En conséquence, les macrophages riches en PRMT6 sécrètent davantage de CCL2, attirant des macrophages supplémentaires et construisant un « centre inflammatoire » qui nourrit les vaisseaux sanguins et les cellules progénitrices à l’origine de la formation osseuse. Lorsque le CCL2 a été réduit spécifiquement uniquement dans les macrophages, le résultat a fortement rappelé la perte de PRMT6 — moins de macrophages, des niches inflammatoires affaiblies et moins d’os surnuméraire. La réintroduction de CCL2 a partiellement restauré à la fois l’afflux de macrophages et la formation osseuse anormale.
Une opportunité ciblée pour prévenir l’os indésirable
Dans l’ensemble, l’étude montre que la PRMT6 dans les macrophages agit comme un amplificateur épigénétique précoce : elle renforce un signal chimique clé qui recrute davantage de cellules immunitaires, lesquelles conduisent à la formation d’os là où il ne devrait pas y en avoir. Parce que le blocage de la PRMT6 uniquement pendant la phase inflammatoire précoce réduisait fortement l’os indésirable tout en préservant la guérison tendineuse normale — et améliorant même l’organisation tissulaire — cette voie offre une stratégie prometteuse. En théorie, un court traitement bien synchronisé ciblant la PRMT6 après un traumatisme majeur ou une chirurgie pourrait prévenir un handicap à long terme dû à l’os ectopique, sans compromettre la capacité naturelle du corps à se réparer.
Citation: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
Mots-clés: ossification hétérotopique, macrophages, inflammation, régulation épigénétique, signalisation CCL2