Clear Sky Science · fr
C/EBPβ dicte la transcription de FSHβ après la ménopause et le blocage de la voie AEP/C/EBPβ atténue l’ostéoporose
Pourquoi cette recherche compte pour la vie après la ménopause
On explique souvent aux femmes que la chute d’œstrogènes est le principal responsable de la fragilité osseuse après la ménopause. Cette étude apporte un nouvel élément au puzzle : une autre hormone, l’hormone folliculo-stimulante (FSH), et une paire de protéines dans le cerveau et l’os — C/EBPβ et AEP — agissent de concert pour accélérer la perte osseuse. Fait encore plus intrigant, les chercheurs montrent chez la souris que bloquer cette voie avec un comprimé expérimental peut protéger les os aussi efficacement qu’un médicament anti-ostéoporotique approuvé.
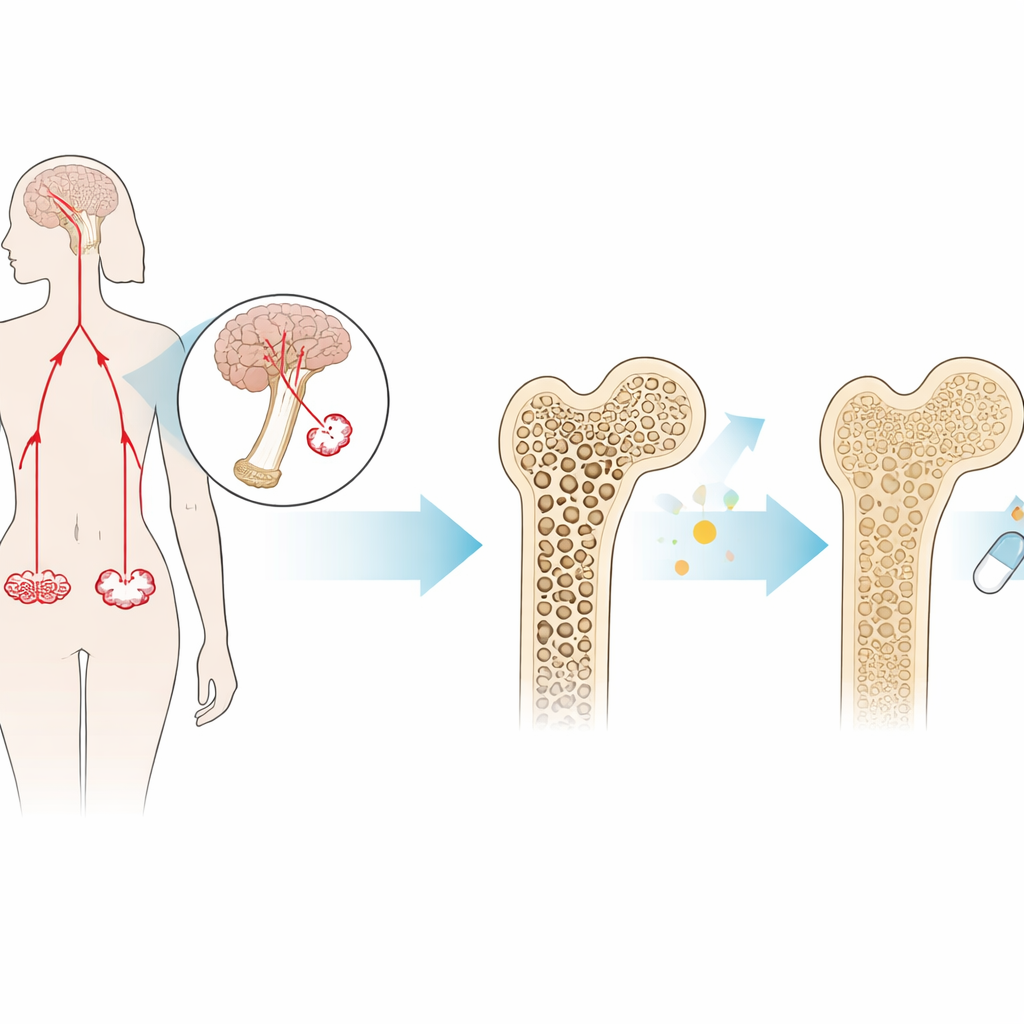
Une hormone méconnue mais d’un grand impact sur l’os
La FSH est produite par l’hypophyse et est surtout connue pour son rôle dans la fertilité. Chez les femmes approchant de la ménopause, son taux augmente fortement plusieurs années avant la dernière période menstruelle. En dehors de sa fonction reproductive, la FSH peut agir directement sur l’os : elle se lie aux récepteurs des cellules qui résorbent l’os (les ostéoclastes), les incitant à ronger l’os plus vite qu’il n’est reconstruit. Des travaux antérieurs ont montré que des souris dépourvues de FSH ou de son récepteur sont protégées de la perte osseuse, même lorsque leurs taux d’œstrogènes sont bas. Cela suggère que la FSH elle-même, et pas seulement la carence en œstrogènes, peut provoquer l’ostéoporose postménopausique.
L’interrupteur de contrôle dans l’hypophyse
La nouvelle étude se concentre sur C/EBPβ, une protéine qui se fixe à l’ADN et active ou réprime des gènes. Les auteurs ont découvert que C/EBPβ se lie directement à la région de contrôle du gène de la sous-unité bêta de la FSH — la partie de l’hormone qui en détermine l’identité — et en augmente la production dans l’hypophyse. Dans des cellules hypophysaires en culture, augmenter l’expression de C/EBPβ a fait monter la FSH, tandis que la réduire l’a diminuée, surtout lorsque les cellules étaient stimulées par le signal reproducteur du cerveau, la GnRH. Chez des souris ovariectomisées, qui reproduisent la ménopause en retirant les ovaires producteurs d’œstrogènes, les animaux avec une expression réduite de C/EBPβ produisaient beaucoup moins de FSH dans leur hypophyse et dans le sang. Ces expériences révèlent C/EBPβ comme un interrupteur clé qui détermine l’ampleur de la hausse de FSH après la chute des œstrogènes.
Une boucle autorenforçante et une nouvelle cible médicamenteuse
C/EBPβ contrôle aussi une autre protéine appelée AEP, une enzyme cliveuse capable d’activer ou d’inactiver d’autres molécules. Dans le cerveau, une chaîne C/EBPβ–AEP a été associée à des lésions de type Alzheimer. Ici, l’équipe s’est demandé si cette même chaîne rétroagissait sur la FSH et l’os. Chez des souris dépourvues d’AEP, les taux de C/EBPβ et de FSH ont diminué dans l’hypophyse, et la perte osseuse après ablation des ovaires a été réduite. Bloquer AEP avec une petite molécule, nommée #11a, a produit un effet similaire : après plusieurs mois de traitement, les souris ovariectomisées présentaient une FSH plus basse, des os plus solides aux analyses haute résolution et moins de cellules ostéoclastiques hyperactives. Une autre classe de composés — des activateurs de TrkB qui diminuent indirectement l’activité d’AEP — a aidé les cellules osseuses en culture mais n’a pas pu abaisser la FSH chez l’animal, principalement parce que leur récepteur cible est rare dans l’hypophyse. Ce contraste renforce la conclusion que l’inhibition directe d’AEP est une manière plus puissante d’éteindre l’axe C/EBPβ–FSH à sa source.
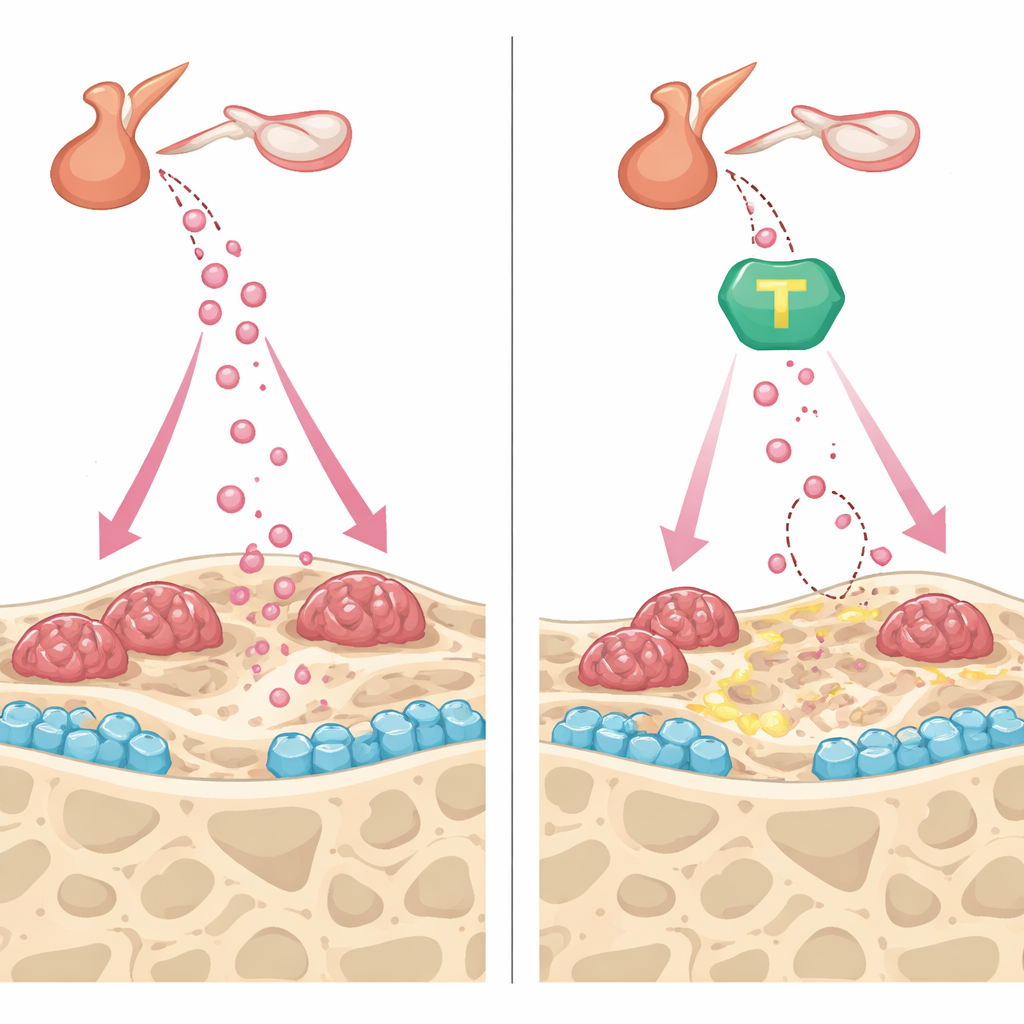
Protéger l’os sur les deux fronts
Au-delà de l’abaissement de la FSH, #11a et l’activateur de TrkB CF3CN ont montré des bénéfices complémentaires à l’intérieur même de l’os. Dans des cultures de cellules formant l’os, les deux composés ont accéléré la maturation et le dépôt minéral, en partie en préservant la fibronectine, une protéine structurelle que l’AEP clive normalement, et en augmentant des signaux pro-ossification tels que l’ostéoprotégérine. Dans les cellules résorbant l’os, les médicaments ont atténué les effets d’un signal clé de résorption, réduisant le nombre de grandes cellules multinucléées et leur capacité à creuser des lacunes dans des coupes d’os. In vivo, chez la souris, #11a et CF3CN ont tous deux freiné le renouvellement osseux rapide déclenché par l’ablation des ovaires, stabilisant la densité osseuse et la microarchitecture. Fait remarquable, lorsque #11a a été comparé directement au tériparatide, un traitement injectable approuvé par la FDA qui favorise la formation osseuse, la pilule expérimentale a égalé la capacité du tériparatide à restaurer le volume et la résistance osseuse dans ce modèle.
Ce que cela pourrait signifier pour la prise en charge future de l’ostéoporose
Pour un non-spécialiste, la conclusion est que ce travail identifie une voie à double effet qui relie l’inflammation associée à la ménopause à l’augmentation de la FSH et aux lésions osseuses, et montre que cibler AEP peut interrompre cette chaîne. Chez la souris, un inhibiteur oral d’AEP non seulement réduit l’excès de FSH qui alimente la perte osseuse, mais modifie aussi directement l’équilibre à l’intérieur de l’os en faveur de la construction plutôt que de la dégradation. Bien que ces résultats doivent encore être vérifiés chez l’humain, ils suggèrent que les traitements futurs de l’ostéoporose pourraient aller au-delà du simple remplacement d’œstrogènes ou de la stimulation de la formation osseuse, et viser plutôt à calmer ce circuit hormonal et enzymatique récemment cartographié qui conduit à la fragilité osseuse postménopausique.
Citation: Xie, Z., Liao, J., Xiong, J. et al. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res 14, 31 (2026). https://doi.org/10.1038/s41413-026-00510-y
Mots-clés: ostéoporose postménopausique, hormone folliculo-stimulante, voie C/EBPβ AEP, remodelage osseux, thérapie ciblée hormonale