Clear Sky Science · fr
La formation de cicatrices fibreuses induite par le TGF-β limite la récupération après lésion de la moelle épinière
Pourquoi les cicatrices dans la moelle épinière comptent
Lorsqu’une lésion grave de la moelle épinière survient, de nombreuses personnes gardent une paralysie permanente ou une perte de sensation parce que les fibres nerveuses endommagées ne repoussent pas. Cette étude pose une question simple mais cruciale : qu’est‑ce qui bloque exactement cette repousse — et peut‑on éliminer cette barrière en toute sécurité ? En révélant comment un type particulier de cicatrice se forme à l’intérieur de la lésion, les auteurs indiquent une nouvelle voie pour aider le système nerveux à se réparer.
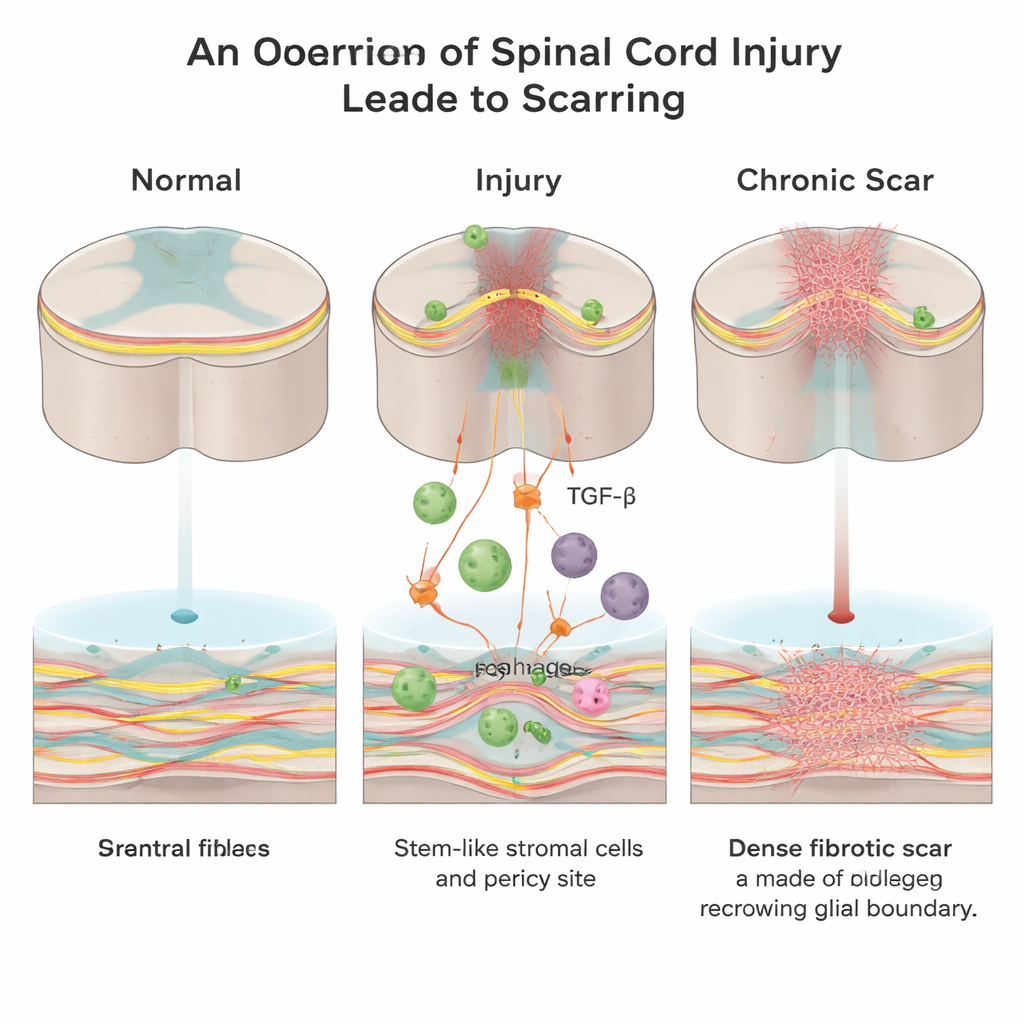
Un mur caché à l’intérieur de la lésion
Après une lésion de la moelle épinière, l’organisme s’efforce de colmater la blessure. Deux principaux types de tissu cicatriciel se forment : une cicatrice « gliale » produite par des cellules de soutien appelées astrocytes, et une cicatrice « fibreuse » riche en collagène, fibronectine et cellules fibroblastiques. Si la cicatrice gliale peut jouer des rôles protecteurs, la cicatrice fibreuse crée une barrière physique et chimique dense que les fibres nerveuses en croissance ne peuvent pas facilement franchir. Jusqu’à présent, les scientifiques savaient beaucoup moins de choses sur la manière dont ce noyau fibreux apparaît et quels signaux en pilotent la formation.
Le rôle des cellules immunitaires et d’un signal puissant
Travaillant chez la souris adulte, les chercheurs se sont focalisés sur une molécule de signalisation appelée facteur de croissance transformant bêta (TGF‑β), qui aide à coordonner la réparation des blessures dans tout l’organisme et est souvent hyperactive dans les maladies fibreuses. Ils ont découvert qu’après une lésion de la moelle épinière, les cellules immunitaires envahissantes connues sous le nom de macrophages deviennent une source majeure de TGF‑β1 actif au site de la lésion. Cette poussée de TGF‑β1 recrute des cellules stromales/mères mésenchymateuses locales et des cellules associées aux vaisseaux appelées péricytes et les pousse à se transformer en fibroblastes — les mêmes cellules qui déposent la cicatrice riche en collagène.
Atténuer le signal pour ouvrir un passage
Pour tester si cette voie cause réellement une cicatrisation nuisible, l’équipe a utilisé plusieurs manipulations génétiques chez la souris. Lorsqu’ils ont supprimé les macrophages, ou éliminé le gène du TGF‑β1 uniquement dans les cellules de la lignée macrophagique, la quantité de tissu fibreux dans la moelle lésée a fortement diminué, et davantage de fibres nerveuses et de voies contenant de la sérotonine ont pu traverser la zone lésée. De même, supprimer le récepteur du TGF‑β spécifiquement dans les péricytes a réduit leur réponse au TGF‑β, entraîné moins d’accumulation de collagène et amélioré la locomotion et la sensibilité lors des tests comportementaux. Il est important de noter que les péricytes et les cellules apparentées de type souche subsistaient, mais étaient moins susceptibles de devenir des fibroblastes formant la cicatrice.
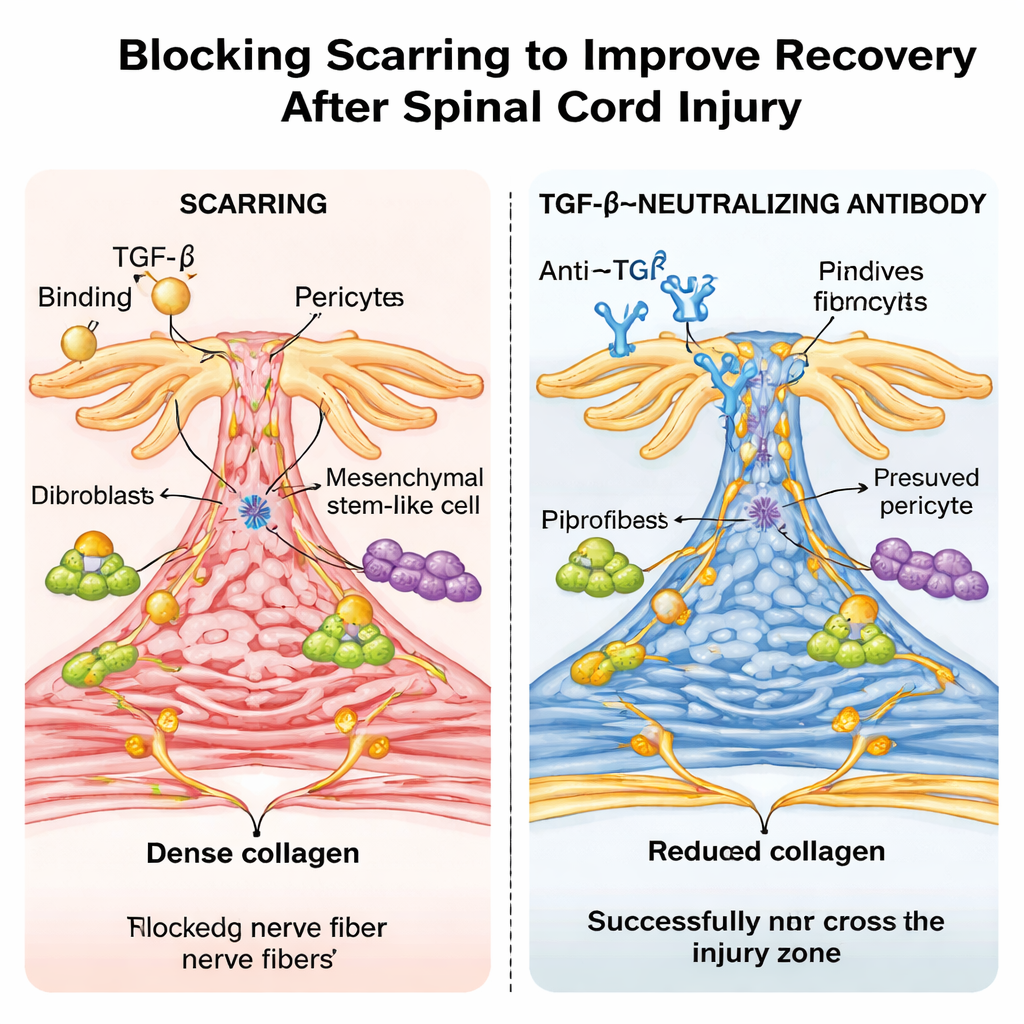
Un anticorps de type médicament et un effet d’âge surprenant
Les chercheurs ont ensuite tenté une approche plus pertinente cliniquement : traiter des souris normales avec un anticorps de laboratoire neutralisant le TGF‑β. Des doses répétées après la lésion ont réduit les niveaux de TGF‑β actif dans le sang et la moelle épinière, réduit la taille de la cicatrice fibreuse et permis aux fibres nerveuses de franchir la lésion plus efficacement, avec des gains marqués en marche et en fonction sensorielle. Le séquençage d’ARN à cellule unique a confirmé que les gènes répondant au TGF‑β étaient fortement actifs dans les types cellulaires formant la cicatrice chez les souris non traitées et étaient atténués par l’anticorps. Fait frappant, lorsque le même type d’écrasement de la moelle épinière a été réalisé chez des souriceaux nouveau‑nés, les animaux ont guéri presque sans formation de cicatrice fibreuse, n’ont montré aucune activation détectable du TGF‑β au site de la lésion et ont retrouvé une motricité quasi normale — rappelant la réparation sans cicatrice observée chez certains animaux non mammifères.
Ce que cela pourrait signifier pour les traitements futurs
Pris ensemble, ces résultats suggèrent qu’une activation excessive du TGF‑β après une lésion de la moelle épinière détourne des cellules de réparation utiles pour ériger un mur fibreux rigide qui bloque la repousse nerveuse et la récupération fonctionnelle. En empêchant cette suractivation — soit en ciblant la production de TGF‑β dans les macrophages, en bloquant son récepteur sur les péricytes et les cellules stromales, ou en utilisant un anticorps neutralisant — il pourrait être possible de réduire la cicatrice néfaste tout en préservant ou en favorisant des réponses tissulaires plus bénéfiques. Bien que la traduction de ces stratégies à l’homme nécessitera des études rigoureuses pour éviter des effets indésirables, ce travail met en lumière la cicatrisation fibreuse induite par le TGF‑β comme une barrière centrale, et potentiellement pharmacologique, à la réparation de la moelle épinière.
Citation: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
Mots-clés: lésion de la moelle épinière, cicatrice fibreuse, TGF-bêta, macrophages, régénération nerveuse