Clear Sky Science · fr
HIF-1α et BMAL1 dans la régénération osseuse : dialogue entre la réponse à l’hypoxie et le rythme circadien
Pourquoi les os cassés guérissent mieux qu’on ne le pense
Lorsque nous nous fracturons un os ou que l’on nous arrache une dent, notre organisme lance discrètement un projet de réparation remarquablement bien coordonné. Au cœur de la zone blessée, le niveau d’oxygène chute et notre horloge interne jour‑nuit continue de battre. Cet article explore comment deux commutateurs maîtres — HIF‑1α, qui détecte le faible taux d’oxygène, et BMAL1, une protéine centrale de l’horloge — coopèrent pour guider les cellules osseuses à travers l’inflammation, la formation de nouveau tissu et la restauration finale de la résistance. Mieux comprendre ce partenariat pourrait améliorer les traitements des fractures, de l’ostéoporose, de l’arthrite et même des implants dentaires.
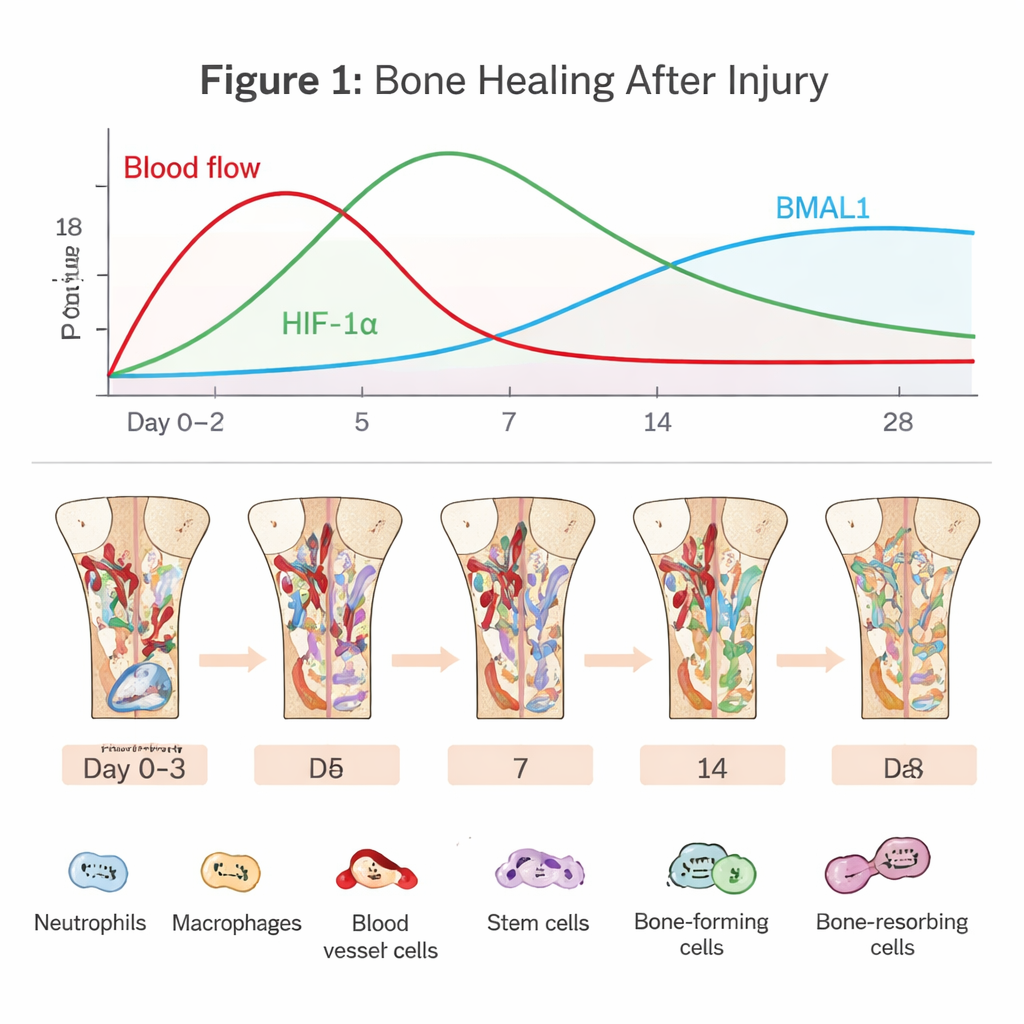
Le drame caché à l’intérieur d’un os en réparation
La régénération osseuse commence au moment où les vaisseaux sanguins se déchirent. Un caillot se forme, privant la zone d’une grande partie de son oxygène et créant une poche sévèrement hypoxique. Des cellules immunitaires comme les neutrophiles et les macrophages affluent pour nettoyer les débris et combattre les microbes. Simultanément, des cellules souches de la moelle osseuse et des cellules vasculaires sont recrutées pour reconstruire la zone. Cette phase initiale « inflammatoire » est à double tranchant : une poussée brève et bien synchronisée d’inflammation déclenche la réparation, mais si elle dure trop longtemps ou est trop intense, la guérison peut stagner ou échouer. L’article souligne que négocier ce chemin étroit dépend largement de la façon dont les cellules perçoivent l’oxygène et le temps.
Comment les cellules tirent parti du faible apport en oxygène
Dans la zone fracturaire pauvre en oxygène, la protéine HIF‑1α se stabilise et active des gènes qui aident les cellules à s’adapter. Elle incite les cellules endothéliales à faire germer de nouveaux vaisseaux sanguins, permettant à l’oxygène et aux nutriments de rejoindre la lésion. Elle reprogramme aussi le métabolisme cellulaire vers la glycolyse, un mode de production d’énergie qui fonctionne même en l’absence d’oxygène. Pour les cellules souches et les ostéoblastes formant l’os, une activation modérée de HIF‑1α peut stimuler la prolifération, la migration et la formation osseuse, en partie en augmentant des facteurs comme le VEGF qui relient la néovascularisation à la formation osseuse. Mais si l’hypoxie est trop sévère ou prolongée, des molécules de stress et des espèces réactives de l’oxygène s’accumulent, poussant les ostéoblastes vers la mort et stimulant les ostéoclastes résorbant l’os. Le même signal hypoxique peut donc soit soutenir, soit compromettre la guérison, selon son intensité et sa durée.
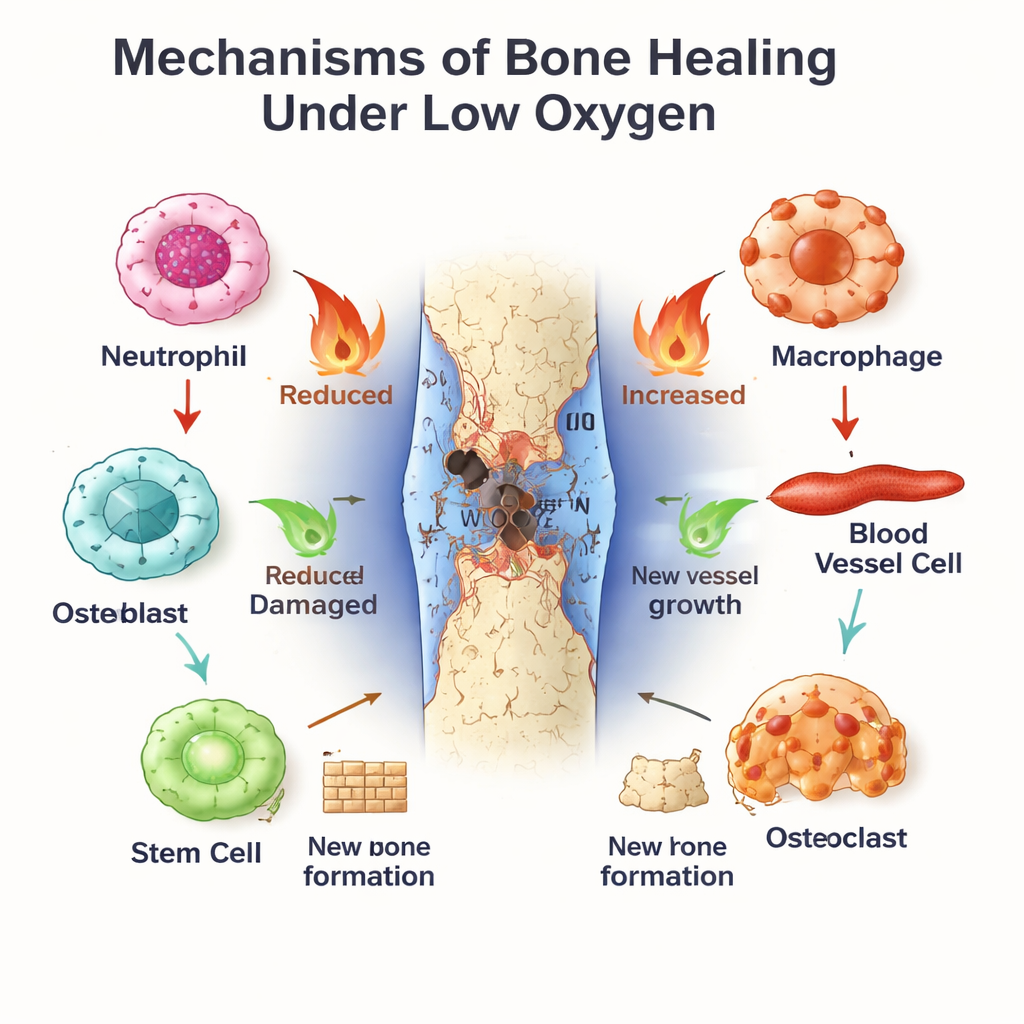
L’horloge interne comme chef d’orchestre de la réparation osseuse
En parallèle fonctionne l’horloge circadienne, un chronométreur moléculaire présent dans presque toutes les cellules. BMAL1, l’un de ses composants centraux, contribue à établir les rythmes quotidiens de l’activité immunitaire, du comportement vasculaire et de la différenciation des cellules souches. Les neutrophiles et les macrophages montrent des différences selon l’heure du jour dans l’intensité de leur réponse à la blessure et dans la rapidité avec laquelle ils vieillissent ou passent d’un état inflammatoire (de type M1) à un état de réparation (de type M2). Dans les cellules vasculaires et les cellules souches médullaires, BMAL1 favorise une prolifération saine et une formation osseuse ordonnée, en partie en modulant des voies de croissance comme Wnt et TGF‑β/SMAD. Quand BMAL1 est perturbé — par des défauts génétiques, le travail posté ou des maladies métaboliques — les os ont tendance à perdre de la masse, les cellules souches s’épuisent et l’équilibre entre formation et résorption osseuse bascule vers la perte.
Un dialogue entre la détection de l’oxygène et l’horloge biologique
Le cœur de la revue est l’émergence d’un « dialogue » entre HIF‑1α et BMAL1. Ces deux protéines présentent des structures similaires et peuvent interagir physiquement, formant même des paires mixtes qui se fixent à l’ADN et contrôlent des ensembles de gènes qui se chevauchent. Chacune peut influencer la production et la stabilité de l’autre, créant des boucles de rétroaction qui relient le rythme jour‑nuit à la façon dont les cellules répondent à l’hypoxie. Ensemble, elles régulent aussi l’équilibre redox cellulaire — la production d’espèces réactives de l’oxygène par rapport à la capacité antioxydante disponible — et co‑contrôlent des enzymes clés qui déterminent si les cellules s’appuient davantage sur la respiration dépendante de l’oxygène ou sur la glycolyse indépendante d’oxygène. Ce contrôle conjoint contribue à déterminer si l’environnement de la fracture favorise une reconstruction constructive ou une inflammation excessive et une résorption osseuse.
Implications pour la maladie et le traitement
Le partenariat HIF‑1α–BMAL1 se retrouve dans de nombreuses affections osseuses. Chez les travailleurs postés, le sommeil perturbé et l’exposition à la lumière altèrent probablement BMAL1, augmentent le stress oxydatif et gênent la réparation guidée par HIF‑1α, contribuant à l’ostéoporose. Dans le diabète, l’hyperglycémie affaiblit à la fois la fonction de l’horloge et la signalisation hypoxique, compromettant la néovascularisation et la formation osseuse pilotée par les cellules souches. Dans l’arthrose, la perte de BMAL1 dans les cellules cartilagineuses perturbe leur rythme et leur relation protectrice avec HIF‑1α, accélérant la dégradation du cartilage. Autour des implants en titane, une hypoxie contrôlée et un rythme circadien sain semblent favoriser une meilleure ostéointégration, suggérant que des revêtements d’implants futurs pourraient être conçus pour activer en douceur à la fois HIF‑1α et BMAL1. Globalement, l’article conclut que la réussite de la régénération osseuse dépend non seulement des cellules présentes, mais aussi de la manière dont elles lisent l’oxygène et le temps — et que cibler ce dialogue pourrait ouvrir de nouvelles voies vers une guérison plus rapide et plus solide.
Citation: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
Mots-clés: régénération osseuse, rythme circadien, hypoxie, ostéoporose, cicatrisation des fractures