Clear Sky Science · fr
Biomatériaux intelligents pour la réparation et la régénération du squelette lié au vieillissement
Des os plus solides dans un monde qui vieillit
Beaucoup considèrent l’affaiblissement des os et les douleurs articulaires comme des conséquences inévitables du vieillissement. Pourtant, des scientifiques conçoivent aujourd’hui des matériaux « intelligents » capables de détecter quand et où l’os faiblit, puis d’aider à sa réparation. Ces matériaux visent à consolider les fractures de façon plus fiable, ralentir ou inverser l’ostéoporose et l’arthrose, et réduire la nécessité de chirurgies répétées — offrant aux personnes âgées une meilleure chance de rester actives et autonomes.
Comment les os vieillissent et pourquoi ils se cassent plus facilement
L’os est un tissu vivant qui se reconstruit en permanence, mais cet équilibre se dérègle avec l’âge. Les cellules souches de la moelle osseuse se détournent de la production d’ostéoblastes (cellules formatrices d’os) au profit d’adipocytes ; les cellules qui forment l’os s’épuisent tandis que les ostéoclastes (cellules résorbantes) deviennent suractives. La matrice de collagène et de minéraux devient plus sèche et plus fragile, et l’architecture microscopique se raréfie. Les changements hormonaux, une inflammation chronique de bas grade, un excès d’espèces réactives de l’oxygène et un environnement local acide ajoutent du stress. En surface, cela se traduit par des os plus fins et plus poreux, des articulations raides, des déformations de la colonne vertébrale et un risque accru de fractures et de pathologies comme l’ostéoporose et l’arthrose.
Pourquoi les traitements actuels ne suffisent pas
Les traitements principaux d’aujourd’hui comprennent des médicaments qui ralentissent la perte osseuse ou stimulent la formation osseuse, ainsi que des interventions chirurgicales et des implants métalliques ou céramiques pour stabiliser les fractures ou remplacer les articulations endommagées. Ces approches ont sauvé de nombreuses vies mais présentent des limites importantes. Les médicaments systémiques atteignent souvent une fraction infime du tissu osseux et peuvent provoquer des effets indésirables tels que des problèmes mandibulaires, des caillots sanguins, voire un risque accru de cancer en cas d’utilisation prolongée. Les thérapies par cellules souches sont prometteuses chez l’animal mais posent des problèmes de survie cellulaire, de comportement imprévisible et de risque tumoral potentiel. Les implants conventionnels apportent de la solidité mais sont des objets « idiots » : ils ne détectent pas leur environnement, ne régulent pas la libération de médicaments et peuvent échouer dans un os fragile et âgé.
Transporteurs de médicaments intelligents qui patrouillent dans l’organisme
Les biomatériaux intelligents apportent de l’intelligence à cette problématique. Une stratégie majeure consiste en un « acheminement intelligent » systémique des médicaments via des nanoparticules ou des gels mous qui circulent dans le sang et ne s’activent qu’aux endroits problématiques. Ces vecteurs peuvent être conçus pour répondre à des signaux internes tels que l’acidité, des niveaux élevés d’espèces réactives de l’oxygène ou des enzymes destructrices de l’os ; ou à des stimuli externes comme la lumière, les ultrasons, la chaleur ou les champs magnétiques. Par exemple, certaines particules restent intactes dans les tissus sains mais s’ouvrent et libèrent leur cargaison médicamenteuse dans les zones acides et riches en enzymes où les cellules résorbantes sont suractives. D’autres captent l’excès d’oxydants tout en libérant lentement un anti-inflammatoire, ou transportent des colorants d’imagerie pour que les médecins puissent suivre leur trajet en temps réel. En combinant plusieurs déclencheurs — pH et oxydants, par exemple — les chercheurs affinent le ciblage et réduisent les effets secondaires.
Échafaudages locaux qui agissent comme des os intelligents temporaires
Lorsque les os vieillissants présentent de larges défauts ou des fractures complexes, des « échafaudages intelligents » locaux peuvent être implantés directement dans le vide. Ces structures 3D, fabriquées en métaux, céramiques, polymères ou en combinaisons, sont conçues pour correspondre à la résistance, à la porosité et à la flexibilité de l’os. Leur architecture spongieuse permet la croissance des vaisseaux sanguins et du nouvel os, tandis que le matériau se dissout progressivement et est remplacé par le tissu du patient. 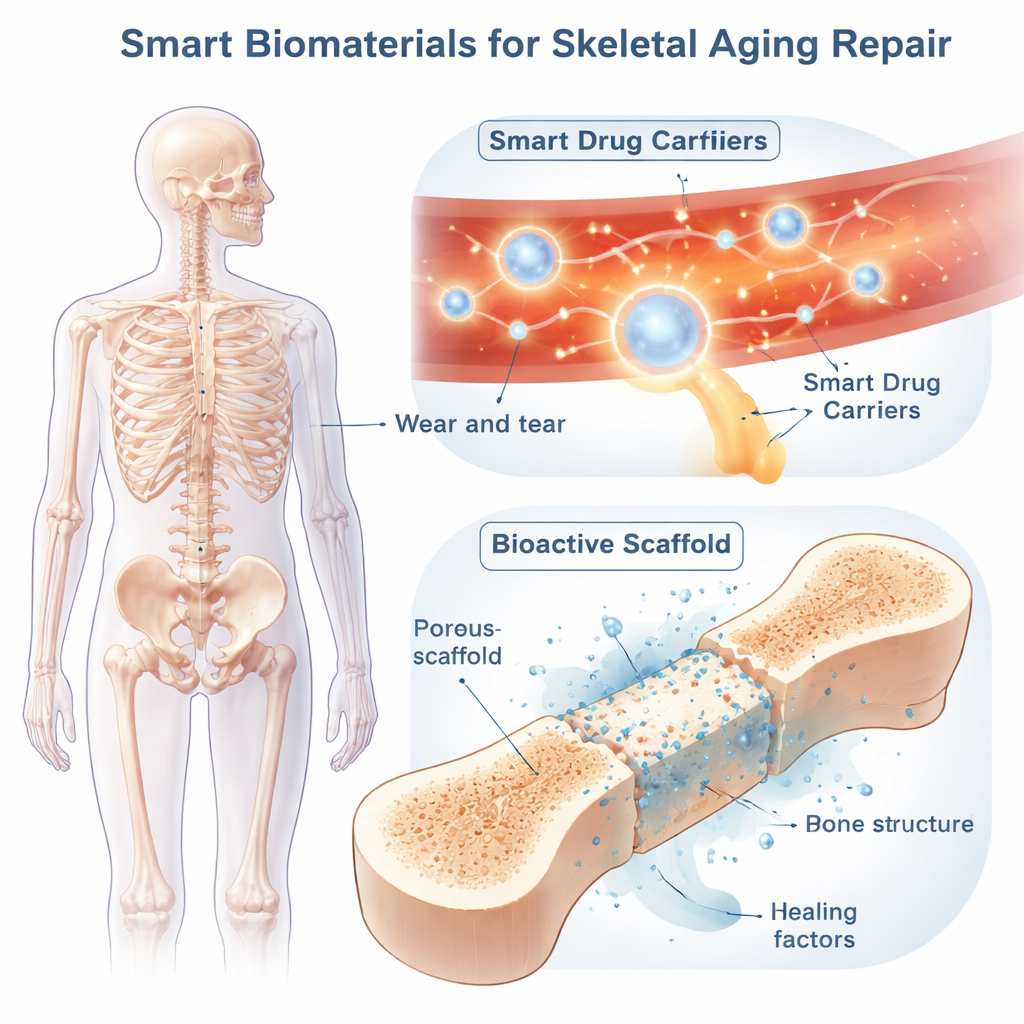
Du laboratoire à la clinique : outils, obstacles et axes futurs
Pour réaliser ces systèmes complexes, les scientifiques utilisent des techniques de fabrication avancées comme l’impression 3D et la fabrication additive pour ajuster précisément la taille des pores, la rigidité et la charge en médicament. Pourtant, transformer les biomatériaux intelligents en traitements de routine reste difficile. La plupart des particules injectées s’accumulent encore dans des organes tels que le foie et la rate plutôt que dans l’os, et de nombreux modèles animaux ne reproduisent pas la complexité du vieillissement humain. La production à grande échelle, le contrôle qualité, l’autorisation réglementaire et le coût demeurent des obstacles majeurs. Les chercheurs voient un espoir dans la combinaison de matériaux intelligents avec l’intelligence artificielle pour personnaliser la conception des échafaudages et le dosage des médicaments, ainsi que dans l’ajout de capteurs intégrés capables de suivre la guérison et d’ajuster automatiquement la thérapie en boucle fermée. 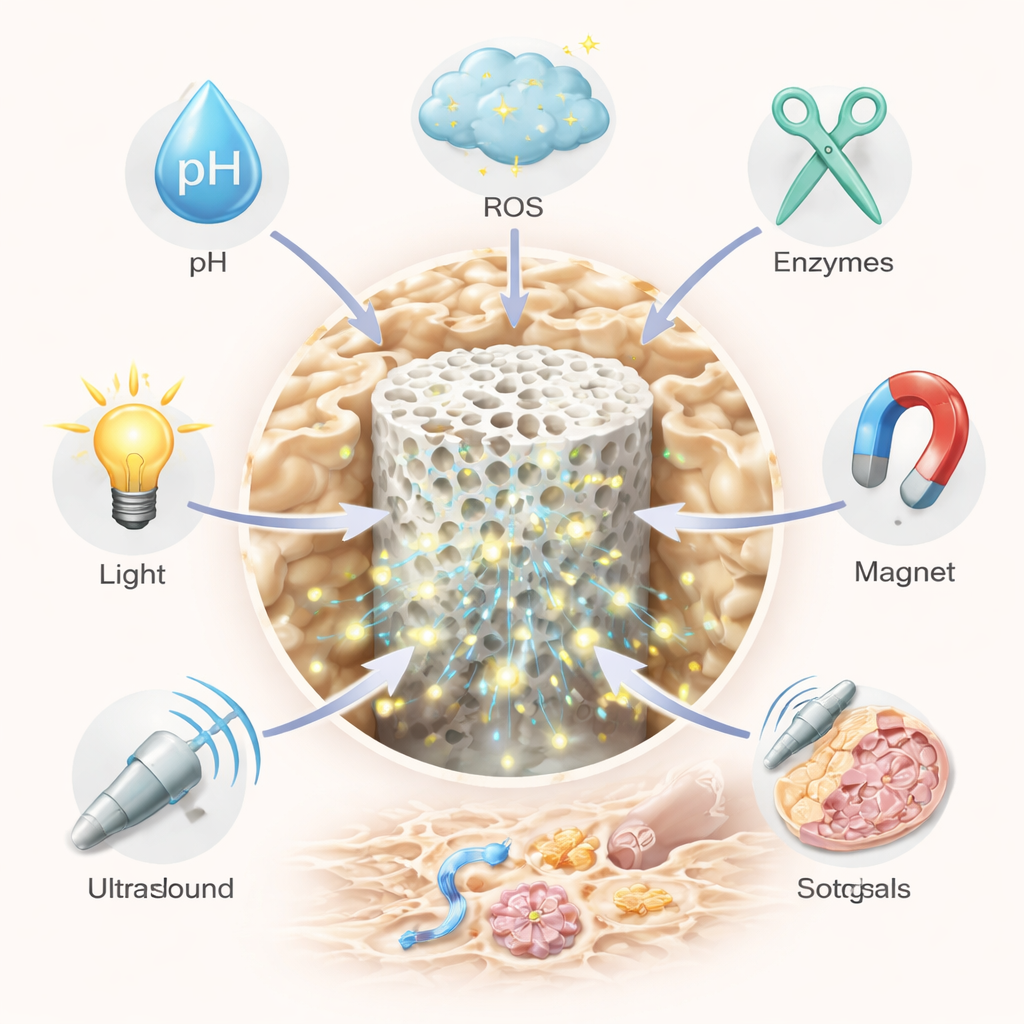
Ce que cela pourrait signifier pour les patients
En substance, ces travaux montrent que la fragilité osseuse liée à l’âge n’est pas une simple décroissance inéluctable mais un problème d’ingénierie complexe potentiellement soluble. Les biomatériaux intelligents agissent comme de petites équipes de réparation programmables : patrouillant dans le sang, s’installant sur les sites endommagés et libérant exactement ce qui est nécessaire, au bon moment, pour restaurer la structure et la fonction de l’os. Bien que ces technologies restent majoritairement au stade de la recherche, elles dessinent un avenir où les fractures guériraient plus vite, où les implants dureraient plus longtemps et où les traitements seraient adaptés à la biologie osseuse propre à chaque personne — aidant davantage de personnes à rester mobiles et autonomes jusque dans un âge avancé.
Citation: Liang, D., Wang, H., Jiang, Y. et al. Smart biomaterials for skeletal aging repair and regeneration. Bone Res 14, 24 (2026). https://doi.org/10.1038/s41413-026-00505-9
Mots-clés: biomatériaux intelligents, vieillissement squelettique, régénération osseuse, ostéoporose, échafaudages réactifs aux stimuli