Clear Sky Science · fr
Les vésicules extracellulaires dérivées des macrophages inflammatoires synoviaux aggravent les lésions du cartilage de manière triée par FMRP dans l’arthrose
Pourquoi l’inflammation articulaire compte pour les genoux douloureux
Beaucoup de personnes considèrent l’arthrose comme un simple « à‑force-de » lié au vieillissement des articulations, mais des preuves croissantes montrent qu’une inflammation de bas grade à l’intérieur de l’articulation peut faire progresser silencieusement la maladie. Cette étude pose une question précise : comment les cellules immunitaires de la membrane synoviale communiquent‑elles avec les cellules du cartilage, et peut‑on interrompre cette conversation pour protéger les articulations ? Les réponses révèlent un minuscule système de transport moléculaire qui aggrave les lésions — mais offre aussi une nouvelle voie pour diagnostiquer et traiter l’arthrose.
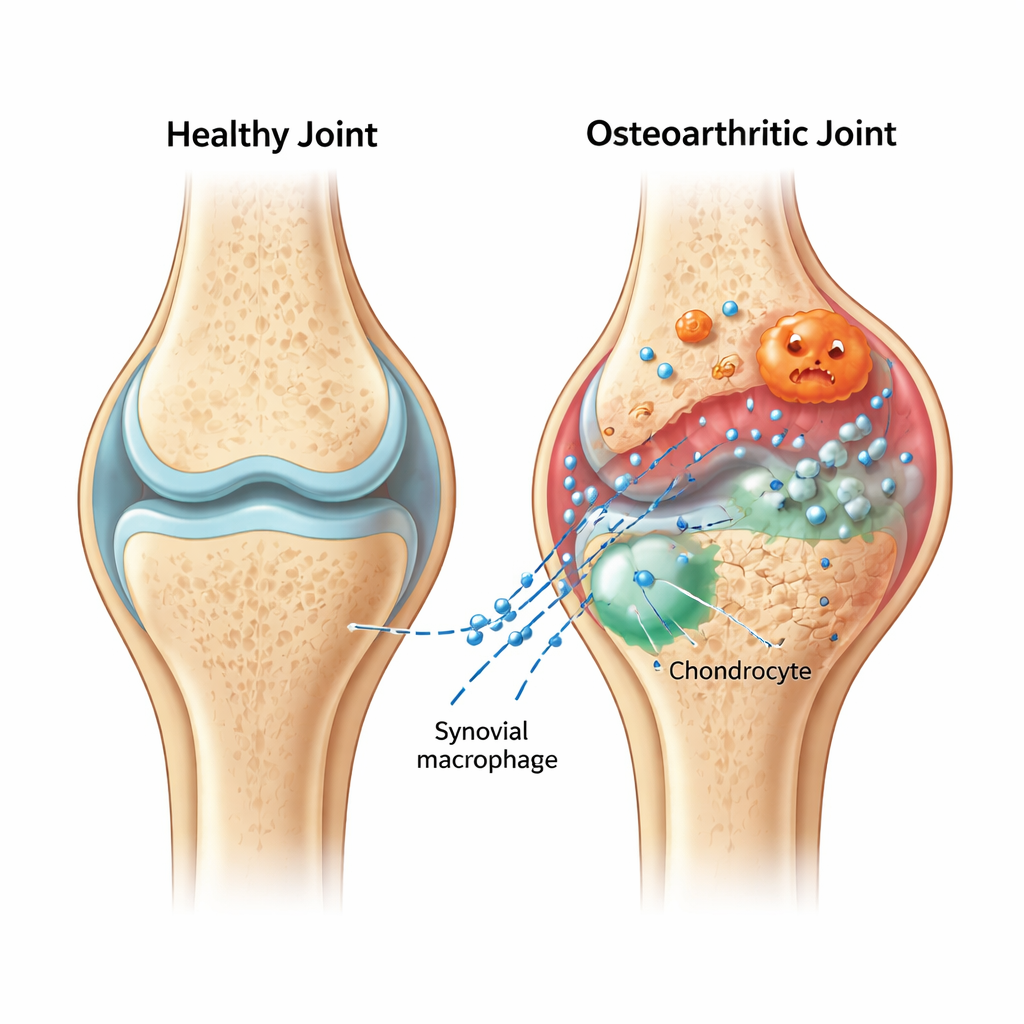
De petits colis qui apportent de mauvaises nouvelles
Dans un genou arthritique, la membrane synoviale s’enflamme et se remplit de cellules immunitaires appelées macrophages. Les auteurs se sont concentrés sur la version « pro‑inflammatoire » de ces cellules et sur les bulles microscopiques qu’elles libèrent, connues sous le nom de vésicules extracellulaires. Ces vésicules agissent comme des colis scellés, transportant des molécules entre les cellules. Chez des rats porteurs d’une arthrose induite chirurgicalement, l’équipe a montré que les vésicules issues de macrophages enflammés vont au cartilage et aggravent les lésions : la surface normalement lisse et amortissante devient plus rugueuse et plus fine, les protéines clés du cartilage diminuent tandis que les enzymes de dégradation augmentent.
Comment l’inflammation coupe le système d’auto‑nettoyage du cartilage
Les cellules du cartilage, ou chondrocytes, dépendent d’un processus d’entretien appelé autophagie pour recycler les composants usés et rester saines tout au long de la vie. Quand les chercheurs ont comparé les gènes activés dans le cartilage exposé aux vésicules inflammatoires à ceux exposés à une solution saline inerte, ils ont observé des signes nets de suppression des voies d’autophagie. Au microscope électronique, le cartilage provenant d’articulations traitées par vésicules contenait beaucoup moins des vésicules caractéristiques du recyclage. En culture cellulaire, les chondrocytes exposés aux vésicules de macrophages formaient aussi moins d’autophagosomes et d’autolysosomes, confirmant que leur machinerie d’auto‑nettoyage était désactivée à mesure que les lésions s’accumulaient.
Un seul microARN bascule un commutateur critique
En creusant davantage, l’équipe a examiné les petits ARN régulateurs empaquetés à l’intérieur des vésicules de macrophages. Une molécule, le miR‑155‑5p, s’est distinguée : elle était enrichie dans les vésicules d’animaux arthrosiques et dans les tissus articulaires d’arthrose humaine, en particulier dans la synoviale. Les expériences ont montré que le miR‑155‑5p délivré par les vésicules entre dans les chondrocytes et cible directement une protéine appelée GSK‑3β, qui aide normalement à retenir une voie de contrôle de la croissance connue sous le nom de mTORC1. Lorsque GSK‑3β est supprimée, mTORC1 devient hyperactif et l’autophagie chute, laissant les cellules du cartilage moins capables de faire face au stress. Bloquer le miR‑155‑5p avec un « antagomiR » conçu chez le rat a restauré l’autophagie, préservé la structure du cartilage et réduit les signes d’arthrose, tandis que des souris génétiquement privées de miR‑155 dans leurs macrophages développaient une forme plus légère de la maladie et moins de synovite.
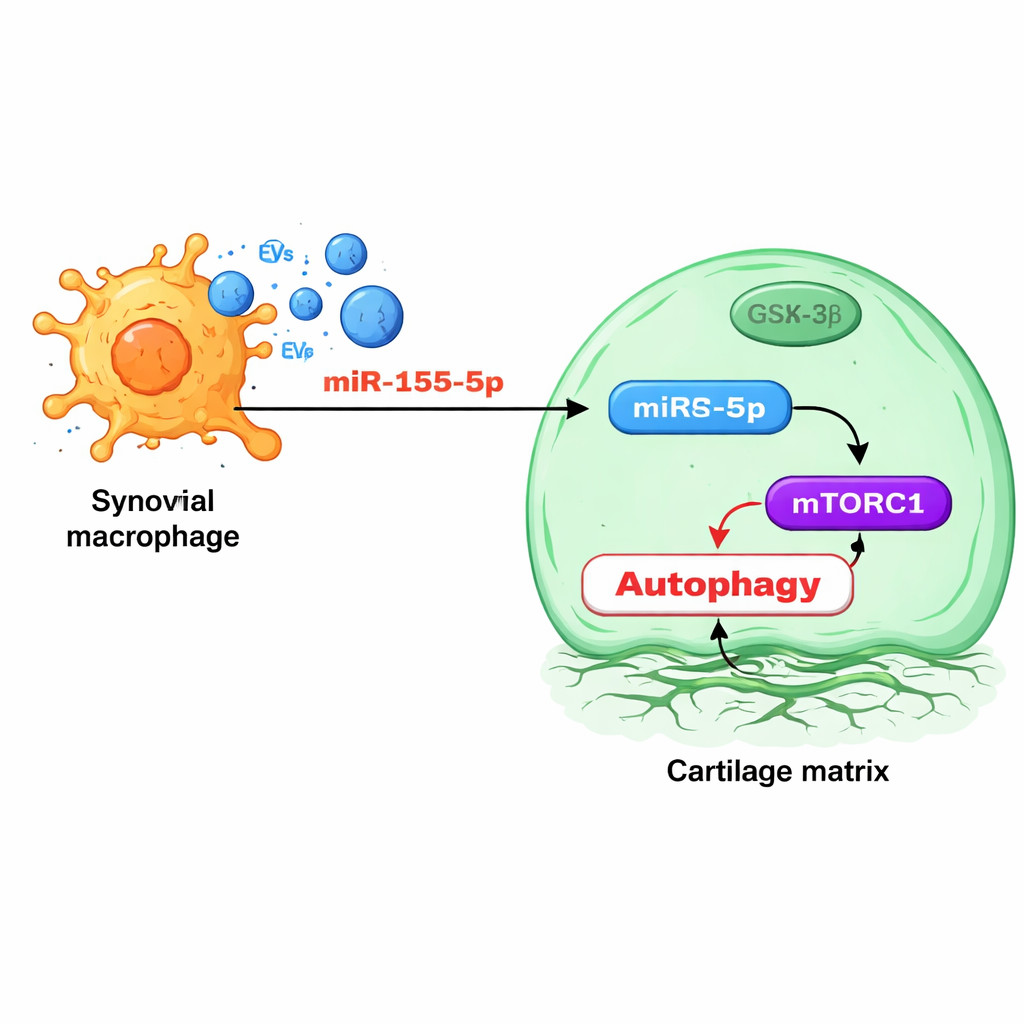
Tri et ciblage du signal délétère
De manière intrigante, l’étude a trouvé que les macrophages utilisent une protéine liant l’ARN spécifique, FMRP, pour charger sélectivement le miR‑155‑5p dans les vésicules. Lorsque les niveaux de FMRP augmentaient, les vésicules contenaient plus de miR‑155‑5p et endommageaient davantage les chondrocytes ; quand FMRP était réduit, les vésicules devenaient moins toxiques et l’autophagie des chondrocytes reprenait. Les niveaux de FMRP dans les vésicules circulant dans le sang augmentaient avec la progression de l’arthrose chez les rats et les patients humains, ce qui suggère que cette protéine, ou les vésicules qui la portent, pourrait servir de marqueur sanguin de l’activité de la maladie sans recourir à l’imagerie ou à des procédures invasives.
Une thérapie sans cellules qui cible les bonnes cellules
À partir de ces connaissances mécanistiques, les chercheurs ont conçu une thérapie potentielle utilisant des vésicules provenant de cellules stromales dérivées du tissu adipeux, un type de cellule proche des cellules souches présentes dans la graisse. Ils ont décoré ces vésicules d’un petit peptide qui agit comme un dispositif d’adressage pour les macrophages pro‑inflammatoires, et les ont chargées d’un antagomiR‑155‑5p. Chez des rats arthrosiques, des injections répétées de ces vésicules ciblées ont réduit l’inflammation synoviale, orienté les macrophages vers un état plus « réparateur », abaissé les niveaux de miR‑155‑5p dans l’articulation, restauré GSK‑3β et amélioré la structure et la composition du cartilage plus fortement que des vésicules non ciblées. Lorsqu’elles ont été appliquées à des échantillons de tissu synovial humain en laboratoire, les vésicules modifiées ont aussi réduit les marqueurs inflammatoires et renforcé les signaux anti‑inflammatoires.
Ce que cela signifie pour les personnes atteintes d’arthrose
Ce travail requalifie l’arthrose non seulement comme une maladie due à l’usure mécanique, mais comme un dialogue moléculaire entre les cellules inflammées de la membrane articulaire et le cartilage. Les macrophages pro‑inflammatoires envoient des vésicules chargées de miR‑155‑5p, qui désactivent les systèmes d’auto‑réparation des chondrocytes via la voie GSK‑3β/mTORC1 et accélèrent la dégradation des tissus. En bloquant ce signal — soit génétiquement, soit avec des vésicules thérapeutiques ciblées — les chercheurs ont pu atténuer à la fois l’inflammation et les lésions du cartilage dans des modèles animaux et des tissus humains. Bien qu’il reste beaucoup à faire avant que de telles stratégies n’atteignent la clinique, l’étude met en lumière de nouvelles possibilités : des tests sanguins basés sur le contenu des vésicules pour suivre la maladie, et des traitements précis et sans cellules qui calment l’inflammation nuisible tout en aidant le cartilage à se protéger.
Citation: Zhao, S., Wang, J., Xue, M. et al. Synovial inflammatory macrophage-derived extracellular vesicles exacerbate cartilage lesions with a FMRP-selectively sorted manner in osteoarthritis. Bone Res 14, 26 (2026). https://doi.org/10.1038/s41413-025-00502-4
Mots-clés: arthrose, vésicules extracellulaires, macrophages, cartilage, microARN-155