Clear Sky Science · fr
Efficacité du renforcement par cellules souches (RCS) pour la toxicité hématologique liée à la thérapie par lymphocytes CAR-T chez des patients atteints de myélome multiple réfractaire/récidivant (MMR/RRMM) — expérience du monde réel du consortium américain d’immunothérapie du myélome multiple
Pourquoi cela compte pour les patients et leurs familles
Pour les personnes atteintes d’un myélome multiple difficile à traiter, la thérapie par lymphocytes CAR-T a représenté une avancée majeure, mais elle peut laisser la moelle osseuse en difficulté pour produire de nouvelles cellules sanguines. Cette étude examine si l’administration d’un « boost » de leurs propres cellules souches prélevées et congelées antérieurement peut, en toute sécurité, aider à accélérer la récupération des numérations sanguines, réduisant potentiellement les infections, les saignements, les hospitalisations et le stress lié à une faiblesse prolongée et aux transfusions.
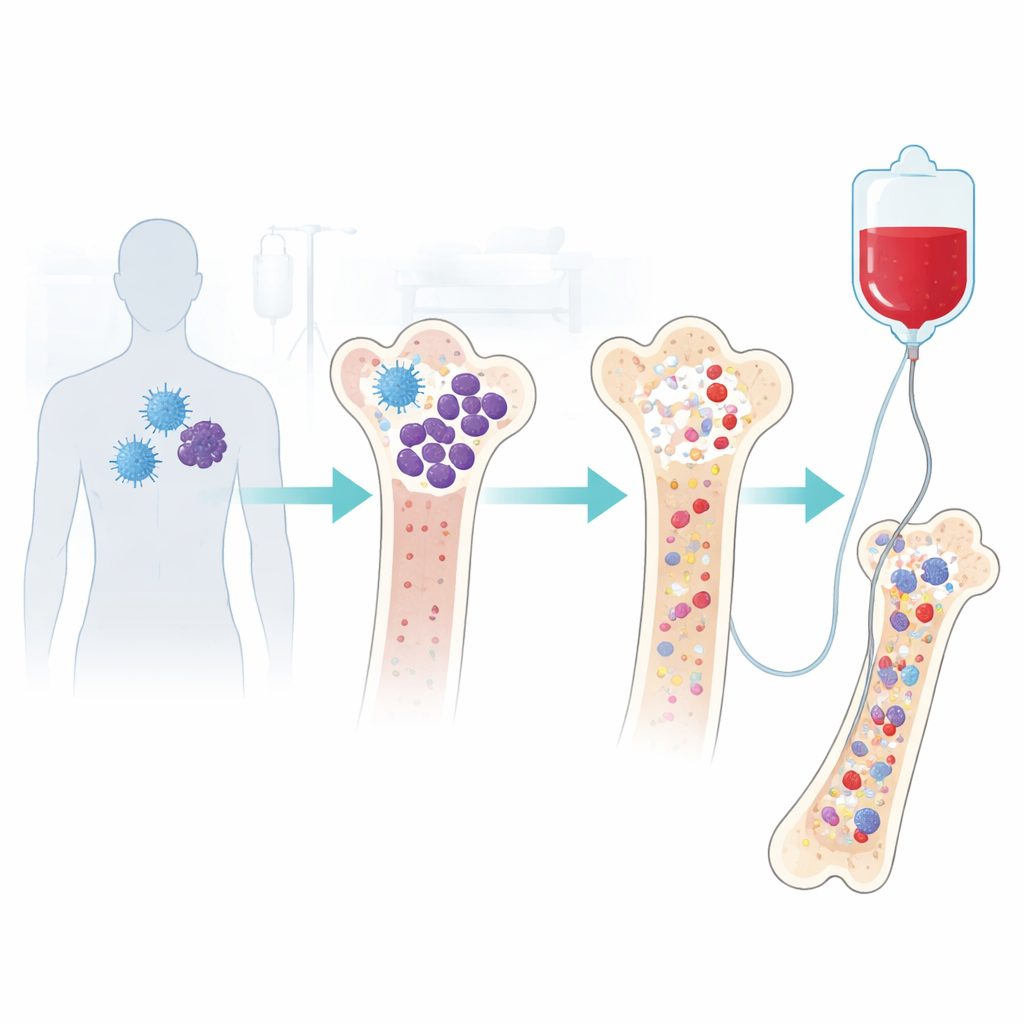
Un traitement puissant avec un revers persistant
La thérapie CAR-T réarme les cellules immunitaires du patient pour traquer et détruire les cellules de myélome. Bien que souvent efficace, ce traitement intensif peut endommager temporairement la moelle osseuse — notre « usine » interne de production sanguine. De nombreux patients voient leurs chiffres sanguins se rétablir en un à trois mois. Mais une minorité importante développe des « cytopénies » prolongées, c’est-à-dire des taux dangereusement bas de globules blancs, de globules rouges et de plaquettes. Cela augmente le risque d’infections graves, de fatigue et de saignements, et peut contraindre les patients à des transfusions fréquentes et à des injections de facteurs de croissance. Les médecins manquaient de meilleures options pour aider ces patients à récupérer sans compromettre les bénéfices de la CAR-T.
Un test en conditions réelles d’une idée simple
Les chercheurs ont examiné 590 adultes atteints de myélome multiple réfractaire ou récidivant traités par des produits CAR-T commerciaux dans 19 centres anticancéreux américains. Quatre-vingt-onze ont présenté des cytopénies prolongées ; parmi eux, 39 ont reçu un renforcement autologue par cellules souches et 52 ont reçu uniquement des soins de soutien standard. Le boost utilisait des cellules souches prélevées et congelées auparavant, souvent lors d’une greffe de cellules souches antérieure. Aucune chimiothérapie supplémentaire n’a été administrée avant le boost. Pour rendre la comparaison équitable, les patients du groupe contrôle ont été choisis parce qu’ils présentaient des baisses tout aussi sévères des globules blancs et des plaquettes à 30 jours après la CAR-T.
Récupération sanguine plus rapide et plus complète
Dans le groupe ayant reçu le renforcement par cellules souches, presque tous les patients évaluables (97,4 %) ont atteint la récupération des numérations sanguines selon les critères standard de greffe. Après le boost, les neutrophiles (globules blancs anti-infection) se sont généralement rétablis en environ 13 jours, les plaquettes en 18 jours et l’hémoglobine en 24 jours. À 90 jours après la CAR-T, les patients ayant reçu le boost présentaient des numérations sanguines clairement meilleures que les patients appariés n’ayant pas reçu le boost : hémoglobine plus élevée et plaquettes beaucoup plus nombreuses, avec une tendance également vers une meilleure numération des globules blancs. Ces bénéfices sont apparus même en se concentrant uniquement sur le sous-groupe le plus sévèrement atteint dans le groupe boost, suggérant que l’effet n’était pas seulement dû à la sélection de cas plus légers.
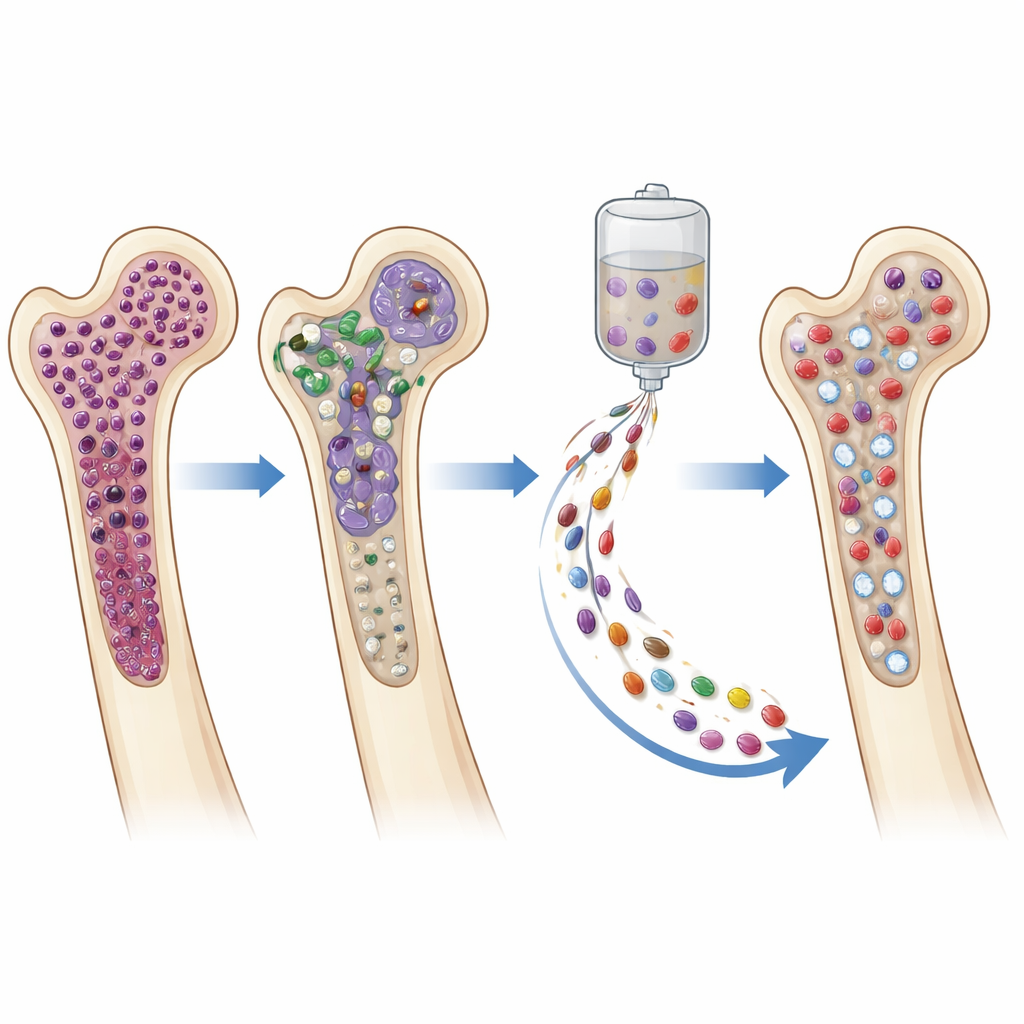
Sécurité, infections et contrôle du cancer
Il est important de noter que le renforcement par cellules souches n’a pas introduit de nouveaux problèmes de sécurité. Aucune complication n’a été directement attribuée au boost lui-même, et les infections graves dans le groupe boost sont survenues avant, et non après, l’administration des cellules souches. Quelques patients ont présenté des problèmes immunitaires complexes liés à la CAR-T, mais il n’y a pas eu de signal montrant que le boost ait aggravé ces problèmes dans cette cohorte. Tout aussi crucial, les cellules souches supplémentaires ne semblaient pas affaiblir l’effet anticancéreux de la CAR-T. Les taux de rémission profonde et de négativité pour la « maladie résiduelle minimale » étaient similaires entre les groupes, et les résultats de survie étaient au moins aussi bons dans le groupe boost, en gardant à l’esprit que les patients devaient survivre suffisamment longtemps pour recevoir le renforcement.
Ce que cela pourrait signifier pour les soins futurs
Pour les patients, l’idée essentielle est que la conservation de leurs propres cellules souches peut offrir une option de sauvetage puissante si les numérations sanguines stagnent après la CAR-T. Dans cette large série du monde réel, un renforcement par cellules souches — administré sans chimiothérapie supplémentaire — était sûr et a conduit à une récupération rapide et fiable de l’hématopoïèse chez presque tous les patients traités, tout en préservant les bénéfices anticancéreux de la CAR-T. Les auteurs suggèrent des critères pratiques pour envisager un boost, tels qu’un besoin persistant de transfusions au-delà de 30 jours et des numérations très basses sans signe d’amélioration. Des études prospectives sont encore nécessaires, mais ces résultats soutiennent l’idée de faire de la collecte et du stockage de cellules souches une étape routinière de la planification d’une CAR-T chez les patients myélomateux à haut risque.
Citation: Varga, C., Robinson, M., Davis, J.A. et al. Efficacy of stem cell boost (SCB) for chimeric antigen receptor-T cell therapy (CAR-T)-related hematologic toxicity in patients with relapsed/refractory multiple myeloma (RRMM)—real world experience from the US multiple myeloma immunotherapy consortium. Blood Cancer J. 16, 39 (2026). https://doi.org/10.1038/s41408-026-01469-z
Mots-clés: Thérapie CAR-T, myélome multiple, renforcement par cellules souches, récupération de la moelle osseuse, toxicité hématologique