Clear Sky Science · fr
Évaluation de la microdureté de la dentine après application de différents médicaments intracanalaires. Une étude in vitro
Pourquoi cela compte pour vos dents
Le traitement de canal est souvent considéré comme la dernière chance de sauver une dent fortement endommagée. Si les dentistes utilisent des médicaments puissants à l’intérieur de la racine nettoyée pour éliminer les bactéries et favoriser la guérison, ces mêmes substances peuvent involontairement fragiliser la dent de l’intérieur. Cette étude examine quels médicaments intracanalaires couramment utilisés protègent le mieux la couche dure interne de la dent — appelée dentine — afin que les dents traitées restent solides et moins sujettes aux fissures ou aux fractures avec le temps.
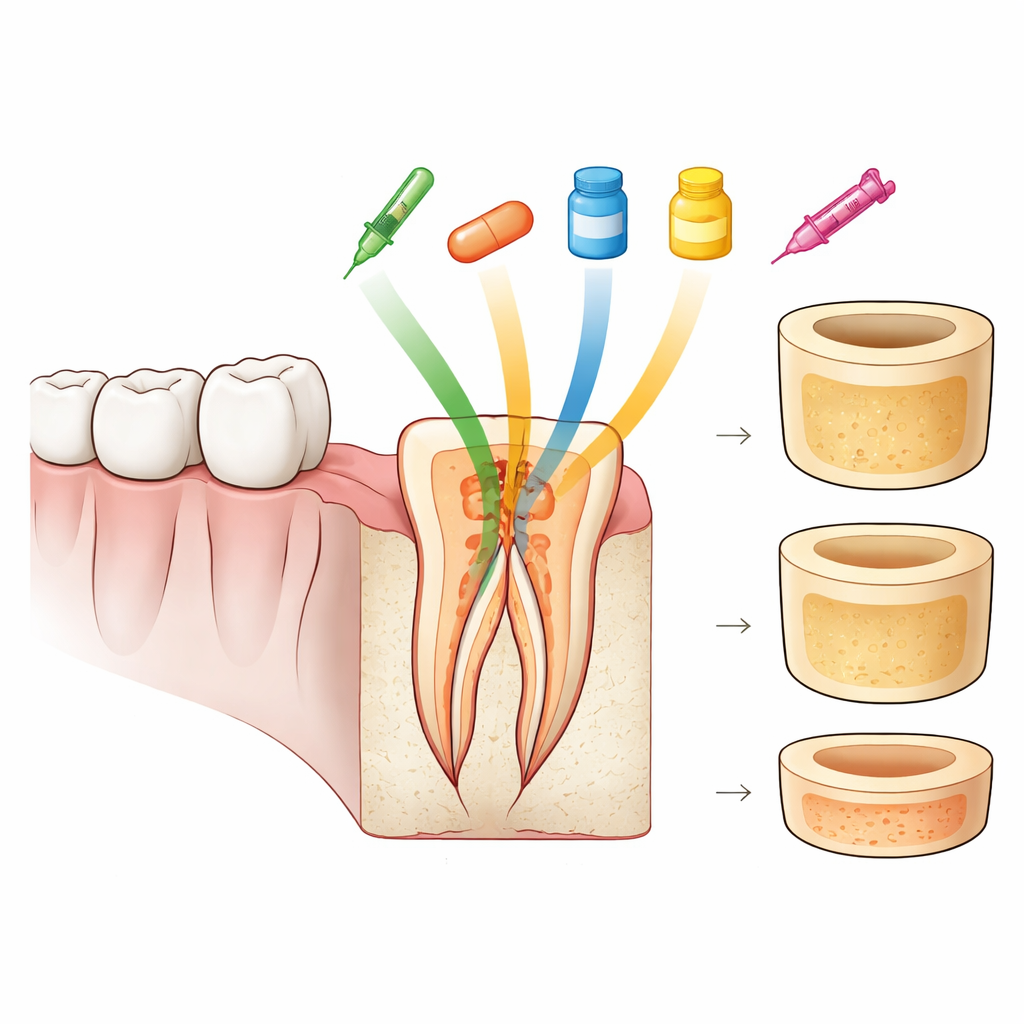
Conserver la solidité d’une dent traitée
Pour qu’un traitement de canal dure, deux choses doivent se produire : les germes à l’intérieur de la racine doivent être éliminés et la structure restante de la dent doit rester mécaniquement intacte. Si la dentine devient plus molle, les obturations et matériaux d’obturation n’adhèrent pas aussi bien et la racine peut devenir plus susceptible de se fracturer. De nombreux médicaments peuvent désinfecter le canal, mais ils peuvent aussi dissoudre des minéraux ou endommager l’armature interne de la dent. Les auteurs se sont concentrés sur une mesure simple mais révélatrice — la « microdureté », essentiellement la résistance de la dentine à l’empreinte — comme indicateur de la solidité globale.
Cinq médicaments mis à l’épreuve
Les chercheurs ont collecté quarante‑cinq dents humaines à racine unique extraites pour des raisons non liées à la carie radiculaire. Ils ont tronçonné les dents à une longueur standard et préparé les canaux radiculaires comme le ferait un dentiste lors d’un traitement courant. Les dents ont ensuite été réparties aléatoirement en cinq groupes, chacun recevant un médicament différent dans le canal pendant deux semaines : une pâte moderne à base de silicate de calcium (Bio‑C Temp), des fibres ultrafines chargées d’antibiotiques (nanofibres antibiotiques modifiées, ou m‑TAP), un gel antibiotique à large spectre (lévofloxacine), un matériau classique de longue date (hydroxyde de calcium) et un médicament hypocholestérolémiant réutilisé en odontologie (simvastatine). Après retrait des médicaments, l’équipe a mesuré la dureté de la dentine dans trois zones le long de la racine — près de la couronne (coronal), au milieu et près de l’apex (apical) — à l’aide d’un instrument d’indentation précis.
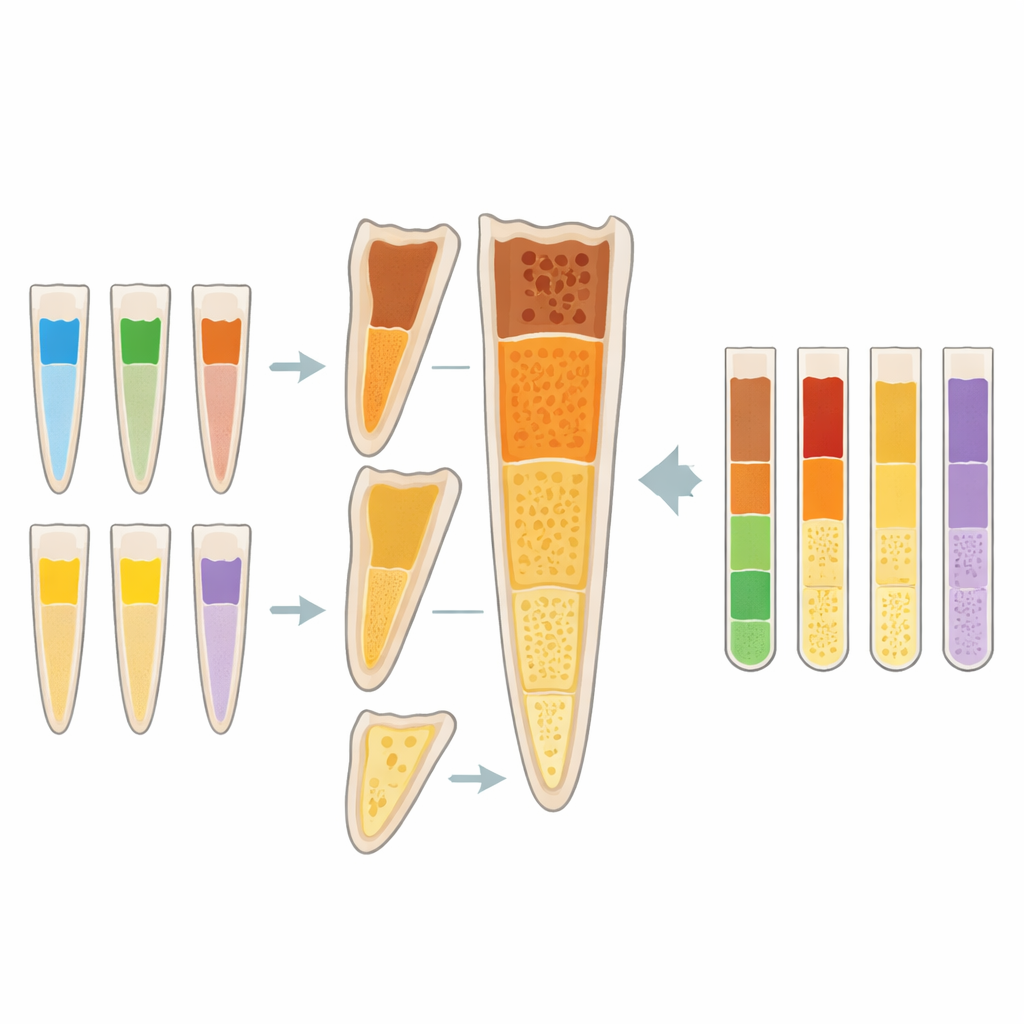
Ce qui s’est passé à l’intérieur des racines
Bio‑C Temp et les nanofibres antibiotiques se sont distingués, affichant la dureté de dentine la plus élevée dans l’ensemble, en particulier dans les parties coronale et médiane de la racine. La lévofloxacine et la simvastatine ont donné des résultats intermédiaires : elles n’ont pas atteint les performances des deux premiers, mais elles étaient nettement supérieures à l’option la plus faible. L’hydroxyde de calcium — l’outil de travail de longue date dans de nombreuses pratiques dentaires — a systématiquement donné les valeurs de dureté les plus faibles, indiquant un ramollissement accru de la dentine. Fait intéressant, près de l’extrémité apicale de la racine, les cinq médicaments ont produit une réduction de dureté similaire, suggérant que cette région a tendance à être plus fragile quel que soit le produit utilisé, probablement en raison de différences anatomiques naturelles et d’une pénétration limitée des matériaux.
Pourquoi certaines options ont mieux fonctionné
La performance supérieure de Bio‑C Temp semble provenir de sa base en silicate de calcium, qui peut libérer des ions favorisant de nouveaux dépôts minéraux dans les microcanaux de la dentine, contribuant ainsi à reconstruire et raidir le tissu plutôt qu’à le dégrader. Le système de nanofibres antibiotiques offre une forte action antibactérienne à très faibles concentrations de médicament, ce qui peut limiter la perte minérale liée à l’acidité parfois observée avec les pâtes antibiotiques traditionnelles. En revanche, la forte alcalinité de l’hydroxyde de calcium peut perturber le réseau de collagène qui maintient les minéraux de la dentine, affaiblissant progressivement la structure interne. Les résultats mitigés pour la lévofloxacine et la simvastatine reflètent les preuves limitées à ce jour : les antibiotiques peuvent éroder les minéraux dentaires s’ils sont trop acides, tandis que la simvastatine peut soutenir la formation minérale mais n’a pas égalé les meilleurs matériaux dans ce test à court terme.
Ce que cela signifie pour les patients
Dans l’ensemble, l’étude montre que tous les médicaments de canal ne sont pas également compatibles avec la solidité interne de la dent. Les auteurs écartent l’idée que ces matériaux ont des effets similaires : Bio‑C Temp et les nanofibres antibiotiques ont le mieux préservé la dureté, tandis que l’hydroxyde de calcium a le plus ramolli la dentine. Pour les patients, cela signifie que des matériaux plus récents peuvent offrir un meilleur équilibre entre l’élimination des germes et le maintien d’une dent suffisamment solide pour durer. Bien que des recherches supplémentaires soient nécessaires — en particulier des études à long terme reproduisant les forces réelles de mastication — ces résultats suggèrent qu’un choix attentif du médicament intracanalaire pourrait réduire le risque de fractures radiculaires futures et permettre aux dents traitées de rester fonctionnelles pendant de nombreuses années.
Citation: Elgamal, S.G., Aly, K.H.A. & Hosny, N.S. Assessment of the dentine microhardness following the application of different intracanal medicaments. An in-vitro study. BDJ Open 12, 23 (2026). https://doi.org/10.1038/s41405-026-00408-1
Mots-clés: traitement de canal radiculaire, résistance de la dentine, médicaments intracanaux, pâte à base de silicate de calcium, nanofibres dentaires