Clear Sky Science · fr
L’expression astrocytaire d’APOE3-Christchurch améliore la pathologie amyloïde-β cérébrale chez des souris 5xFAD
Pourquoi cette variante cérébrale compte
La maladie d’Alzheimer est généralement présentée comme une accumulation implacable d’amas protéiques nocifs dans le cerveau. Pourtant, quelques personnes paraissent exceptionnellement résistantes, restant lucides malgré des risques génétiques élevés. Cette étude se concentre sur l’une de ces variantes protectrices d’un gène courant impliqué dans le métabolisme du cholestérol et pose une question concrète : si l’on augmente la présence de cette version protectrice dans le cerveau — spécifiquement produite par les cellules de soutien appelées astrocytes — peut-on rendre les changements de type Alzheimer moins nocifs ?
Une variante génétique protectrice sous les projecteurs
Le travail porte sur une version rare du gène APOE, nommée APOE3-Christchurch. Dans un cas réel remarquable, une femme porteuse d’une mutation causant une forme précoce et agressive d’Alzheimer est restée indemne sur le plan cognitif pendant des décennies de plus que prévu, et cette variante APOE semblait être une raison majeure. Des études antérieures chez l’animal suggéraient qu’APOE3-Christchurch peut ralentir la propagation d’une autre protéine marquante de la maladie, la protéine tau. Mais son influence sur l’amyloïde‑bêta, la protéine qui forme les plaques classiques dans les cerveaux atteints d’Alzheimer, restait encore mal définie. Les chercheurs ont donc cherché à savoir comment cette variante se comporte lorsqu’elle est exprimée spécifiquement par les astrocytes, ces cellules étoilées qui nourrissent et protègent les neurones.
Tester la variante dans une souris modèle d’Alzheimer
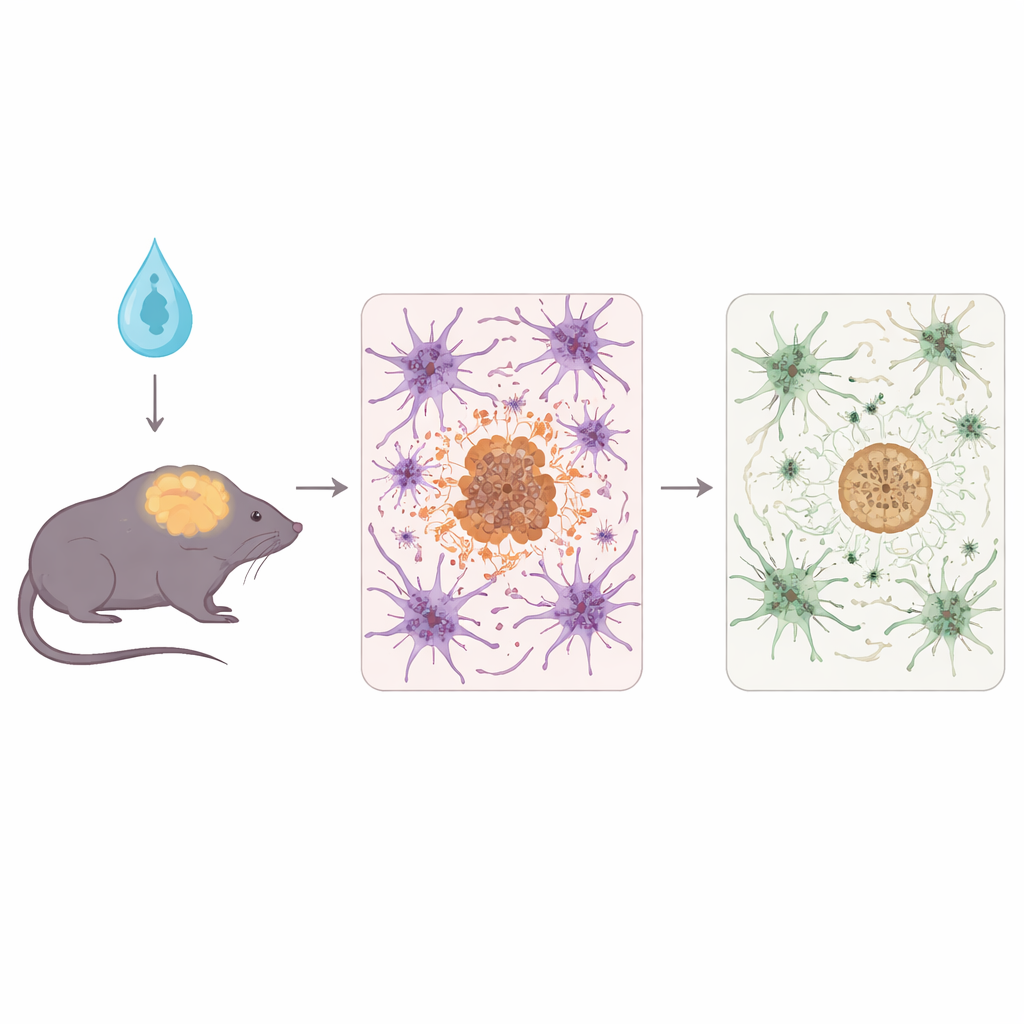
Pour étudier cela, l’équipe a utilisé des souris 5xFAD, un modèle bien établi qui développe rapidement une importante accumulation d’amyloïde et des lésions cérébrales associées. Peu après la naissance, les souris ont reçu un vecteur viral inoffensif qui a amené leurs astrocytes à produire soit l’APOE3 humain courant, soit la version protectrice APOE3-Christchurch, soit une protéine témoin neutre. Les scientifiques ont ensuite examiné les animaux à un stade avancé de la maladie, analysant les tissus cérébraux par des tests biochimiques, la microscopie à fluorescence et le séquençage de l’ARN pour voir comment l’amyloïde, les fibres nerveuses avoisinantes et les réponses immunitaires étaient modifiées.
Rendre les plaques moins toxiques, pas seulement moins nombreuses
Les deux formes d’APOE produites par les astrocytes ont réduit la charge globale en plaques amyloïdes et les signes de dommages autour de ces plaques comparé aux témoins. Mais APOE3-Christchurch a montré des effets plus nuancés. Elle a déplacé l’amyloïde vers des plaques plus compactes, sphériques et fibrillaires et réduit les niveaux de certaines formes solubles et oligomériques d’amyloïde‑bêta — des espèces considérées comme particulièrement toxiques pour les synapses. Les neurites, ces fines projections des cellules nerveuses situées près des plaques, présentaient moins de distorsion et de lésions en présence d’APOE3-Christchurch. Parallèlement, les cellules immunitaires cérébrales appelées microglies et astrocytes étaient globalement moins réactives, et les analyses du transcriptome ont révélé un affaiblissement des voies immunitaires et de stress protéique, suggérant un environnement plus calme et moins hostile pour les neurones.
Indices issus de cultures cellulaires et de l’activité génétique
Pour confirmer que ces effets ne se limitaient pas aux souris, l’équipe a aussi utilisé des astrocytes dérivés de cellules souches humaines, modifiés pour porter soit APOE3 soit la variante Christchurch. Les astrocytes portant APOE3-Christchurch sécrétaient plus de protéine APOE, et leur milieu conditionné réduisait la formation d’oligomères d’amyloïde‑bêta dans un test in vitro contrôlé. Dans le cerveau des souris, l’expression d’APOE3-Christchurch modifiait des réseaux de gènes impliqués dans le repliement des protéines, le stress cellulaire et la signalisation immunitaire, et diminuait les niveaux de protéines liées aux réponses au stress et au désordre du métabolisme lipidique. Ensemble, ces éléments suggèrent qu’APOE3-Christchurch ne se contente pas de modifier la quantité d’amyloïde — elle change sa forme et la manière dont les cellules cérébrales y réagissent.
Ce que cela pourrait signifier pour de futurs traitements
Si les effets protecteurs observés ici sont modestes plutôt que miraculeux, ils sont néanmoins très instructifs. L’étude montre qu’augmenter spécifiquement APOE3-Christchurch dans les astrocytes peut rendre les dépôts amyloïdes plus compacts et apparemment moins toxiques, réduire les dommages neuronaux avoisinants et atténuer les signaux inflammatoires et de stress, même sans éliminer totalement l’amyloïde. Pour un lecteur non spécialiste, l’idée essentielle est que toutes les plaques ne sont pas également dommageables : les remodeler et les neutraliser peut être aussi important que les éliminer. Ces résultats étayent l’idée que des thérapies inspirées d’APOE3-Christchurch — peut‑être délivrées par thérapie génique ou par des médicaments mimant son comportement — pourraient aider le cerveau à mieux tolérer la présence d’amyloïde et potentiellement ralentir ou atténuer la progression de la maladie d’Alzheimer.
Citation: Raulin, AC., Alnobani, A., Rodriguez-Martinez, P. et al. Astrocytic APOE3-Christchurch expression ameliorates brain amyloid-β pathology in 5xFAD mice. Transl Psychiatry 16, 224 (2026). https://doi.org/10.1038/s41398-026-04002-9
Mots-clés: Maladie d’Alzheimer, APOE3-Christchurch, amyloïde-bêta, astrocytes, thérapie génique