Clear Sky Science · fr
De faibles concentrations d’oligomères d’amyloïde‑bêta induisent une synaptogenèse caractéristique des troubles cognitifs légers et modifient le protéome de novo
Modifications précoces pouvant annoncer des troubles de la mémoire
Avant que la maladie d’Alzheimer n’emporte la mémoire des personnes, le cerveau traverse un état intermédiaire flou appelé trouble cognitif léger. Durant cette phase, des difficultés de réflexion sont détectables mais la vie quotidienne se poursuit souvent. Étonnamment, certaines régions cérébrales présentent alors davantage, et non moins, de connexions entre neurones. Cette étude se demande si de faibles quantités d’une molécule toxique liée à Alzheimer peuvent provoquer cette flambée de nouvelles connexions, et si un médicament déjà testé chez des patients atteints de cancer pourrait atténuer ces modifications très précoces.
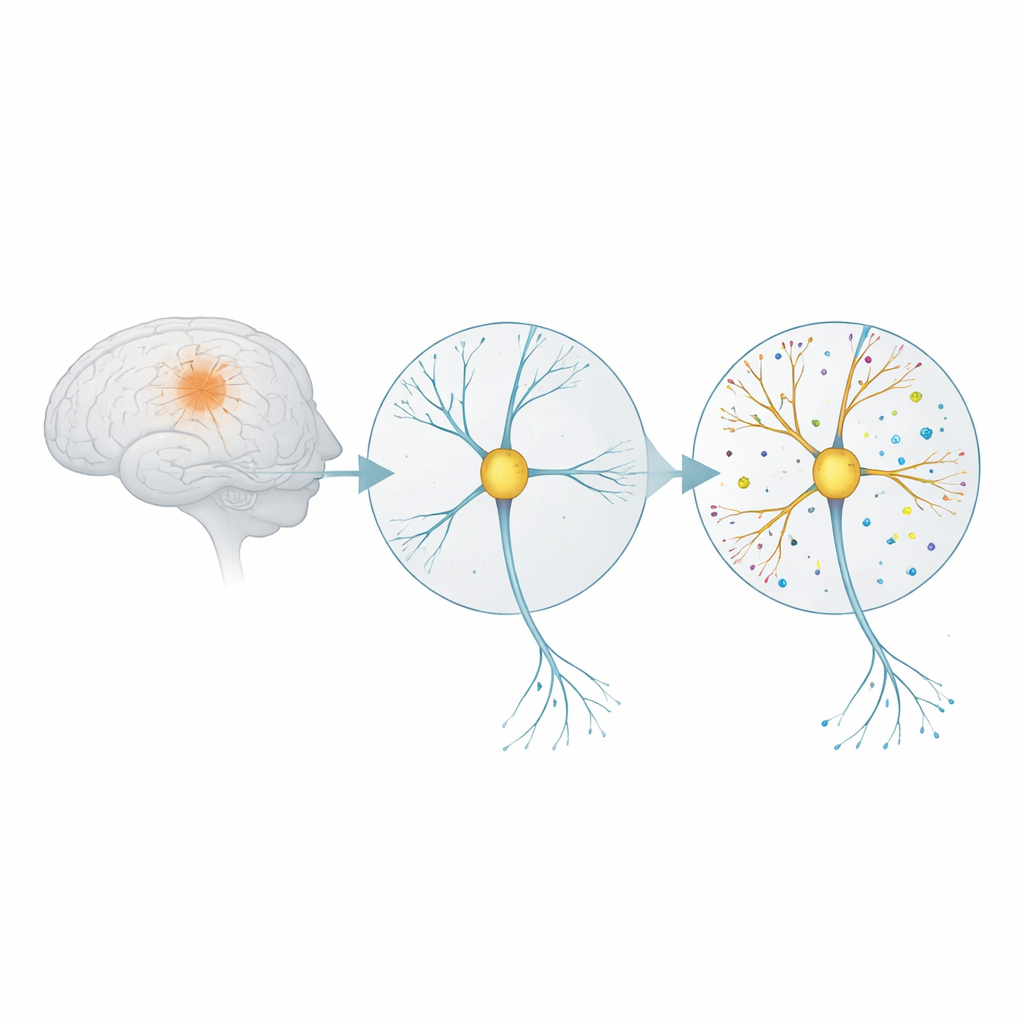
Comment les connexions cérébrales réagissent à un déclencheur toxique
La maladie d’Alzheimer est étroitement associée à de petits agrégats d’un fragment protéique appelé amyloïde‑bêta. Sous forme d’oligomères, ce fragment est particulièrement nocif pour les synapses — les points de contact par lesquels les neurones communiquent. Les chercheurs ont cultivé des cellules cérébrales de rat en culture jusqu’à formation de réseaux matures, puis les ont exposées pendant cinq jours à une faible dose d’oligomères d’amyloïde‑bêta. Ils ont aussi testé l’effet d’un composé nommé eFT508, qui bloque une enzyme de signalisation (MNK) impliquée dans le démarrage de la synthèse protéique intracellulaire. Ce dispositif visait à reproduire des stades très précoces de la maladie, avant une mort cellulaire généralisée.
Voir en détail les nouveaux synapses cachés
Pour examiner l’évolution des connexions, l’équipe a utilisé la « microscopie d’expansion », une technique qui dilate physiquement des cellules préservées dans un gel souple afin de rendre visibles des structures très petites avec plus de précision. Ils ont marqué les fibres nerveuses et les deux faces de la synapse avec des marqueurs fluorescents et les ont reconstruites en 3D. L’exposition à l’amyloïde‑bêta a provoqué une augmentation nette du nombre de synapses le long des branches neuronales. On a observé en particulier davantage de boutons simples — contacts un à un — et des « épines multi‑innervées » inhabituelles, où plusieurs fibres entrantes convergent sur un même site récepteur. Ces motifs ressemblent aux augmentations synaptiques décrites chez des personnes atteintes de trouble cognitif léger. En présence d’eFT508, le nombre de synapses est revenu vers la normale, suggérant que le médicament pourrait contrer cette surcroissance précoce.
Des nouvelles protéines changent, même si le total reste identique
Les synapses se remodèlent en permanence par la synthèse et la dégradation des protéines. L’équipe a ensuite analysé quelles protéines étaient nouvellement synthétisées pendant et après l’exposition à l’amyloïde‑bêta. Ils ont fourni aux neurones un acide aminé artificiel inoffensif qui s’incorpore dans les protéines fraîchement synthétisées, puis ont utilisé des réactions chimiques de « click » et la spectrométrie de masse pour isoler et identifier ces molécules. De manière surprenante, la quantité totale de nouvelles protéines synthétisées n’a pas changé après plusieurs jours d’exposition à faible dose d’amyloïde‑bêta, avec ou sans eFT508. Mais l’examen des espèces protéiques produites a donné un tableau très différent : plus d’un millier de protéines nouvellement synthétisées ont été détectées, et des dizaines d’entre elles ont été modulées à la hausse ou à la baisse en réponse à l’amyloïde‑bêta. Beaucoup participent à la communication synaptique, à l’architecture interne de la cellule, aux mitochondries productrices d’énergie, aux systèmes d’élimination des déchets et au contrôle de la qualité protéique.
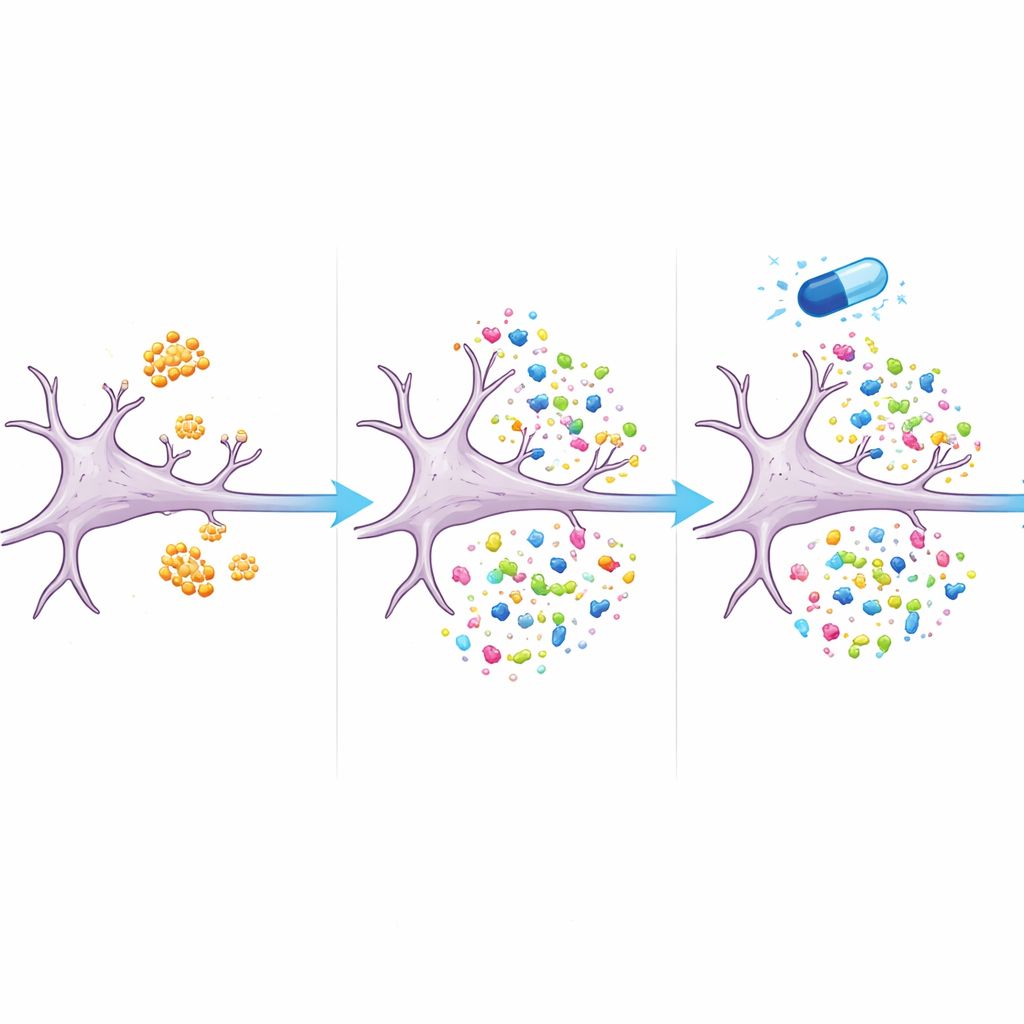
Un médicament qui réoriente l’équilibre protéique
De manière cruciale, de nombreuses protéines perturbées sont revenues vers des niveaux plus normaux lorsque les cellules ont été traitées simultanément par eFT508 et amyloïde‑bêta. Plus des deux tiers des protéines altérées par l’amyloïde‑bêta seules n’étaient plus significativement différentes des cellules non traitées en présence du médicament. Cela comprenait des protéines liées à la structure et à la fonction synaptiques, ainsi que des composants des systèmes de recyclage cellulaire et de production d’énergie. Les résultats suggèrent que eFT508 n’éteint pas simplement la production protéique ; il semble plutôt remodeler le profil des protéines synthétisées, orientant le système loin d’un schéma de type Alzheimer vers un équilibre plus sain.
Ce que cela pourrait signifier pour les traitements futurs
Ce travail décrit les dommages précoces associés à Alzheimer comme une phase de sur‑connexion et de déséquilibre protéique subtil plutôt que de perte nette. De faibles niveaux d’amyloïde‑bêta favorisent la formation de synapses supplémentaires, parfois atypiques, et déforment sélectivement le mélange de protéines produit par les neurones. Dans ce modèle en culture, eFT508 peut à la fois normaliser le nombre de synapses et corriger de nombreux changements protéiques, laissant entrevoir que le réglage fin de la synthèse protéique pourrait ralentir ou prévenir la transition du trouble cognitif léger vers une démence manifeste. Bien qu’il reste beaucoup à tester chez l’animal vivant et chez l’humain, l’étude met en lumière une nouvelle façon de penser — et peut‑être d’intervenir — aux tout premiers stades de la maladie d’Alzheimer.
Citation: Wu, K., Lee, S., Martinez-Serra, R. et al. Low concentrations of amyloid-beta oligomers induce synaptogenesis characteristic for mild cognitive impairment and alter the de novo proteome. Transl Psychiatry 16, 132 (2026). https://doi.org/10.1038/s41398-026-03905-x
Mots-clés: Maladie d’Alzheimer, modifications des synapses, oligomères d’amyloïde bêta, <keyword>dégénérescence neurodébutante