Clear Sky Science · fr
Effets prénataux et postnataux de l’activation immunitaire gestationnelle sur les voies synaptiques et neurodéveloppementales via des mécanismes épigénétiques
Comment le système immunitaire maternel façonne le cerveau de l’enfant
Les infections pendant la grossesse sont depuis longtemps associées à un risque accru de troubles tels que la schizophrénie, l’autisme et le TDAH chez les enfants, mais le « pont » biologique entre une mère malade et un cerveau adulte vulnérable restait flou. Cette étude, réalisée chez la souris, montre comment la réponse immunitaire maternelle à la grippe pendant la gestation peut laisser des marques chimiques durables sur le cerveau en développement, modifier la communication entre cellules cérébrales et potentiellement augmenter le risque de troubles neurologiques et de santé mentale ultérieurs.
Maladie pendant la grossesse et risque cérébral à vie
Les études épidémiologiques chez l’homme ont montré que lorsque des femmes enceintes contractent des infections, leurs enfants ont une probabilité plus élevée de développer, à l’âge adulte, une gamme de troubles psychiatriques et neurodéveloppementaux. Les auteurs se concentrent sur l’activation immunitaire maternelle, la cascade de signaux immunitaires libérés lorsque l’organisme combat une infection. Ces signaux peuvent traverser ou influencer le placenta et interagir avec le cerveau en développement à un moment où les circuits se mettent en place. Le cortex frontal — essentiel pour la planification, la prise de décision et le contrôle émotionnel — se développe sur une longue période et est particulièrement sensible aux perturbations précoces.
Disséquer les effets prénataux et postnataux
Pour séparer ce qui se passe in utero de ce qui se produit après la naissance, les chercheurs ont infecté des souris gestantes avec un virus grippal léger et non létal au cours d’un stade précoce de la gestation équivalent à la fin du premier trimestre chez l’humain. Certains petits sont restés avec leur mère biologique, tandis que d’autres ont été placés en famille d’accueil dans les 24 heures suivant la naissance. Cela a généré quatre groupes : des descendants sans exposition avant ou après la naissance, exposés uniquement avant la naissance, uniquement après la naissance, ou pendant les deux périodes. À l’âge adulte, l’équipe a examiné les neurones du cortex frontal, étudiant à la fois l’activité des gènes et les « marques épigénétiques » — des étiquettes chimiques sur les protéines empaquetant l’ADN qui aident à contrôler l’activation ou la répression des gènes. 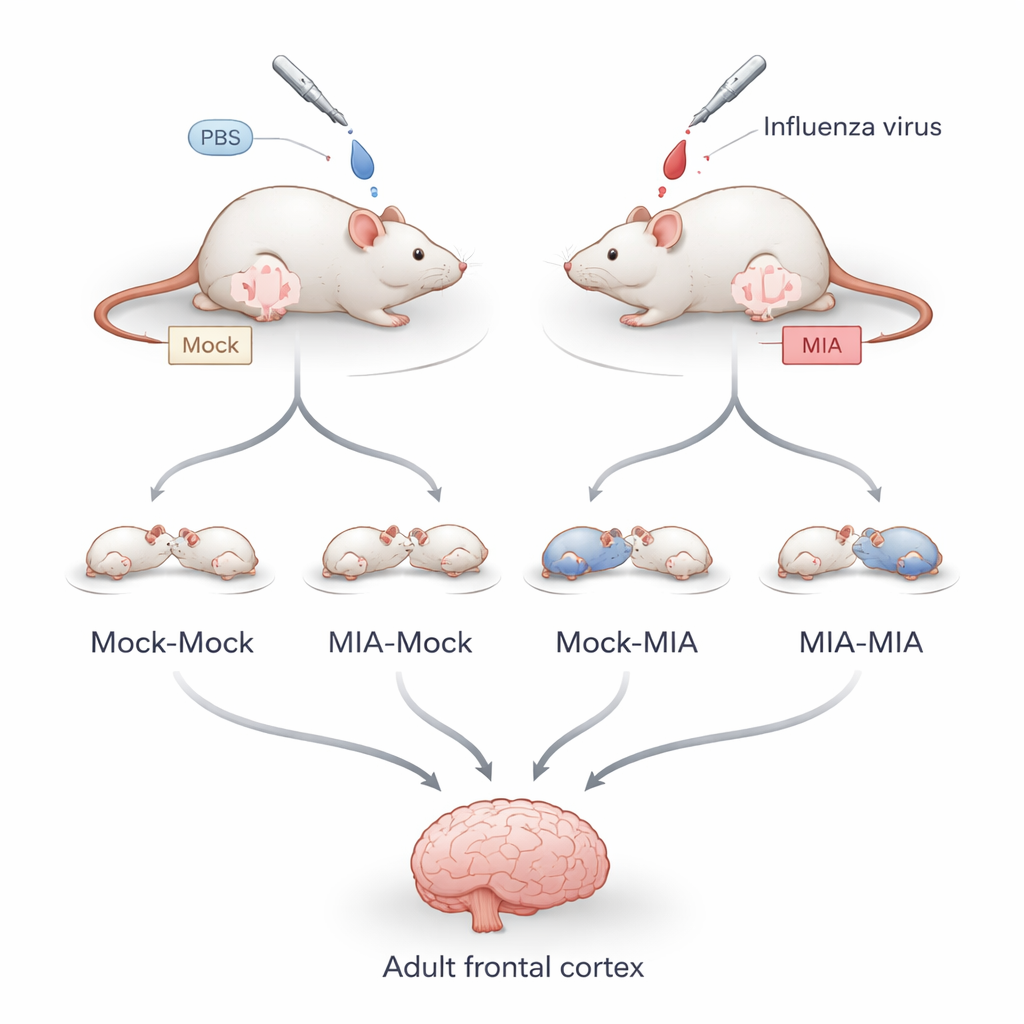
Marques chimiques durables sur l’ADN cérébral
L’étude s’est concentrée sur deux marques d’histones, H3K27ac et H3K4me3, qui signalent des interrupteurs actifs et des points de départ pour les gènes. Grâce à des méthodes de séquençage sensibles, les auteurs ont cartographié des dizaines de milliers de ces régions régulatrices et mesuré quels gènes étaient plus ou moins actifs dans chaque groupe. Ils ont constaté que l’activation immunitaire maternelle prénatale entraînait des changements étendus et durables dans les régions enhancers — des segments d’ADN qui servent de boutons de contrôle pour l’activité génétique. Ces altérations étaient particulièrement enrichies dans les gènes impliqués dans la construction du prosencéphale, l’orientation des fibres nerveuses en croissance et l’établissement des premiers points de communication entre neurones. Beaucoup de ces mêmes gènes présentaient également une activité modifiée après la naissance chez les petits élevés par des mères ayant subi une activation immunitaire, indiquant une trajectoire régulatrice soutenue au cours du développement plutôt qu’un choc de courte durée.
Des changements épigénétiques aux synapses et aux circuits
Les expositions prénatales et postnatales ont influencé des voies moléculaires qui régissent la manière dont les neurones communiquent entre eux. Des gènes liés au glutamate (le principal neurotransmetteur excitateur), au GABA (le principal neurotransmetteur inhibiteur) et à la dopamine (importante pour la motivation et la récompense) ont montré des modifications coordonnées de leurs éléments régulateurs et de leurs niveaux d’expression. Ces systèmes sont régulièrement impliqués dans la schizophrénie, la dépression, l’autisme et l’addiction. Les auteurs ont également trouvé que des gènes impliqués dans l’organisation des synapses, la croissance des axones et le raffinement des circuits cérébraux étaient affectés, en particulier par l’exposition postnatale, ce qui suggère que le comportement maternel et des changements immunitaires persistants après la naissance contribuent à façonner le câblage et le réglage des réseaux neuronaux. Des analyses de réseaux ont mis en évidence un ensemble central de facteurs de transcription — des régulateurs maîtres de l’activité génétique — perturbés au cours des deux fenêtres temporelles.
Liens avec le risque psychiatrique humain
Pour évaluer la pertinence de ces changements chez la souris pour les maladies humaines, l’équipe a converti les emplacements des enhancers et promoteurs de souris vers leurs homologues humains les plus proches et les a comparés à de grandes études génétiques sur les troubles psychiatriques. Les régions modifiées par l’activation immunitaire maternelle étaient fortement enrichies en loci de risque humain pour la schizophrénie, le trouble bipolaire, la dépression, le névrosisme et le TDAH, mais pas pour la plupart des affections non psychiatriques. Ce profil suggère que les mêmes types de régions régulatrices de l’ADN qui portent un risque génétique hérité pour les maladies mentales sont aussi sensibles aux défis immunitaires pendant la grossesse et la petite enfance, en faisant un point de convergence entre gènes et environnement. 
Que signifie cela pour la santé humaine
Pour le lecteur non spécialiste, le message principal est que la réponse immunitaire maternelle — pas seulement l’infection elle-même — peut laisser des « notes en marge » durables dans le manuel d’instructions du cerveau en développement. Ces annotations épigénétiques, écrites avant et peu après la naissance, peuvent modifier subtilement la façon dont les cellules cérébrales croissent et communiquent dans des circuits qui contrôlent la pensée, l’humeur et le comportement. Si la plupart des enfants de mères malades ne développeront pas de troubles psychiatriques, ce travail aide à comprendre pourquoi certains peuvent être plus vulnérables et souligne l’importance de prévenir et de gérer les infections et l’inflammation pendant la grossesse et la petite enfance dans une optique de santé cérébrale à long terme.
Citation: Zhu, B., Li, G., Saunders, J.M. et al. Prenatal and postnatal effects of gestational immune activation on synaptic and neurodevelopmental pathways via epigenetic mechanisms. Transl Psychiatry 16, 82 (2026). https://doi.org/10.1038/s41398-026-03884-z
Mots-clés: activation immunitaire maternelle, épigénétique, neurodéveloppement, signalisation synaptique, risque psychiatrique