Clear Sky Science · fr
Imagerie fonctionnelle de l’inhibition de l’acide gras amide hydrolase dans le trouble de stress post-traumatique : un essai clinique randomisé
Pourquoi la chimie du cerveau compte pour la récupération après un traumatisme
Beaucoup de personnes ayant vécu un traumatisme développent un trouble de stress post-traumatique (TSPT), caractérisé par des cauchemars, des réminiscences et une tension permanente. Les traitements les mieux étayés sont des formes de thérapie par la parole qui exposent progressivement les personnes aux souvenirs traumatiques de façon sûre, aidant le cerveau à apprendre que le danger passé n’est plus présent. Les chercheurs ont espéré que l’ajout d’un médicament renforçant les propres substances calmantes, de type cannabinoïde, du cerveau faciliterait cet apprentissage et rendrait la thérapie plus efficace. Cette étude a testé rigoureusement cette idée et a aussi regardé à l’intérieur du cerveau pour voir ce qui se passait réellement.
Une idée prometteuse issue du système cannabinoïde du cerveau
Le corps produit ses propres substances de type cannabis, appelées endocannabinoïdes, qui régulent le stress, la peur et l’apprentissage émotionnel. L’une d’elles, l’anandamide, semble particulièrement importante pour « l’extinction de la peur » — le processus d’apprentissage qu’un signal auparavant menaçant est maintenant sûr. Chez les animaux et les volontaires sains, l’élévation des niveaux d’anandamide améliore cet apprentissage de sécurité et atténue les réponses au stress. Une enzyme clé, l’acide gras amide hydrolase (FAAH), dégrade l’anandamide. Bloquer la FAAH avec un médicament augmente l’anandamide dans l’organisme et, espéraient les chercheurs, dans les régions cérébrales qui contrôlent la peur et l’émotion.
Sur cette base, l’équipe a mené un essai clinique randomisé en double aveugle auprès de 100 adultes atteints de TSPT. Pendant 12 semaines, les participants ont pris soit un médicament bloquant la FAAH soit un placebo, et après 4 semaines ils ont tous commencé un programme de thérapie cognitivo-comportementale délivré par internet (iCBT) axé sur le traumatisme. Des rapports antérieurs sur cet essai ont montré que, contrairement aux attentes, l’inhibiteur de la FAAH n’a pas réduit les symptômes du TSPT plus que le placebo au cours du traitement. L’article présent fouille les scanners cérébraux pour se demander : au moins le médicament a-t-il modifié l’activité cérébrale ou la communication entre des zones clés de l’émotion, même si les symptômes ne se sont pas améliorés ?
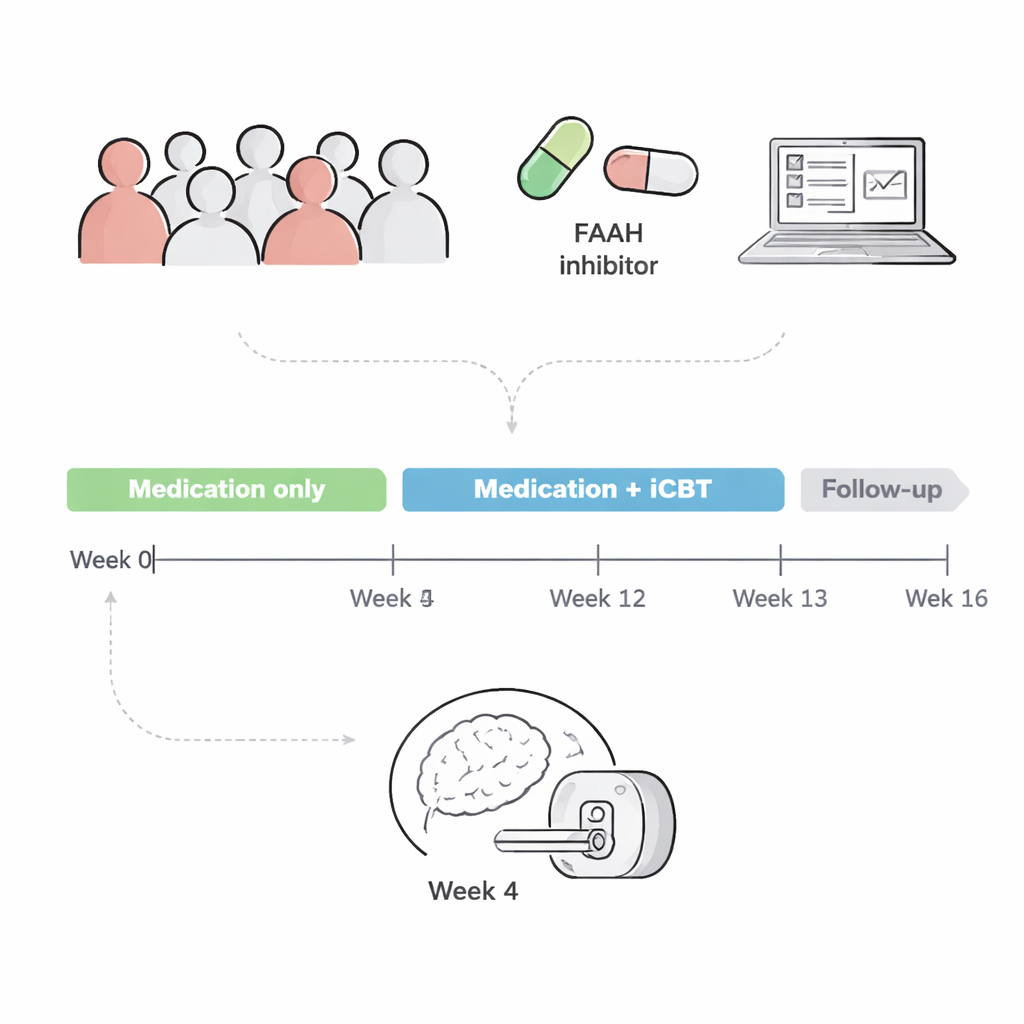
Observer le cerveau au repos et en situation émotionnelle
Soixante-seize participants ont passé une IRM fonctionnelle après 4 semaines de prise de médicament ou de placebo, juste avant de commencer la thérapie. Les chercheurs ont recueilli deux types de données cérébrales. D’abord, une image en « état de repos » a mesuré la force avec laquelle l’activité de différentes régions cérébrales augmentait et diminuait ensemble, signe d’une connectivité fonctionnelle. Ensuite, durant une tâche de « conflit émotionnel », les participants ont vu des visages et des mots émotionnels qui parfois concordaient et parfois s’affrontaient, une version émotionnelle d’un test de Stroop. Cette tâche a déjà été liée à la qualité de la réponse à la thérapie du TSPT.
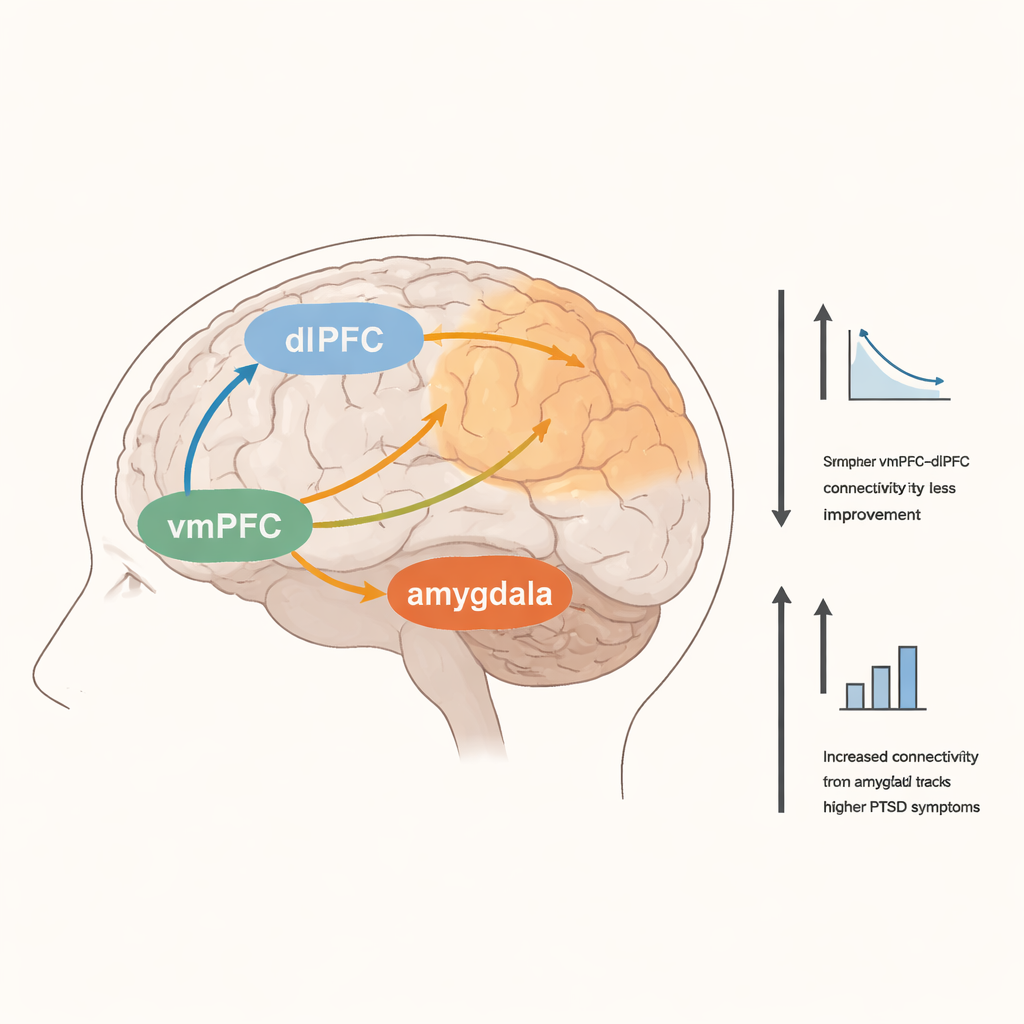
L’équipe s’est concentrée sur un réseau longuement impliqué dans le TSPT : l’amygdale, qui détecte la menace et la saillance émotionnelle ; le cortex préfrontal ventromédial (vmPFC), impliqué dans l’apprentissage de la sécurité et la régulation émotionnelle ; et le cortex préfrontal dorsolatéral (dlPFC), associé au contrôle effortful et aux stratégies d’adaptation. Ils ont également examiné une zone appelée l’insula antérieure, qui aide à intégrer les sensations corporelles avec les états émotionnels. En reliant les mesures cérébrales aux symptômes évalués par le clinicien et aux auto-évaluations des patients, les chercheurs ont recherché des motifs susceptibles de distinguer les personnes ayant le plus progressé durant l’essai.
Ce qui a changé dans le cerveau — et ce qui n’a pas changé
Le médicament bloquant la FAAH a clairement fait son effet biochimique : les niveaux sanguins d’anandamide étaient plus élevés chez les personnes qui l’avaient reçu. Pourtant, lorsque l’équipe a comparé les groupes médicament et placebo, elle n’a trouvé aucune différence significative dans la connectivité au repos ni dans l’activation cérébrale liée à la tâche. Le renforcement espéré des circuits de la peur et de l’émotion n’est simplement pas apparu dans les scanners. À la place, d’autres schémas sont apparus, liés à la gravité des symptômes et au degré d’amélioration au fil du temps, indépendamment de la pilule prise.
Les personnes rapportant des symptômes de TSPT plus sévères au moment de l’examen présentaient des connexions fonctionnelles plus fortes entre le vmPFC et des régions cérébrales étendues liées à l’attention, et entre l’amygdale et des zones impliquées dans la perception et le mouvement du corps. Des liens plus forts entre le vmPFC et l’insula antérieure étaient également associés à des symptômes auto-déclarés plus élevés. Fait intéressant, une meilleure amélioration clinique sur l’ensemble des 12 semaines était liée à une activation plus faible du dlPFC droit durant la tâche de conflit émotionnel, et à une connectivité au repos plus faible entre le vmPFC et cette même région du dlPFC. Cela suggère que les patients qui ont finalement mieux répondu pourraient s’être appuyés moins sur un contrôle effortful de haut niveau et davantage sur d’autres formes de traitement émotionnel, peut‑être plus automatiques.
Ce que cela signifie pour les futurs traitements du TSPT
La conclusion principale, en termes concrets, est que l’augmentation d’un des produits cannabinoïdes endogènes du cerveau, l’anandamide, n’a pas suffi à améliorer la thérapie ni à remodeler les circuits clés de la peur et de l’émotion chez des personnes atteintes de TSPT, du moins dans cet échantillon majoritairement féminin et non issu du combat. L’étude met néanmoins en lumière le dlPFC comme possible marqueur de ceux plus susceptibles de bénéficier d’une thérapie d’exposition, et souligne que le TSPT implique des changements étendus dans la façon dont les réseaux d’émotion et d’attention communiquent entre eux. Pour les patients et les cliniciens, ces résultats rappellent que des idées prometteuses provenant d’études animales et d’études humaines précoces ne se traduisent pas toujours directement en traitements efficaces, et que la compréhension de la réponse cérébrale complexe au traumatisme exigera de regarder au‑delà d’un seul produit chimique, vers des schémas cérébraux globaux et des différences individuelles.
Citation: Tansey, R., Perini, I., Petrie, G.N. et al. Functional neuroimaging of fatty acid amide hydrolase inhibition in posttraumatic stress disorder: a randomized clinical trial. Transl Psychiatry 16, 95 (2026). https://doi.org/10.1038/s41398-026-03864-3
Mots-clés: TSPT, endocannabinoïde, inhibiteur de la FAAH, IRM fonctionnelle, extinction de la peur