Clear Sky Science · fr
Bases biologiques et prédisposition génétique à la schizophrénie au sein des voies régulatrices de la microARN-137 pendant le développement cérébral
Comment une petite molécule peut façonner le risque de schizophrénie
La schizophrénie est souvent perçue comme un trouble cérébral mystérieux qui survient à la fin de l’adolescence ou au début de l’âge adulte, mais ses racines peuvent remonter avant la naissance. Cet article examine comment une petite molécule régulatrice, appelée microARN-137 (miR-137), peut influencer le développement et la communication des cellules cérébrales, modifiant à la fois la probabilité de développer une schizophrénie et les types de symptômes observés. En retraçant les effets de la miR-137 du cerveau prénatal à l’âge adulte, les chercheurs visent à clarifier pourquoi certains individus sont plus vulnérables à la psychose et aux troubles mentaux connexes.
Un petit régulateur à grande influence
La miR-137 est un court fragment d’ARN qui ne code pas lui-même pour des protéines, mais agit comme un réglage fin d’autres gènes. Il aide à déterminer quand et avec quelle intensité de nombreux gènes liés au cerveau sont activés ou réprimés. Des études génétiques antérieures ont montré que des variants courants proches du gène MIR137 sont parmi les facteurs de risque connus les plus forts pour la schizophrénie. Beaucoup des gènes sous le contrôle de la miR-137 participent à la construction des neurones, au façonnage de leurs ramifications et à la formation des synapses — les jonctions par lesquelles les cellules cérébrales communiquent. Toutefois, la plupart des travaux précédents reposaient sur des prédictions informatiques ou des modèles cellulaires simplifiés, qui peuvent passer à côté du fait que la miR-137 peut agir différemment aux divers stades du développement cérébral et selon les régions du cerveau.
Regarder directement dans le cerveau humain
Pour obtenir une image plus réaliste, les auteurs se sont concentrés sur les « cibles directes » de la miR-137 identifiées dans de vrais tissus cérébraux humains à l’aide d’une méthode qui cartographie physiquement où les microARN se lient à leurs gènes partenaires. Ils ont combiné des données de deux périodes clés : le début du développement prénatal et l’âge adulte. Cela leur a permis de constituer deux ensembles de gènes distincts : un groupe de cibles prénatales et un groupe de cibles adultes. Ils ont ensuite comparé ces ensembles à plusieurs jeux de gènes plus traditionnels dérivés d’outils de prédiction informatique ou de manipulations cellulaires en laboratoire. À l’aide d’une série de méthodes statistiques, ils ont examiné comment chaque ensemble de gènes s’exprimait selon les régions cérébrales et les étapes de la vie, dans quels types cellulaires il apparaissait, et dans quelle mesure il chevauchait le risque génétique pour la schizophrénie et des affections apparentées.
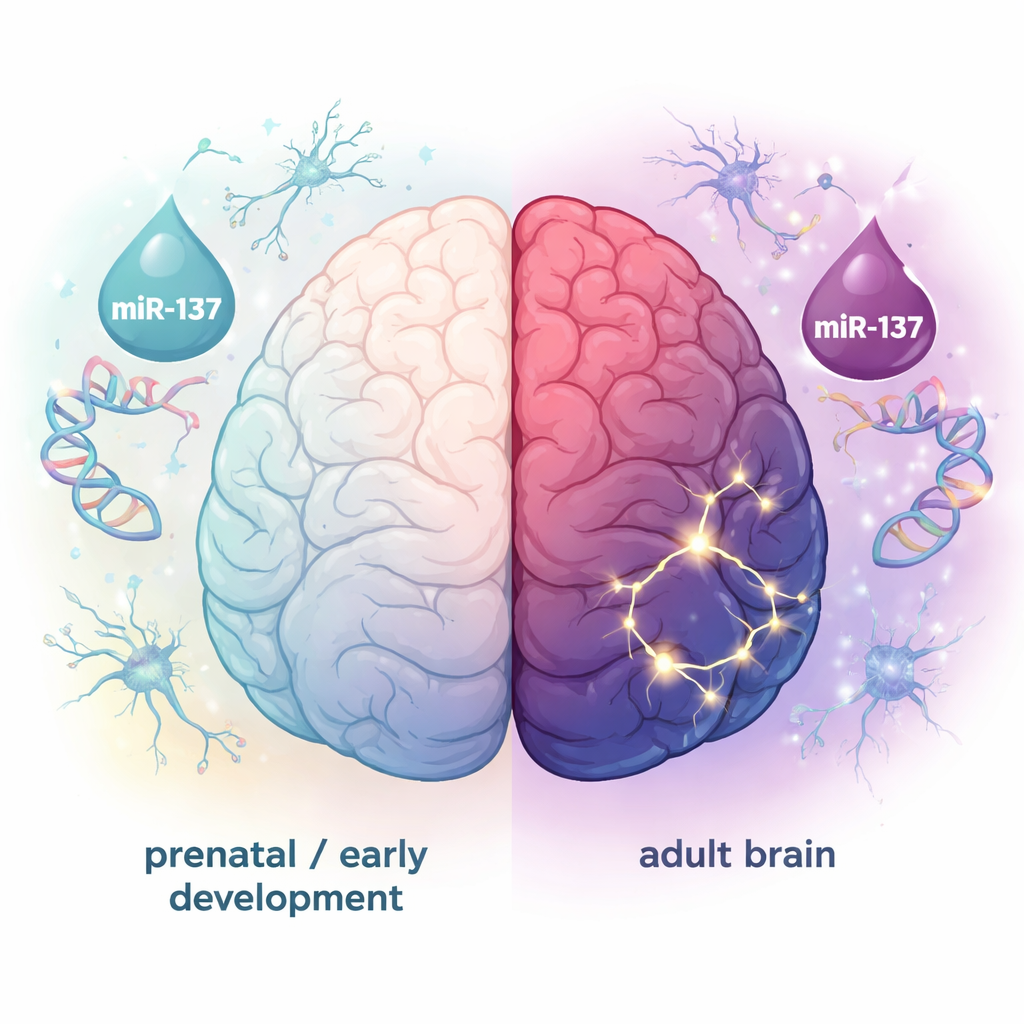
Des stades différents, des fonctions cérébrales différentes
Les groupes de cibles prénatales et adultes de la miR-137 se sont révélés largement distincts, ne partageant qu’une poignée de gènes. Les cibles prénatales étaient fortement liées aux tâches de construction précoce du cerveau, comme la génération de nouveaux neurones et cellules gliales et l’orientation de leur développement initial. Leur activité était relativement élevée tôt dans la vie puis décline, avec une exception notable dans le cervelet adulte. En revanche, les cibles adultes étaient enrichies en gènes impliqués dans les synapses, les prolongements neuronaux et la communication intercellulaire. Ces gènes étaient fortement actifs dans de nombreuses régions cérébrales adultes, en particulier dans les neurones et les oligodendrocytes, et leur expression avait tendance à culminer au début de l’âge adulte — précisément la période où la schizophrénie apparaît souvent pour la première fois. D’autres ensembles de gènes prédits de manière plus large n’affichaient pas ce schéma clair, spécifique au développement et au type cellulaire.
Relier la régulation génique à la maladie et aux symptômes
Lorsque l’équipe a comparé des personnes atteintes de schizophrénie à des individus non affectés, elle a constaté que de nombreux gènes cibles adultes de la miR-137 étaient systématiquement moins actifs dans les tissus cérébraux des patients. Des baisses similaires ont été observées dans le trouble bipolaire et l’autisme, suggérant une signature moléculaire partagée entre les grandes maladies psychiatriques. Les analyses génétiques ont corroboré ce schéma : tant les cibles prénatales qu’adultes de la miR-137 portaient une charge inhabituellement élevée de variants de risque communs pour la schizophrénie, et les cibles adultes captaient également un risque génétique partagé entre la schizophrénie, le trouble bipolaire, la dépression et l’autisme. Fait important, lorsque les chercheurs ont calculé des scores polygéniques limités à ces gènes cibles dans un large échantillon espagnol, les scores basés sur les cibles adultes aidaient à distinguer les patients des témoins, tandis que les scores basés sur les cibles prénatales étaient particulièrement liés à la sévérité des symptômes « négatifs », tels que l’émoussement affectif, le manque de motivation et le retrait social.
Ce que cela signifie pour la compréhension de la schizophrénie
Pour les non-spécialistes, le message principal est que la miR-137 n’agit pas comme un simple interrupteur marche/arrêt pour la schizophrénie, mais comme un panneau de contrôle en mouvement dont l’influence évolue de la vie prénatale à l’âge adulte. Au début du développement, la miR-137 semble façonner la disposition de base des circuits cérébraux, et la variation héritée dans ses cibles prénatales peut prédisposer certains individus à des symptômes négatifs plus sévères plus tard. Dans le cerveau adulte, les cibles de la miR-137 se regroupent dans les synapses et les voies de communication qui sont génétiquement partagées entre plusieurs troubles psychiatriques. En se concentrant sur des cibles directes et spécifiques au moment étudié dans des tissus cérébraux humains, ce travail affine notre compréhension de la manière dont une voie régulatrice unique peut contribuer à la fois au risque de psychose et à la façon particulière dont celle-ci se manifeste, ouvrant des pistes pour des stratégies de prévention et de traitement plus ciblées.
Citation: Stella, C., De Hoyos, L., Mora, A. et al. Biological underpinnings and genetic predisposition to schizophrenia within microrna-137 regulatory pathways across brain development. Transl Psychiatry 16, 91 (2026). https://doi.org/10.1038/s41398-026-03859-0
Mots-clés: schizophrénie, microARN-137, développement cérébral, risque génétique, fonction synaptique