Clear Sky Science · fr
La modification m6A médiée par METTL3 régule CDKN1A pour atténuer les déficits cognitifs et l’apoptose neuronale induits par une privation de sommeil chronique chez le rat
Pourquoi les nuits blanches peuvent nuire à votre mémoire
Beaucoup considèrent la perte de sommeil chronique comme un élément normal de la vie moderne, mais la science montre que le manque de sommeil peut endommager en silence les zones cérébrales impliquées dans l’apprentissage et la mémoire. Cette étude chez le rat explore les mécanismes moléculaires au sein des neurones de l’hippocampe et identifie un interrupteur chimique spécifique — appelé METTL3 — qui semble protéger les cellules cérébrales des effets néfastes de la privation de sommeil chronique. Comprendre ce mécanisme pourrait à terme orienter vers de nouvelles stratégies pour préserver la mémoire chez les personnes qui ne peuvent pas facilement éviter le manque de sommeil, comme les travailleurs postés, les aidants et les patients souffrant de troubles du sommeil.
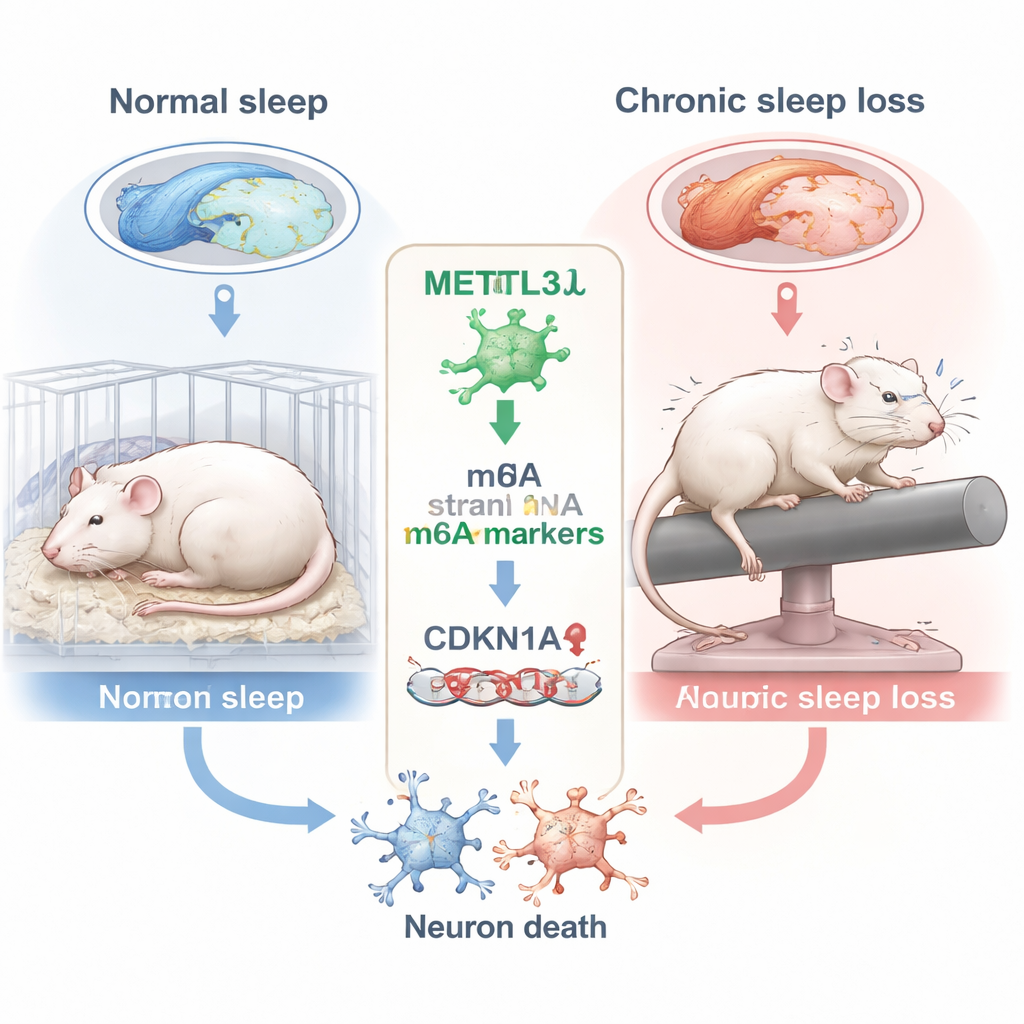
Comment la privation prolongée endommage le centre de la mémoire
Les chercheurs se sont concentrés sur l’hippocampe, une région cérébrale en forme d’hippocampe essentielle à la formation de nouveaux souvenirs. Dans l’hippocampe, ils ont ciblé une sous-région appelée CA3, qui participe au codage et à la récupération d’informations spatiales — des compétences évaluées par des tâches comme la recherche d’une plateforme cachée dans l’eau. Les rats ont été maintenus éveillés 10 heures par jour pendant six semaines à l’aide d’une barre rotative douce qui les poussait à se réveiller. Lors des tests dans le célèbre labyrinthe aquatique de Morris, les rats privés de sommeil empruntaient des trajectoires moins directes, traversaient moins souvent l’emplacement de l’ancienne plateforme et passaient moins de temps dans le quadrant cible, autant de signes d’altération de la mémoire spatiale par rapport aux animaux bien reposés.
Une marque chimique sur l’ARN qui disparaît
Pour comprendre ce qui se passait dans les neurones de CA3, l’équipe a analysé une étiquette chimique sur l’ARN appelée m6A, l’une des marques internes les plus fréquentes sur l’ARN messager. Ces marques contribuent à contrôler la durée de vie des molécules d’ARN et leur efficacité à produire des protéines. Une enzyme clé qui ajoute les marques m6A est METTL3. Grâce au séquençage m6A à haut débit et à l’analyse de l’expression génique, les scientifiques ont constaté que la privation de sommeil chronique réduisait significativement METTL3 dans la région CA3. Cette diminution a été confirmée aux niveaux ARN et protéique. Le profil des gènes affectés suggérait des perturbations du contrôle du cycle cellulaire et des réponses au stress, laissant penser que la perte de sommeil pourrait pousser les neurones vers des états physiologiques défavorables.
Du changement moléculaire à la mort neuronale
Pour évaluer l’effet direct d’un METTL3 diminué sur les neurones, les chercheurs ont travaillé sur des cellules hippocampiques murines en culture. Lorsqu’ils ont utilisé de petits ARN interférents pour silencer METTL3, les cellules sont devenues beaucoup plus vulnérables à un traitement dommageable par la rapamycine, un médicament qui stresse les neurones. Ces cellules appauvries en METTL3 ont montré des niveaux plus élevés de protéines classiques de la « mort cellulaire » comme Bax et la caspase-3 clivée, et davantage de cellules ont été identifiées comme apoptotiques par cytométrie en flux. Des analyses ARN plus approfondies ont mis en évidence un gène unique, CDKN1A (codant pour la protéine p21), comme acteur clé : lorsque METTL3 était réduit, les niveaux de CDKN1A augmentaient fortement.
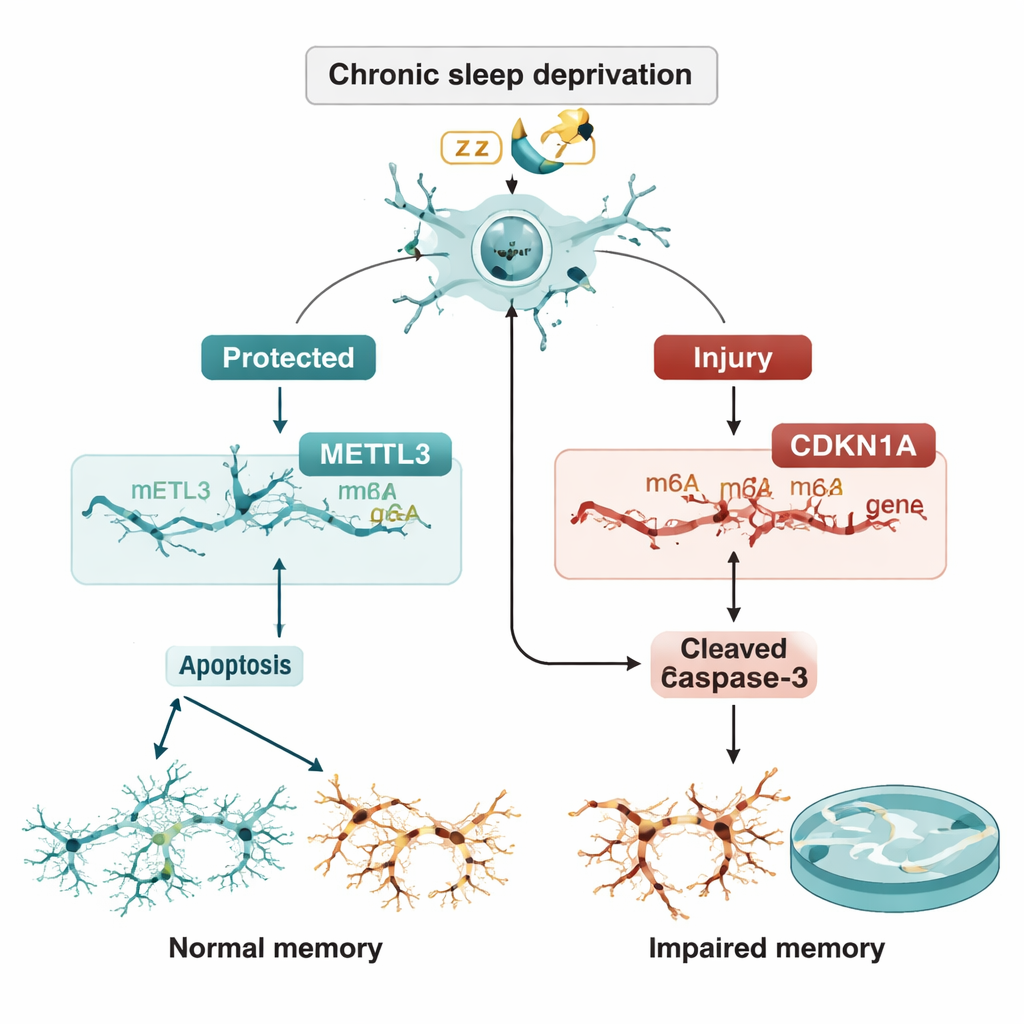
Un équilibre fragile entre protection et autodestruction
L’équipe a ensuite demandé si METTL3 contrôlait CDKN1A via le marquage m6A. Ils ont montré que la réduction de METTL3 diminuait les marques m6A sur l’ARN de CDKN1A et rendait cet ARN plus stable, de sorte que son abondance augmentait au lieu d’être dégradée. L’augmentation de CDKN1A, à son tour, poussait les neurones vers l’apoptose. De manière cruciale, lorsque CDKN1A lui-même était silencieux, l’excès de mort cellulaire induit par la perte de METTL3 était en grande partie rétabli. Chez des rats vivants, l’administration de METTL3 supplémentaires directement dans la région CA3 via un vecteur viral a réduit les niveaux de CDKN1A, diminué l’abondance des protéines d’apoptose, préservé la structure neuronale à l’histologie et amélioré les performances dans le labyrinthe aquatique malgré la privation de sommeil en cours.
Ce que cela signifie pour les personnes qui dorment peu
En résumé, la privation de sommeil chronique semblerait affaiblir une enzyme protectrice, METTL3, dans un circuit clé de la mémoire du cerveau. Lorsque METTL3 décline, il ne peut plus marquer correctement certains ARN, en particulier celui codant CDKN1A. Cet ARN s’accumule alors, poussant les neurones vers la mort programmée et contribuant aux troubles de la mémoire. En restaurant METTL3, les chercheurs ont pu réduire CDKN1A, limiter la perte neuronale et rétablir la mémoire chez des rats privés de sommeil. Bien que ces travaux en soient encore au stade animal, ils identifient la voie METTL3–CDKN1A comme une cible prometteuse pour de futurs traitements visant à protéger le cerveau des conséquences cognitives de la privation de sommeil chronique.
Citation: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
Mots-clés: privation de sommeil chronique, hippocampe, méthylation de l’ARN, apoptose neuronale, déficit de mémoire