Clear Sky Science · fr
Rôles divers et dépendants du lieu de PlexinA2, PlexinA4 et NCAM dans le développement des fibres mousseuses de l’hippocampe
Comment les voies nerveuses façonnent les circuits de la mémoire
L’hippocampe, une région cérébrale essentielle à la formation et à la récupération des souvenirs, est câblé par de minuscules fibres nerveuses qui doivent guider leur croissance avec précision pendant les premiers stades de la vie. Cette étude pose une question apparemment simple : comment ces fibres en croissance savent-elles exactement où aller — et que se passe-t-il lorsque leur système de guidage déraille, contribuant potentiellement à des affections telles que la schizophrénie, l’autisme ou l’épilepsie ?
Deux autoroutes vers le centre de la mémoire
Dans l’hippocampe, des neurones d’une région appelée gyrus denté envoient de longues fibres, appelées fibres mousseuses, vers une autre région nommée CA3. En entrant dans CA3, ces fibres se divisent normalement en deux « autoroutes » distinctes : l’une circule au-dessus d’une couche de corps cellulaires des neurones de CA3 et l’autre en dessous. Chaque autoroute se connecte à différentes parties des cellules de CA3 et contribue à établir l’équilibre d’activité dans ce circuit mnésique. Si ces voies ne se séparent pas correctement, des fibres peuvent aboutir au mauvais endroit, perturbant potentiellement le flux d’information à travers l’hippocampe.
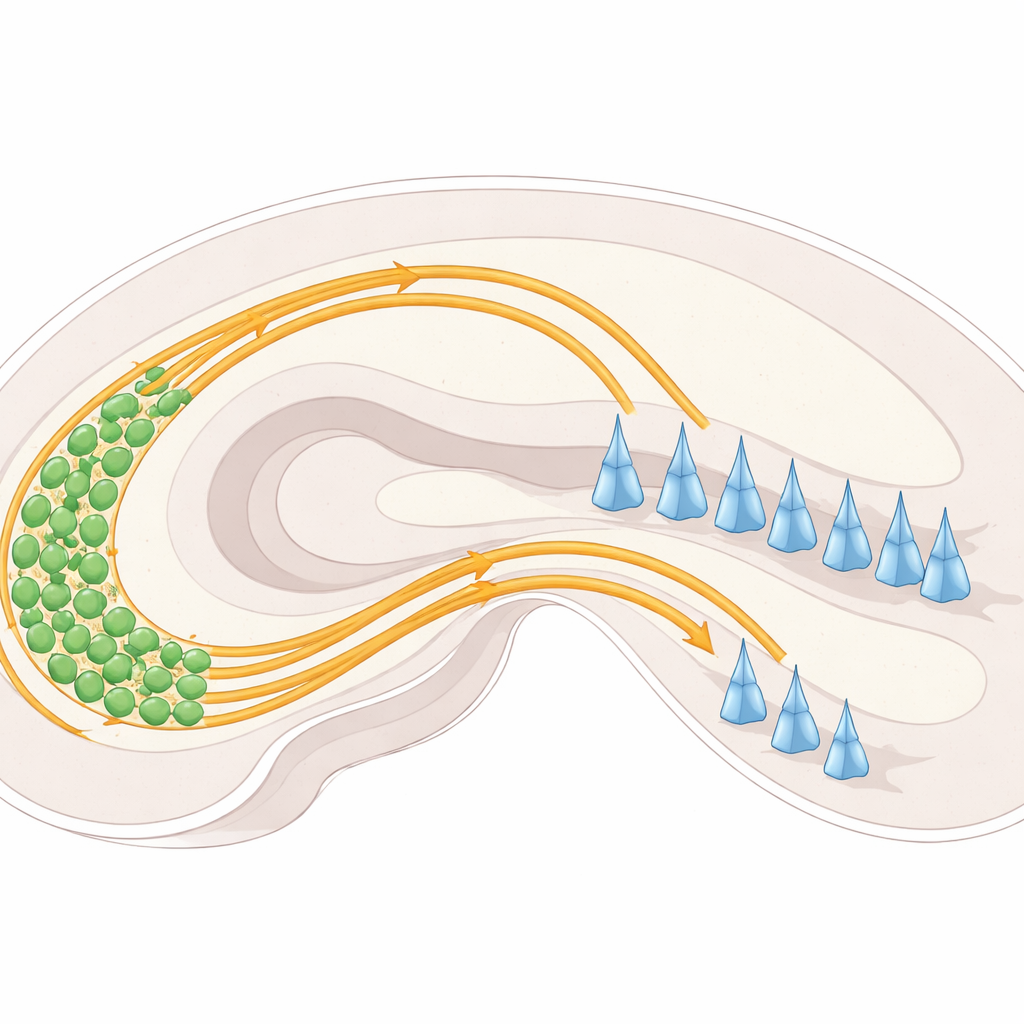
Indices de guidage : répulsions, attractions et adhérences cellule à cellule
Les chercheurs se sont concentrés sur un ensemble de panneaux moléculaires et de « poignées » à la surface des neurones qui orientent les fibres mousseuses. Une famille de protéines appelées plexines (PlexinA2 et PlexinA4) est située à la surface des neurones et répond à des partenaires appelés sémaphorines, en particulier Sema6A. Ces interactions peuvent agir comme des signaux « interdiction d’entrer », repoussant les fibres loin de certaines régions, ou affiner la façon dont les fibres voisines s’agrègent. Une autre protéine de surface, NCAM, fonctionne davantage comme du velcro, favorisant l’adhésion et aidant les faisceaux de fibres à rester cohérents. En examinant où ces protéines sont exprimées et ce qui arrive lorsqu’elles sont supprimées ou modifiées chez la souris, l’équipe a cartographié leur coopération dans des cerveaux vivants plutôt que dans des cellules isolées.
Dissection des rôles avec des souris conçues
Pour démêler le rôle de chaque composant, les scientifiques ont créé et combiné 27 lignées de souris différentes. Certaines étaient dépourvues de Sema6A, d’autres manquaient de PlexinA2 ou de PlexinA4, et d’autres portaient des mutations ponctuelles subtiles qui désactivaient uniquement un « noyau enzymatique » spécifique au sein des plexines tout en laissant le reste de la molécule intact. Ils ont aussi retiré sélectivement Sema6A ou NCAM uniquement de certains types cellulaires, comme les cellules granuleuses du gyrus denté, pour tester où le signal comptait vraiment. Chez les souris dépourvues de Sema6A dans ces cellules granuleuses, les fibres mousseuses ne se séparaient pas proprement en faisceaux supérieurs et inférieurs et le faisceau inférieur poussait trop, dépassant son point d’arrêt normal. Des anomalies de câblage similaires mais non identiques sont apparues chez les souris déficientes en PlexinA2 ou PlexinA4, révélant que ces protéines agissent à des points de contrôle distincts le long d’un même cheminement.
Approfondir les mécanismes et les partenariats
Lorsque les auteurs ont désactivé le cœur catalytique de PlexinA4, beaucoup — mais pas toutes — des mêmes défauts observés chez les souris knockout complètes de PlexinA4 sont réapparus. Cela montre que PlexinA4 s’appuie souvent sur ce noyau pour remodeler le squelette interne des fibres nerveuses en croissance, les aidant à s’agréger correctement et à s’arrêter à la couche adéquate. PlexinA2 s’est avérée différente : certains de ses rôles dépendaient de son cœur catalytique, tandis que d’autres n’en dépendaient pas, indiquant des voies de signalisation supplémentaires indépendantes de l’enzyme. L’équipe a ensuite utilisé une technique de marquage de proximité pour identifier les protéines voisines autour de PlexinA2 sur des jeunes neurones hippocampiques. Plusieurs molécules d’adhésion cellulaire sont apparues, NCAM se distinguant. D’un point de vue génétique, la réduction conjointe de PlexinA2 et de NCAM produisait un mauvais guidage des fibres mousseuses plus marqué que la réduction de l’un ou de l’autre seul, montrant que ces deux systèmes collaborent : NCAM apporte l’adhésion, tandis que la répulsion issue de PlexinA2 calibre la séparation en voies supérieure et inférieure et l’extension du trajet inférieur.
Quand les signaux fonctionnent en sens inverse
Fait intrigant, Sema6A n’agit pas uniquement comme un « panneau » extérieur que lisent les plexines ; elle peut aussi jouer le rôle de récepteur sur les fibres mousseuses elles-mêmes. Les chercheurs ont étudié des souris chez lesquelles la queue interne de Sema6A avait été supprimée tandis que sa portion externe restait intacte. Chez ces animaux, certains défauts de guidage persistaient — en particulier la croissance excessive du faisceau inférieur — indiquant que des signaux circulant vers l’intérieur via la queue de Sema6A (« signalisation inverse ») sont nécessaires pour l’élagage et le modelage normaux des fibres mousseuses. Ce mode inverse fonctionne probablement en parallèle avec la signalisation plus familière basée sur les plexines, de façon dépendante de l’étape et du lieu.
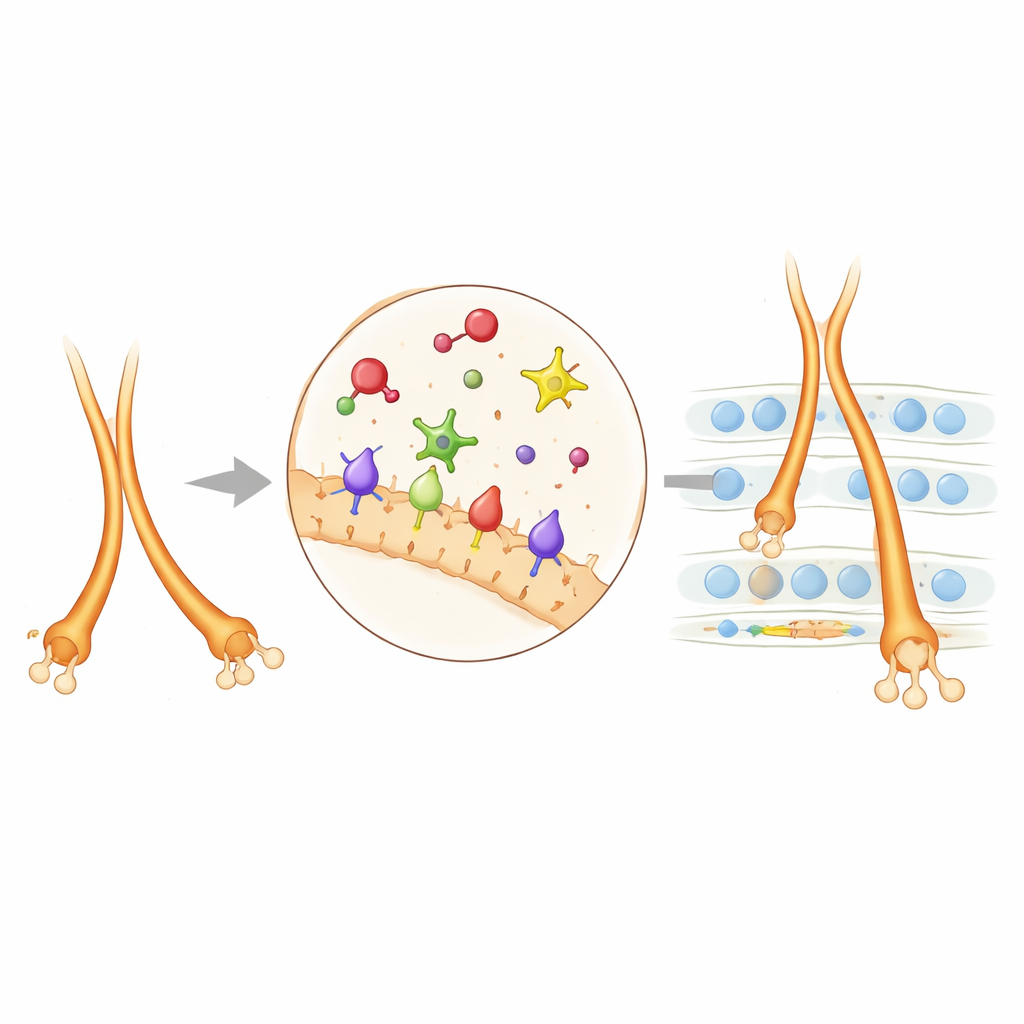
Pourquoi ce câblage importe pour la santé cérébrale
Des mutations dans les versions humaines de PLXNA2, SEMA6A et NCAM1 ont été associées à des troubles du développement neurologique et psychiatriques, depuis la déficience intellectuelle jusqu’à la schizophrénie et l’autisme. En montrant exactement comment ces molécules coopèrent pour sculpter les voies des fibres mousseuses chez la souris, cette étude propose un modèle concret expliquant comment des variations génétiques subtiles pourraient perturber la formation, la séparation et l’élagage de circuits mnésiques clés. En termes courants, le travail suggère que la boîte à outils de guidage du cerveau utilise un mélange minutieusement chronométré de signaux de « pousse », « tire » et « adhérence » pour construire le diagramme de câblage de l’hippocampe — et que même de petites perturbations de cet ensemble peuvent se répercuter sur l’apprentissage, la mémoire et la santé mentale.
Citation: Zhao, XF., Kohen, R., Van Battum, E.Y. et al. Diverse and location-specific roles of PlexinA2, PlexinA4, and NCAM in developing hippocampal mossy fibers. Transl Psychiatry 16, 126 (2026). https://doi.org/10.1038/s41398-026-03846-5
Mots-clés: fibres mousseuses de l’hippocampe, orientation des axones, signalisation sémaphorine-plexine, NCAM et adhésion cellulaire, troubles du développement neurologique