Clear Sky Science · fr
La dysfonction des interneurones GABAergiques sous-tend les oscillations neuronales altérées associées à l’activité épileptoïde chez des souris déficientes en PPT1
Quand les rythmes cérébraux déraillent
Les crises ne sont pas seulement des tempêtes d’activité cérébrale soudaines ; elles résultent souvent de changements subtils dans la manière dont les neurones communiquent. Cette étude examine une maladie cérébrale infantile rare, la maladie CLN1, et pose une question simple aux implications larges : que deviennent les « chefs d’orchestre » internes du cerveau lorsque manque une seule enzyme, la PPT1 ? En suivant ces changements chez la souris au fil du temps, les auteurs montrent comment de petites défaillances précoces de l’inhibition peuvent s’amplifier en crises et en dommages cérébraux étendus.
Les gardiens de l’équilibre cérébral
Notre cerveau repose sur deux grandes catégories de neurones. Les cellules excitatrices, comme les pyramidalaux de l’hippocampe, propagent l’activité. Les cellules inhibitrices, appelées interneurones, font office de freins, limitant cette activité et sculptant les rythmes électriques du cerveau. Parmi elles, deux groupes importants sont les interneurones parvalbumine-positifs (PV+) et somatostatine-positifs (SST+). Ils contribuent à générer et coordonner des ondes cérébrales rythmiques, comme les oscillations thêta et gamma, qui soutiennent des fonctions telles que l’apprentissage et la mémoire. Dans la maladie CLN1, les enfants perdent l’enzyme PPT1, qui enlève normalement des groupes gras sur les protéines. Les auteurs ont utilisé un modèle murin portant la même mutation que chez les patients pour voir comment cette perte affecte les interneurones et les rythmes cérébraux qu’ils aident à contrôler.
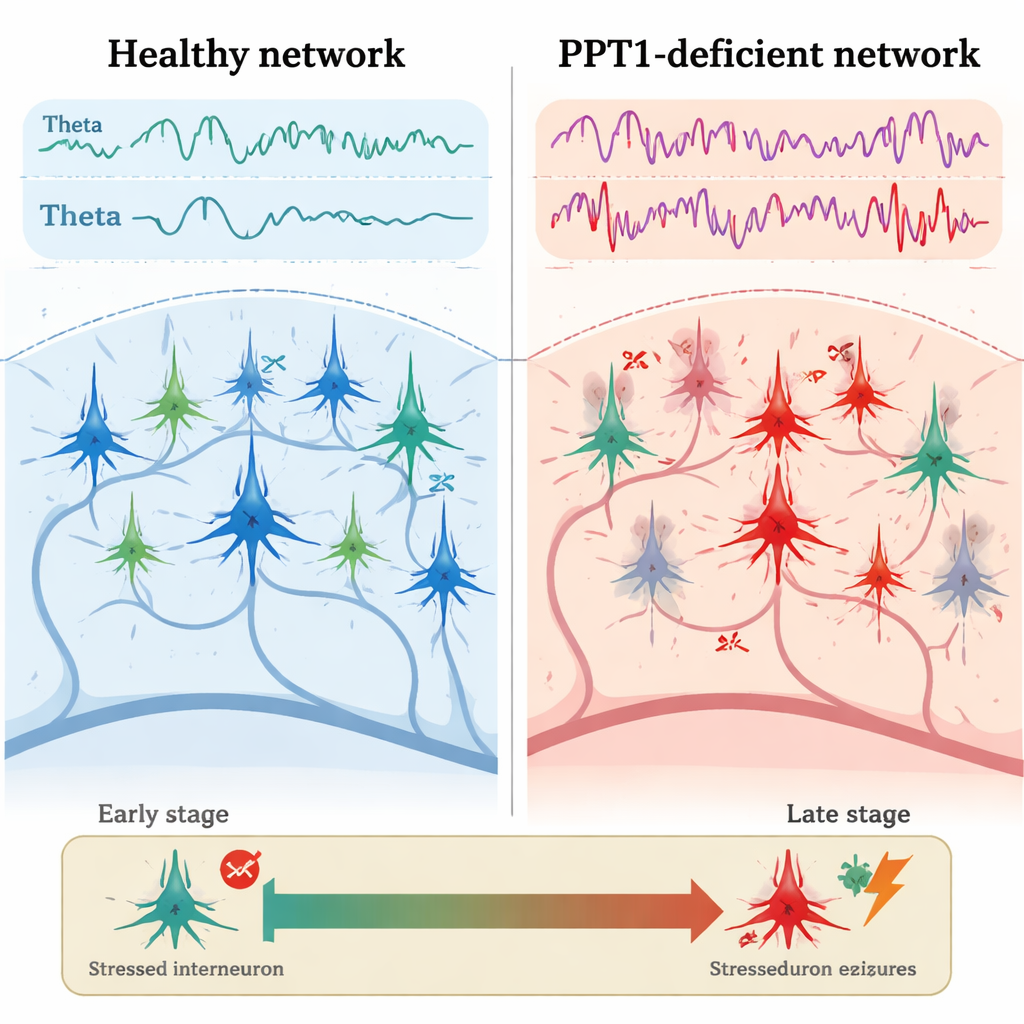
Les premières fissures du système inhibiteur
Chez de jeunes souris mutantes, d’environ trois à quatre mois, le premier problème net est apparu au niveau des interneurones PV+. Des enregistrements électriques de l’hippocampe ont montré que ces cellules inhibitrices tiraient moins fréquemment que chez les souris saines, tandis que les neurones pyramidaux voisins tiraient plus rapidement et avec des pauses entre pics plus courtes. La microscopie a révélé que de nombreux interneurones PV+ avaient activé la caspase-3, un exécuteur clé de la mort cellulaire programmée, même si leur nombre total n’avait pas encore diminué. Parallèlement, la puissance des ondes thêta et gamma était augmentée, et l’imagerie calcique montrait une activité plus forte des neurones hippocampiques lors des déplacements des animaux. De manière cruciale, le « dialogue » habituel entre les rythmes thêta et gamma — où les ondes lentes organisent les plus rapides — était affaibli, suggérant une rupture précoce du timing fin de l’activité réseau.
Des rythmes perturbés aux bouffées épileptiques
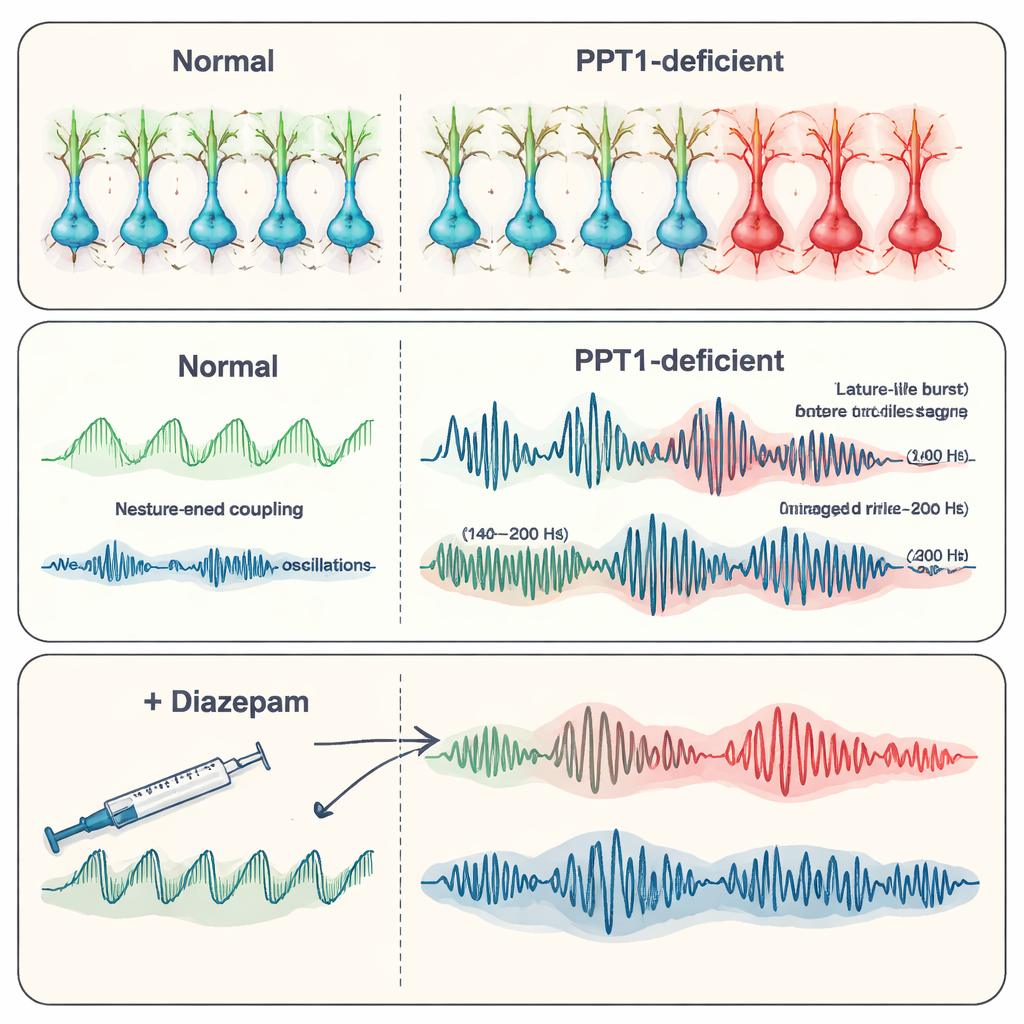
À six-sept mois, la situation s’était aggravée. De nombreux interneurones PV+ avaient été perdus, et les interneurones SST+ montraient désormais aussi des signes d’activation de la caspase-3. Les enregistrements hippocampiques ont révélé des décharges épileptoïdes spontanées — brèves bouffées anormales d’activité associées aux crises. L’équipe s’est intéressée aux « ripples » haute fréquence, des oscillations rapides qui aident normalement au stockage mnésique. Chez les souris mutantes, les ripples physiologiques (environ 140–200 Hz) devinrent moins fréquents mais de plus grande amplitude, tandis que des ripples « pathologiques » encore plus rapides (200–500 Hz), étroitement liés à l’épilepsie, s’intensifièrent et devinrent plus fréquents. Ensemble, ces changements suggèrent un glissement d’oscillations organisées, liées à la mémoire, vers des motifs chaotiques pro-crise à mesure que le contrôle inhibiteur faillait.
Les neurones s’épuisent et le diazépam entre en jeu
À mesure que la maladie progressait, l’hippocampe lui-même a commencé à dégénérer. Les signaux calciques dans les neurones diminuèrent, la coloration de Golgi montra des arbres dendritiques plus fins et moins ramifiés, et il y eut moins de petites épines où se forment les synapses. Le comptage des neurones dans des régions hippocampiques clés (CA1 et CA3) confirma une perte cellulaire étendue, et moins d’unités actives pouvaient être détectées dans les enregistrements électriques. Les chercheurs ont ensuite testé le diazépam, un anticonvulsivant courant qui renforce l’action du neurotransmetteur inhibiteur GABA. Chez les souris mutantes plus âgées, le diazépam réduisit la fréquence des décharges épileptiques et restaura partiellement des schémas oscillatoires plus normaux, y compris le comportement des ripples, même s’il ne réparait pas la perte sous-jacente de récepteurs. Cela suggère que renforcer les signaux inhibiteurs restants peut malgré tout calmer le réseau, au moins temporairement.
Pourquoi ces résultats sont importants
Pour le lecteur non spécialiste, le message principal est que la maladie CLN1 ne se résume pas à une simple accumulation de déchets dans les cellules cérébrales. La perte de PPT1 déclenche une réaction en chaîne : d’abord, des interneurones inhibiteurs spécialisés sont stressés et commencent à faillir, ce qui libère une hyperactivité des neurones pyramidaux et déforme les rythmes cérébraux. Avec le temps, ce déséquilibre conduit à des crises et finalement à une perte à grande échelle de cellules et de connexions cérébrales. L’étude identifie une fenêtre d’intervention précoce, où protéger ou sauver les interneurones PV+ — par exemple en bloquant l’activation des caspases — pourrait prévenir les crises et la dégénérescence ultérieures. Si le diazépam ne guérit pas la CLN1, sa capacité à atténuer les rythmes anormaux dans ce modèle illustre l’idée plus générale selon laquelle restaurer l’inhibition pourrait être une stratégie puissante dans l’épilepsie et les troubles cérébraux connexes.
Citation: Tong, J., Liu, W., Wang, Q. et al. Dysfunction of GABAergic interneurons underlies altered neural network oscillations associated with epileptiform activity in PPT1-deficient mice. Transl Psychiatry 16, 106 (2026). https://doi.org/10.1038/s41398-026-03843-8
Mots-clés: épilepsie, interneurones, hippocampe, oscillations cérébrales, maladie de surcharge lysosomale