Clear Sky Science · fr
Modifications fonctionnelles précoces et GFAP plasmatique dans des familles suédoises porteuses de mutations responsables d’une maladie d’Alzheimer autosomique dominante
Pourquoi cette étude est importante pour les familles
La maladie d’Alzheimer donne souvent l’impression d’apparaître soudainement, mais en réalité des altérations nocives du cerveau s’accumulent silencieusement pendant de nombreuses années. Dans de rares familles porteuses de mutations héritées (« autosomiques dominantes »), les scientifiques peuvent estimer quand les symptômes sont susceptibles de commencer et observer le déroulement de ces changements précoces. Cette étude a suivi des familles suédoises porteuses de telles mutations pour comprendre comment l’utilisation d’énergie par le cerveau, les capacités cognitives et un marqueur sanguin des cellules de soutien cérébrales (GFAP) évoluent bien avant l’apparition des troubles de la mémoire — et comment ces évolutions diffèrent selon les gènes.
Suivre l’horloge de la maladie au sein de familles à haut risque
Parce que les personnes porteuses de la maladie d’Alzheimer autosomique dominante (MAAD) développent en général des symptômes à un âge assez prévisible, les chercheurs peuvent calculer les « années estimées avant l’apparition des symptômes » (EYO) — le nombre d’années qui sépare une personne de l’âge estimé du début des premiers signes. L’équipe a étudié 45 adultes issus de familles suédoises porteuses de mutations des gènes APP ou PSEN1, ainsi que des apparentés non porteurs. Sur en moyenne plus de sept ans, les participants ont subi des examens cérébraux mesurant la consommation de sucre par le cerveau (FDG PET), des tests cognitifs et mnésiques détaillés et, pour un sous-groupe, des analyses sanguines du GFAP, une protéine libérée lorsque les cellules de soutien cérébral appelées astrocytes deviennent réactives. Ce dispositif a permis aux chercheurs d’aligner différentes modifications biologiques le long d’une même chronologie de la maladie plutôt que de comparer des personnes à un seul instant.
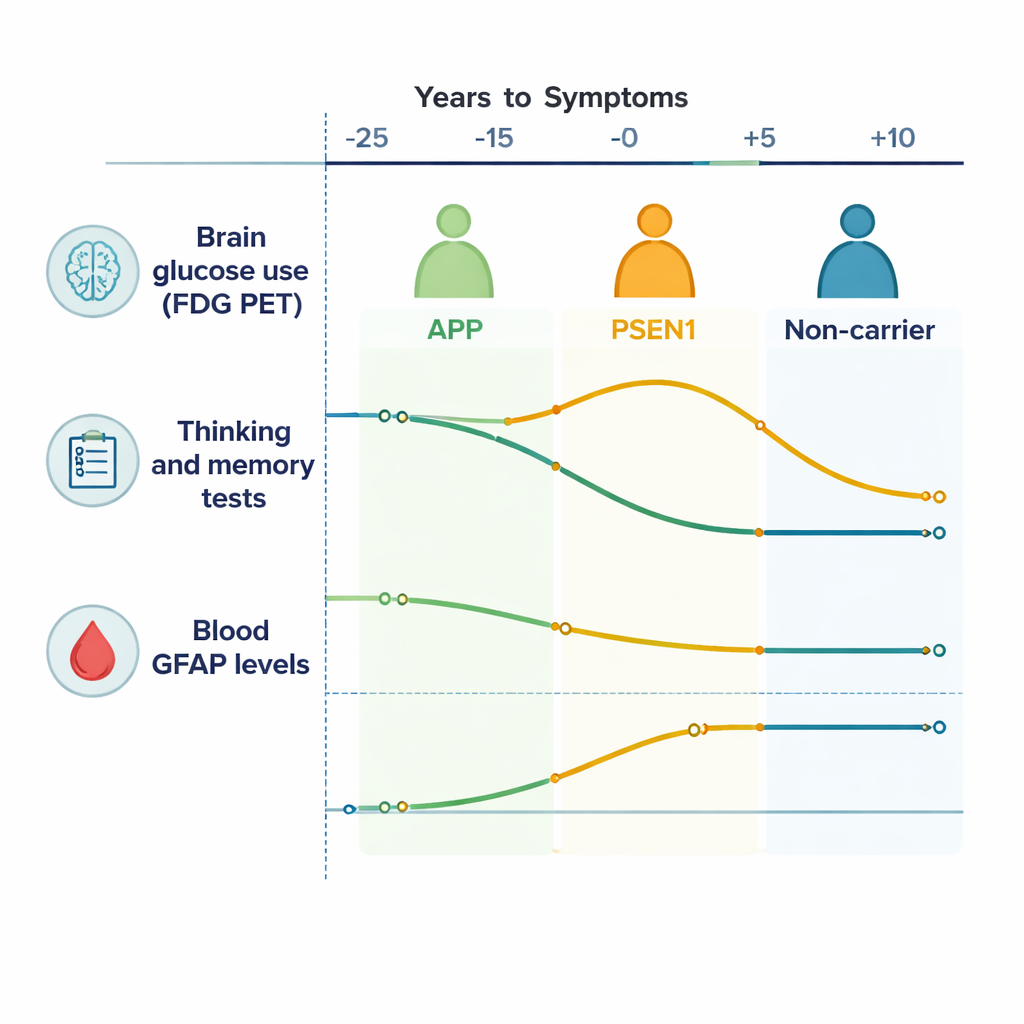
Suivi de l’énergie cérébrale et des fonctions cognitives au fil du temps
À travers les couches externes du cerveau (le cortex), les personnes porteuses de mutations liées à Alzheimer ont montré une diminution progressive du signal FDG PET par rapport aux apparentés non porteurs, ce qui signifie que leur cerveau utilisait moins de glucose au fil du temps — un signe de défaillance des cellules cérébrales. Des régions sous‑corticales profondes, en particulier le noyau caudé et le thalamus, ont également présenté une activité en déclin, surtout chez les porteurs de mutations APP. Les tests cognitifs et mnésiques se sont détériorés dans plusieurs domaines, notamment la mémoire épisodique et la flexibilité mentale, à partir d’environ 10 à 15 ans avant l’âge attendu d’apparition des symptômes. Autrement dit, alors que les personnes se sentaient et fonctionnaient encore normalement dans la vie quotidienne, des tests sensibles et des examens d’imagerie révélaient déjà que leur cerveau travaillait de façon moins efficace.
Des profils différents selon les gènes Alzheimer
Une observation clé est que les deux principaux groupes de mutations — APP et PSEN1 — ne suivent pas des trajectoires identiques. Chez les porteurs de PSEN1, les chercheurs ont observé une période précoce, environ 20 à 10 ans avant l’apparition attendue des symptômes, où certaines régions cérébrales présentaient une consommation de glucose inhabituellement élevée (« hypermétabolisme »), accompagnée d’une meilleure performance aux tests, avant de décliner plus tard. Cela reflète probablement une phase de compensation temporaire, où le cerveau et ses cellules de soutien augmentent leur activité pour faire face à des dommages croissants. Les porteurs d’APP, en revanche, ont montré une baisse plus linéaire et progressive du métabolisme cérébral sans ce pic initial. Ces profils spécifiques aux gènes suggèrent que la « maladie d’Alzheimer » n’est pas une seule histoire biologique, même sous forme héréditaire, mais une famille de processus apparentés qui se déroulent différemment selon la mutation sous‑jacente.
Ce qu’un test sanguin révèle sur le stress cérébral précoce
Le GFAP, mesuré à partir d’un simple prélèvement sanguin, a fourni une fenêtre sur la façon dont les astrocytes réagissent aux premiers changements liés à Alzheimer. Les taux de GFAP avaient tendance à augmenter régulièrement à l’approche de l’âge attendu d’apparition des symptômes, tant chez les porteurs de mutation que chez les non‑porteurs, mais les relations entre GFAP, métabolisme cérébral et fonctions cognitives étaient spécifiques aux gènes. Chez les porteurs d’APP, un taux de GFAP plus élevé était associé à une chute de la consommation de glucose dans des régions profondes du cerveau et à une détérioration des performances sur la plupart des tests cognitifs, ce qui suggère que l’activation des astrocytes est étroitement liée aux dommages précoces et à la perte de fonction. Chez les porteurs de PSEN1, ces liens étaient plus faibles ou absents, ce qui renforce l’idée de voies biologiques distinctes menant au même aboutissement clinique qu’est la démence.
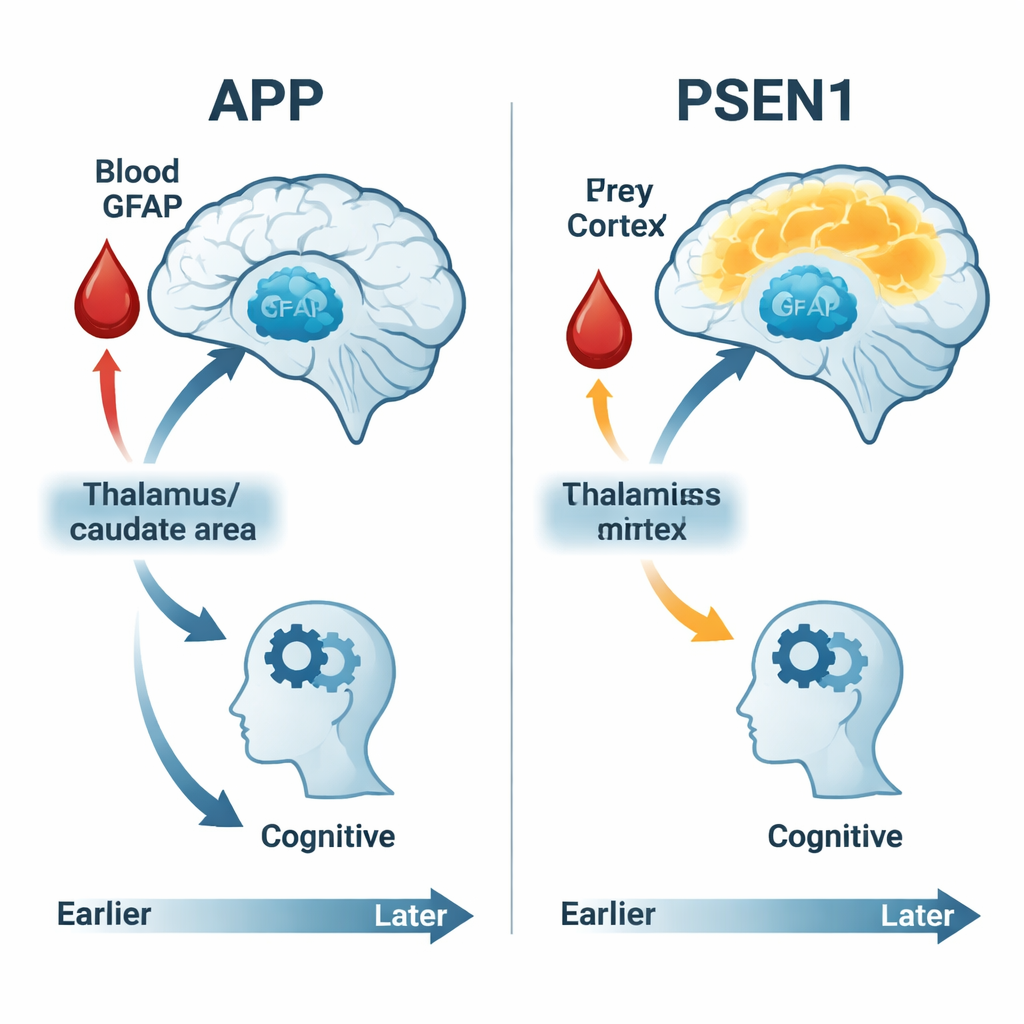
Implications pour la détection précoce et le traitement
Pour un lecteur non spécialiste, le message principal est que, dans ces familles à haut risque, les changements liés à Alzheimer commencent des décennies avant la perte de mémoire évidente — et qu’ils ne se manifestent pas de la même manière chez tout le monde. Les examens du métabolisme du glucose cérébral, des tests cognitifs fins et un marqueur sanguin unique comme le GFAP peuvent ensemble révéler quand le cerveau commence à peiner et à quelle vitesse cette détérioration progresse. Il est important de noter que les personnes porteuses de différentes formes génétiques d’Alzheimer présentent des séquences de modifications distinctes : certaines connaissent une phase précoce d’hyperactivité, d’autres une baisse régulière, et le marqueur sanguin du stress des astrocytes est plus fortement lié aux dommages dans certains groupes que dans d’autres. Reconnaître ces trajectoires distinctes pourrait aider à adapter les futurs médicaments et essais cliniques aux bonnes personnes au bon moment, et renforce le potentiel des tests sanguins comme le GFAP pour détecter la maladie d’Alzheimer plus tôt — avant que les symptômes ne privent les personnes de leur autonomie.
Citation: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Mots-clés: maladie d’Alzheimer autosomique dominante, biomarqueur plasmatique GFAP, métabolisme cérébral du glucose, astrocytes et neurodégénérescence, détection précoce de la maladie d’Alzheimer