Clear Sky Science · fr
Convergence et divergence des gènes éclairées par des variants communs et rares des troubles du spectre autistique dans des voies tissulaires spécifiques et des réseaux de gènes
Pourquoi l’énigme génétique de l’autisme importe
Les familles et les cliniciens savent depuis longtemps que le trouble du spectre autistique (TSA) est très variable : certaines personnes nécessitent un soutien à vie, tandis que d’autres vivent de façon indépendante mais rencontrent des difficultés sociales. Une grande partie de cette diversité provient probablement de la génétique, toutefois le risque est réparti sur des milliers de changements d’ADN, chacun influençant le cerveau et le corps de façon subtile. Cette étude pose une question simple mais importante : comment des mutations rares et puissantes et les nombreux variants communs et plus faibles interagissent-ils dans différents tissus pour façonner l’autisme — et qu’est-ce que cela implique pour la compréhension et le traitement du trouble ?
Deux types d’indices génétiques
Les chercheurs distinguent les variants rares, qui peuvent perturber fortement un gène mais sont présents chez relativement peu de personnes, des variants communs, fréquents dans la population mais généralement d’effet faible. Les variants rares ont été plus faciles à relier à l’autisme dans des familles individuelles, mais ils n’expliquent qu’une petite fraction du risque génétique global. Les variants communs, pris ensemble, rendent compte d’une part bien plus importante de la composante héréditaire de l’autisme, mais l’effet de chacun est minime et facile à négliger. Les auteurs de cet article ont cherché à intégrer à la fois les signaux rares et communs, pour savoir s’ils convergent vers les mêmes systèmes biologiques ou s’ils indiquent des parties différentes du corps et des mécanismes pathologiques distincts.
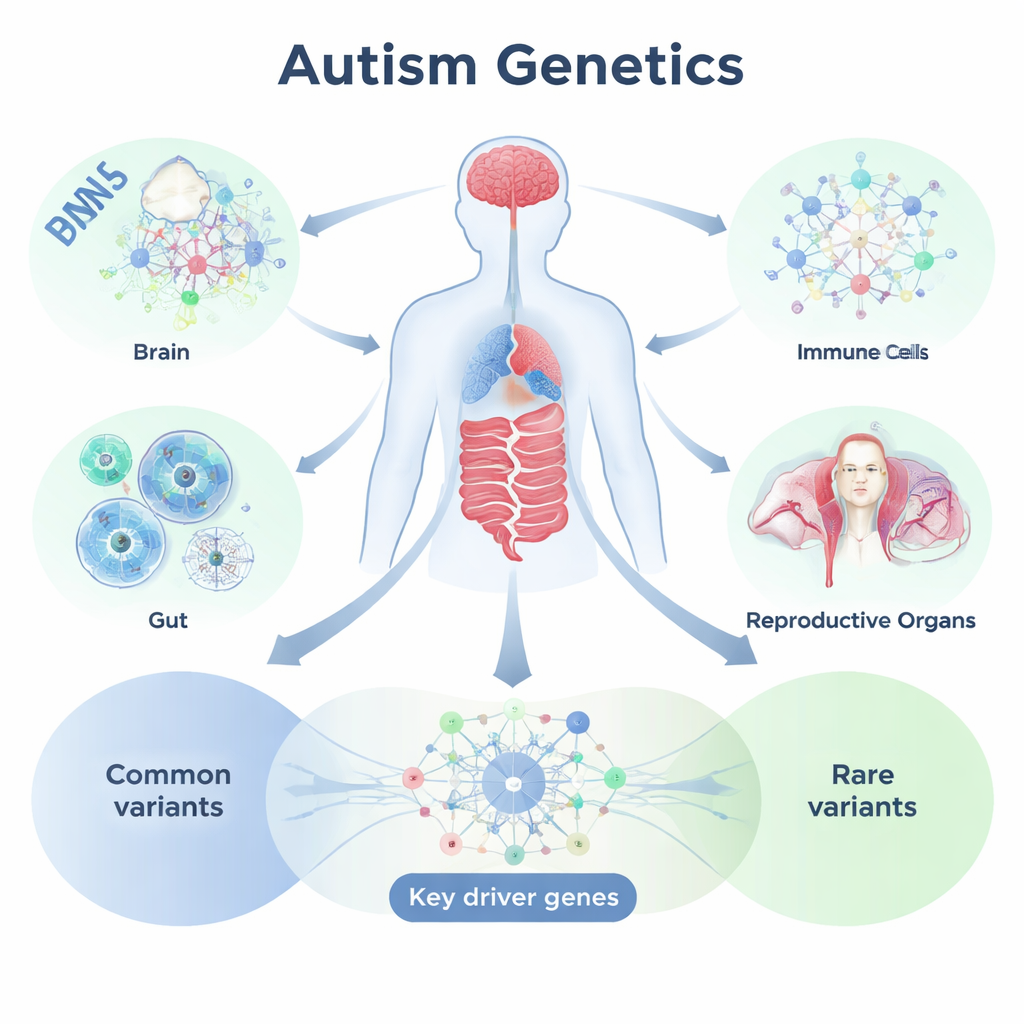
Cartographier les signaux d’ADN sur les tissus et les réseaux
Pour aborder cette question, l’équipe a utilisé un cadre d’analyse nommé Mergeomics, qui combine des études génétiques à grande échelle avec des informations sur la façon dont les gènes sont activés dans des tissus spécifiques. Ils sont partis de données d’association pangénomique portant sur plus de neuf millions de variants d’ADN communs provenant de plus de 18 000 personnes autistes et d’environ 28 000 témoins non autistes. Ils ont ensuite mappé ces variants sur des gènes en s’appuyant sur des données de référence détaillées sur l’activité génétique dans près de 50 tissus, incluant de nombreuses régions cérébrales ainsi que des organes digestifs, immunitaires, reproducteurs et d’autres organes périphériques. En regroupant les gènes qui sont exprimés ensemble dans le même tissu et en examinant à quel point ces groupes de gènes s’alignent avec les variants liés à l’autisme, les chercheurs ont identifié des « modules » tissulaires spécifiques et des réseaux régulateurs qui semblent importants pour le TSA.
Le cerveau et le corps contribuent tous deux
L’analyse a confirmé le rôle central du cerveau — en particulier des régions comme le cortex cingulaire antérieur, l’amygdale, le cortex frontal, le cervelet et des aires corticales plus larges, connus pour être impliqués dans l’émotion, le comportement social, le raisonnement et la coordination. Les réseaux géniques dans ces régions cérébrales étaient riches en variants d’autisme tant communs que rares et étaient liés à la signalisation synaptique, au développement neuronal et au contrôle immunitaire au sein du cerveau. Pourtant, le tableau ne s’est pas limité au crâne. De manière surprenante, de nombreux tissus périphériques, notamment des systèmes digestif, immunitaire, endocrinien et reproducteur, contenaient aussi des modules géniques fortement informés par des variants communs liés à l’autisme. Ces modules étaient associés à des processus tels que les réponses immunitaires, la croissance et la division cellulaires, la production d’énergie, l’épissage de l’ARNm et une voie de contrôle majeure connue sous le nom de mTOR, autant d’éléments impliqués dans le développement cérébral et le comportement.
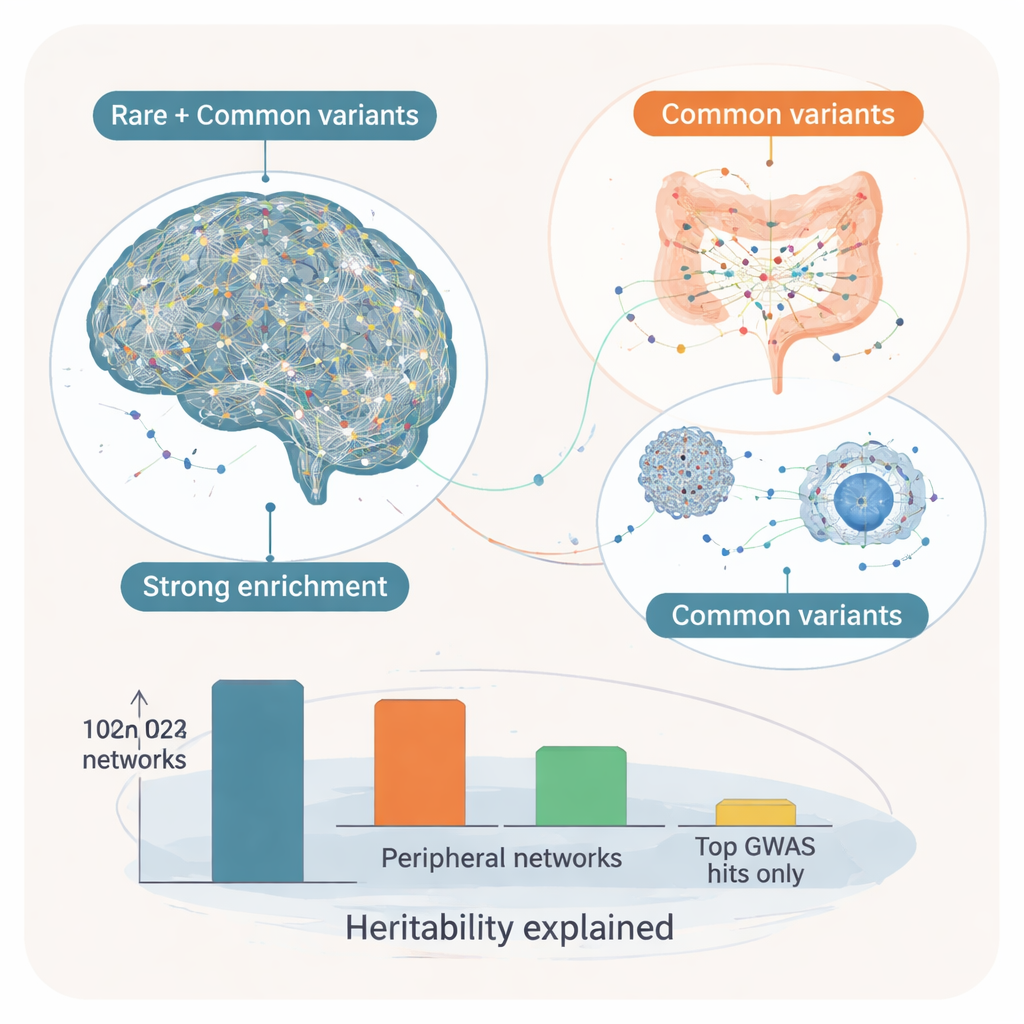
Gènes de contrôle clés et l’idée cœur–modificateur
En intégrant ces modules dans des réseaux régulateurs géniques directionnels, les chercheurs ont ensuite identifié quels gènes occupent des « nœuds » — les soi-disant « drivers clés » qui influencent de nombreux autres gènes. Dans les réseaux cérébraux, ces drivers clés montraient une forte enrichment pour des variants rares à fort impact ainsi que pour des variants communs, suggérant qu’ils forment un ensemble « cœur » de gènes où les deux types de risque convergent. Citons par exemple SYT1, qui aide à contrôler la libération de neurotransmetteurs aux synapses, et ADD2, impliqué dans la structuration et la connectivité des neurones. Leurs réseaux environnants contenaient un mélange de gènes d’autisme rares connus et de cibles de variants communs impliquées dans la communication synaptique et l’excitabilité neuronale. En revanche, les drivers clés dans des tissus périphériques, en particulier digestifs et endocriniens, étaient davantage influencés par les variants communs seuls. Ceux-ci semblent agir comme des « modificateurs », modulant les voies immunitaires, métaboliques et de signalisation qui peuvent façonner la manière dont les vulnérabilités cérébrales centrales se traduisent en symptômes.
Ce que cela signifie pour les personnes et les traitements à venir
Lorsque les auteurs ont estimé quelle part du risque héréditaire de l’autisme pouvait être attribuée à ces réseaux, les modules d’origine cérébrale expliquaient environ 7 % de la composante héréditaire et les modules périphériques environ 3 %, capturant ensemble presque toute l’héritabilité due aux variants communs observée dans l’étude initiale — et bien plus que la fraction minime expliquée par les seuls signaux d’ADN les plus forts. Pour un public non spécialiste, la conclusion est que la génétique de l’autisme suit un schéma à couches : des variants rares et communs convergent sur un ensemble central de réseaux cérébraux essentiels au neurodéveloppement, tandis que des variants communs largement distribués dans l’intestin, le système immunitaire et les tissus hormonaux modifient probablement l’évolution et les manifestations du trouble. Ce cadre cœur–modificateur aide à expliquer pourquoi l’autisme se présente de manière si différente d’une personne à l’autre et suggère que les futures thérapies devront peut-être cibler non seulement le cerveau, mais aussi les systèmes corporels plus larges qui interagissent avec lui.
Citation: Gill, C., Zuo, Y., Ha, D.Sm. et al. Convergence and divergence of genes informed by common and rare variants of autism spectrum disorders in tissue-specific pathways and gene networks. Transl Psychiatry 16, 98 (2026). https://doi.org/10.1038/s41398-026-03824-x
Mots-clés: génétique de l’autisme, variants rares, variants communs, réseaux cérébraux, axe intestin–cerveau