Clear Sky Science · fr
Essai pilote randomisé, en double aveugle et contrôlé par simulation de stimulation transcrânienne par courant alternatif en bande thêta pendant un entraînement cognitif dans la maladie d’Alzheimer légère
Pourquoi cette étude sur la stimulation cérébrale est importante
À mesure que l’espérance de vie augmente, de plus en plus de familles sont touchées par la maladie d’Alzheimer, une affection qui érode lentement la mémoire et l’autonomie. Les médicaments peuvent atténuer certains symptômes, mais leurs bénéfices restent modestes et leurs effets secondaires peuvent s’accumuler avec le temps. Cette étude explore une idée très différente : utiliser de faibles courants électriques appliqués via le cuir chevelu, combinés à des exercices de mémoire ciblés, pour réaligner l’activité cérébrale vers un rythme plus sain et, possiblement, ralentir la dégradation des fonctions cognitives.
Une nouvelle façon d’accorder les rythmes cérébraux
Les chercheurs se sont intéressés à une technique appelée stimulation transcrânienne par courant alternatif, ou tACS. De très faibles courants électriques sont appliqués entre deux électrodes posées sur le front, oscillant à une fréquence déterminée pour « entraîner » ou synchroniser les rythmes cérébraux. Ici, l’équipe a utilisé un signal à 8 Hz, dans la plage dite thêta, qui a été associé à la mémoire et à l’attention. Parallèlement, les patients réalisaient une tâche de type n‑back, un exercice mental qui sollicite la mémoire de travail en demandant de décider si l’image présentée correspond à une image vue peu de temps auparavant. L’idée est que l’association d’une stimulation externe et d’une activité cognitive soutenue pourrait renforcer les circuits cérébraux encore fonctionnels.
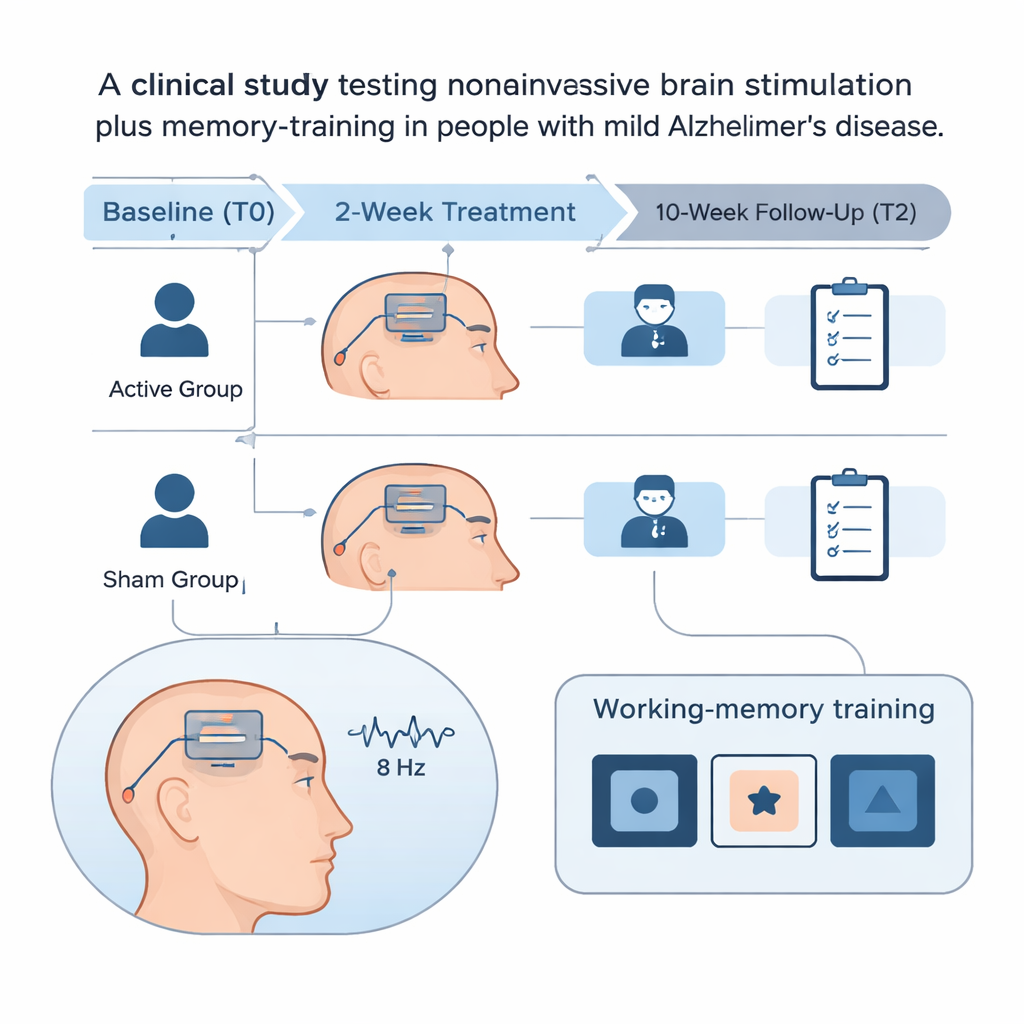
Comment l’essai a été conçu
L’étude a recruté 36 personnes atteintes de la maladie d’Alzheimer légère qui répondaient à des critères diagnostiques stricts et présentaient une atrophie hippocampique sur les examens cérébraux. Les participants ont été assignés au hasard à l’un des deux groupes. Le groupe actif a reçu 20 minutes de véritable tACS en fréquence thêta sur la région frontale pendant qu’ils accomplissaient la tâche n‑back, cinq jours par semaine pendant deux semaines. Le groupe simulé, ou placebo, a ressenti la sensation initiale de picotement de la stimulation mais n’a ensuite reçu aucun courant continu, bien qu’il ait effectué le même entraînement. Ni les patients ni les cliniciens chargés des évaluations ne savaient qui appartenait à quel groupe. Les capacités cognitives, l’humeur et le fonctionnement quotidien ont été mesurés avant le traitement, juste après la période de deux semaines, puis à nouveau 10 semaines plus tard. Des EEG en état de repos, qui enregistrent l’activité électrique naturelle du cerveau, ont également été réalisés.
Évolutions de la mémoire et des fonctions cognitives
Après deux semaines, les personnes du groupe stimulation active ont montré des gains nets sur l’ensemble des capacités cognitives, mesurés par le Mini‑Mental State Examination, un test cognitif standard. L’amélioration était de taille modérée et particulièrement visible dans les scores de mémoire à court terme et dans un test d’apprentissage verbal qui évalue la capacité à retenir des listes de mots. Ces bénéfices mnésiques étaient encore présents 10 semaines plus tard. En revanche, le groupe simulé n’a pas montré d’amélioration à court terme et, au dernier suivi, leurs scores globaux s’étaient détériorés, conformément à la progression habituelle de la maladie d’Alzheimer. D’autres mesures — comme l’humeur, les activités quotidiennes et la charge pesant sur les aidants — n’ont pas montré de changements marqués, ce qui suggère que l’impact principal de ce programme bref ciblait des systèmes mnésiques spécifiques plutôt que tous les aspects de la vie avec une démence.
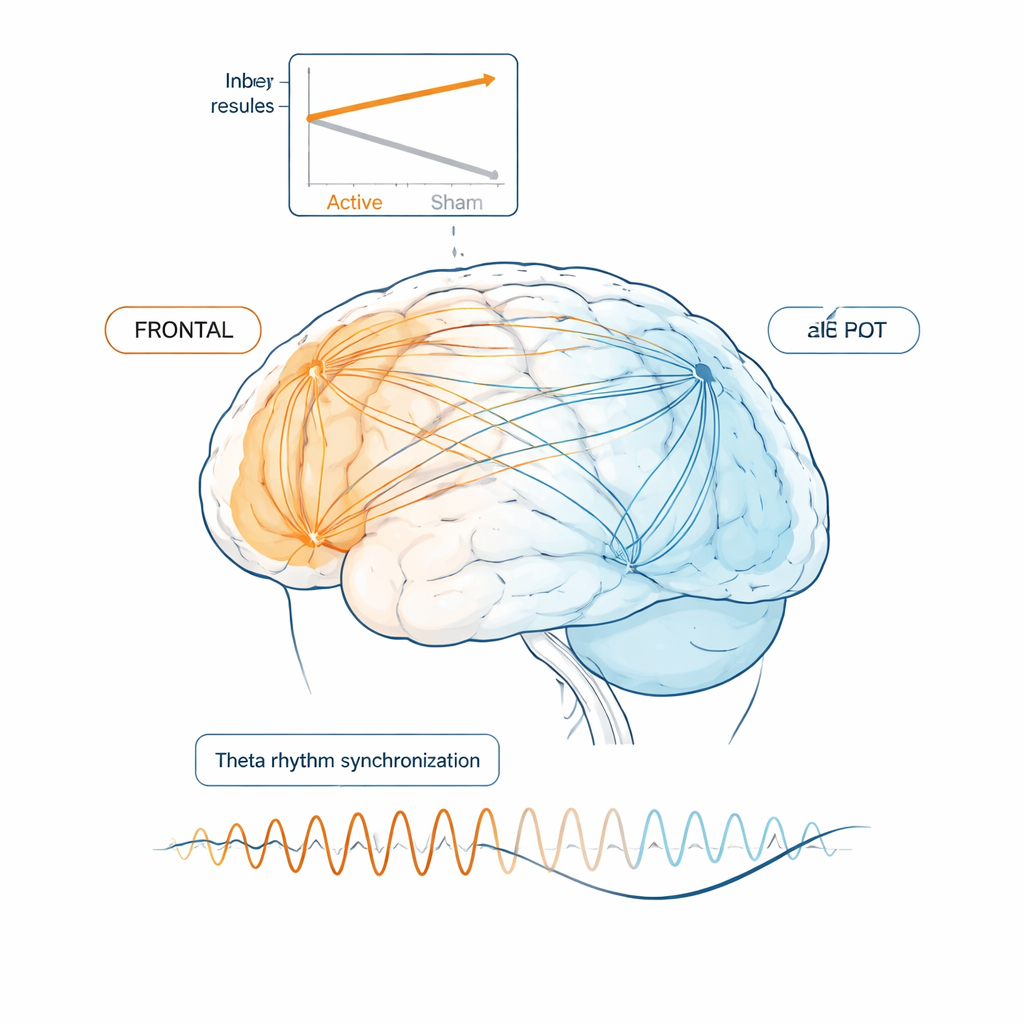
Ce qui se passait à l’intérieur du cerveau
Les enregistrements EEG ont permis d’observer comment les réseaux électriques cérébraux étaient modifiés. Dans le groupe actif, on a observé une baisse notable de l’activité « gamma » rapide (environ 32–40 cycles par seconde) dans les régions frontales et temporales après le traitement. Parallèlement, la force des connexions plus lentes en bande thêta entre ces régions a diminué. Fait surprenant, une connectivité moindre s’est avérée bénéfique : dans le groupe actif, les personnes dont les connexions thêta frontotemporales se sont le plus atténuées ont eu tendance à présenter les plus fortes améliorations aux tests. Le groupe simulé, quant à lui, a montré un schéma souvent observé en début de maladie d’Alzheimer — augmentation de la puissance gamma et renforcement de la connectivité thêta — interprété comme la tentative stressée du cerveau de compenser en travaillant davantage mais moins efficacement.
Ce que cela pourrait signifier pour les soins futurs
Dans l’ensemble, ces résultats suggèrent que le réaccordage doux des rythmes cérébraux avec une tACS en fréquence thêta, surtout lorsqu’il est associé à un entraînement mnésique ciblé, peut aider à normaliser des réseaux hyperactifs dans la maladie d’Alzheimer légère. Plutôt que de simplement augmenter l’activité, l’approche semble réduire les signaux bruités et inefficaces entre des régions clés de la mémoire et, ce faisant, soutenir la mémoire à court terme et la mémoire de travail pendant au moins plusieurs semaines. Il s’agissait d’une petite étude pilote avec de nombreux patients perdus de vue, donc des essais plus larges et plus longs sont nécessaires. Néanmoins, ce travail ouvre la voie à un avenir où « l’accordage » non invasif du cerveau pourrait compléter les médicaments, offrant aux personnes atteintes d’Alzheimer précoce un outil supplémentaire et à faible risque pour préserver leurs capacités cognitives plus longtemps.
Citation: Gong, Q., Fu, X., Feng, D. et al. Randomized, double-blind, sham-controlled pilot trial of theta-band transcranial alternating current stimulation during cognitive training in mild Alzheimer’s disease. Transl Psychiatry 16, 57 (2026). https://doi.org/10.1038/s41398-026-03822-z
Mots-clés: Maladie d’Alzheimer, stimulation cérébrale, entraînement de la mémoire, EEG, déclin cognitif