Clear Sky Science · fr
Le récepteur de l’histamine H3 comme cible pour le trouble de consommation d’alcool : remettre en question la prévisibilité des modèles animaux pour la traduction clinique en développement de médicaments
Pourquoi cette recherche compte pour la vie quotidienne
Le trouble de consommation d’alcool touche des millions de personnes dans le monde, pourtant les médicaments disponibles n’aident qu’une fraction de celles qui en ont besoin. Cet article retrace le parcours complet d’un candidat-médicament prometteur, BP1.3656B, du laboratoire aux essais humains. Il montre comment une idée qui fonctionne parfaitement chez l’animal peut échouer chez l’être humain — et pourquoi cet écart importe pour quiconque espère de meilleurs traitements contre l’alcoolisme problématique.
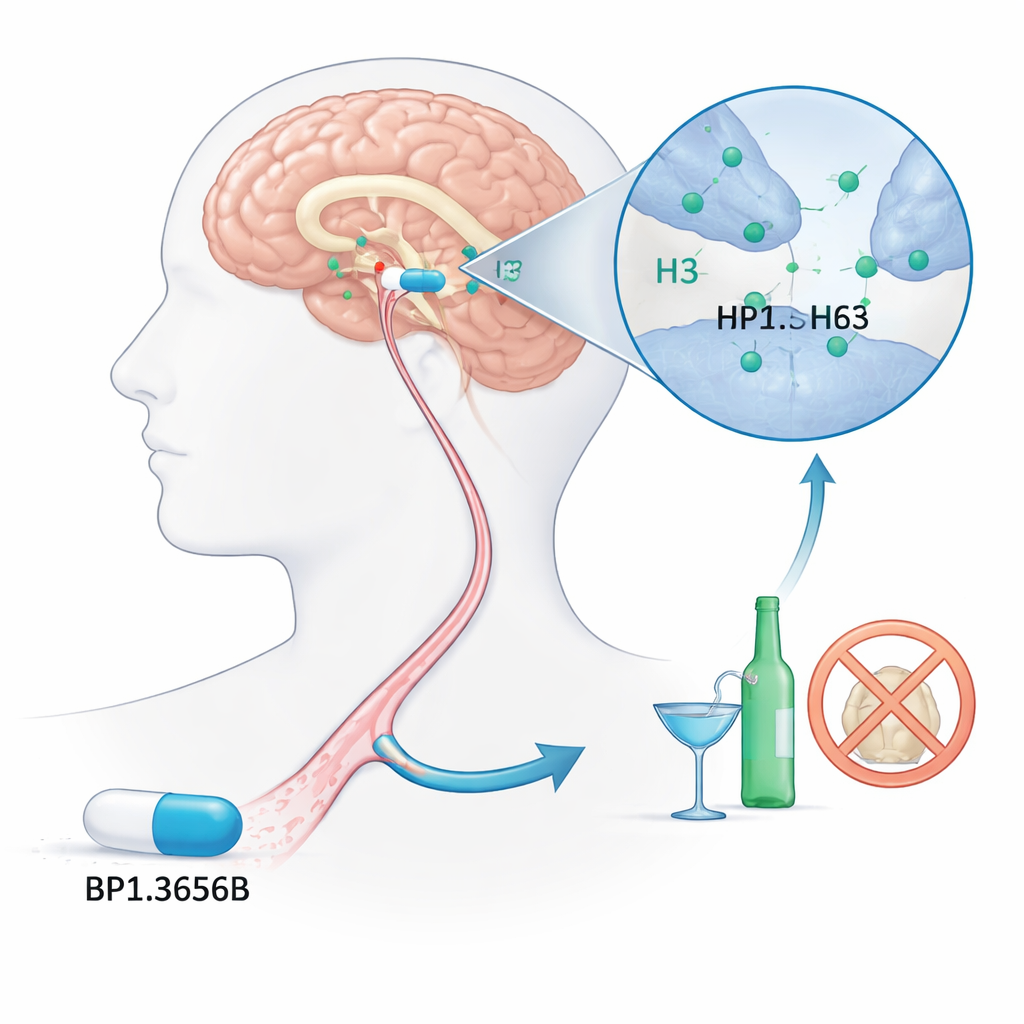
Une nouvelle cible cérébrale pour la consommation problématique
Les chercheurs se sont intéressés à un interrupteur cérébral peu connu : le récepteur de l’histamine H3. L’histamine est surtout connue pour son rôle dans les allergies, mais dans le cerveau elle contribue à réguler l’éveil et la communication entre neurones. Le récepteur H3 fonctionne comme un variateur, diminuant la libération d’histamine et de plusieurs autres messagers chimiques impliqués dans la récompense et la motivation. Parce que l’alcool interagit fortement avec ces systèmes cérébraux, les scientifiques ont longtemps supposé que bloquer les récepteurs H3 pourrait réduire l’envie de boire. BP1.3656B a été conçu comme un bloqueur puissant du H3, dans l’espoir qu’il puisse atténuer l’attraction de l’alcool sur les circuits de récompense du cerveau.
De la chimie aux réussites animales
Aux premiers essais, BP1.3656B a montré le profil dont rêvent les développeurs de médicaments. Il se liait de façon très forte et sélective au récepteur H3, pénétrait bien dans le cerveau et semblait sûr dans les tests standards de laboratoire. Chez la souris, le médicament réduisait l’explosion d’activité qui suit normalement une prise d’alcool et diminuait modestement la consommation excessive dans un test dit « drinking in the dark ». Chez le rat entraîné à appuyer sur un levier pour obtenir de l’alcool, BP1.3656B réduisait fortement la quantité bue et l’effort consenti pour obtenir de l’alcool, tant chez les gros consommateurs que chez les animaux rendus dépendants. Il atténuait aussi la reprise de consommation et diminuait l’anxiété liée au sevrage alcoolique. Pris ensemble, ces résultats suggéraient que le médicament pouvait réduire la motivation pour l’alcool et aider à prévenir le retour à une consommation excessive.
Premiers essais chez l’humain : le médicament atteint‑il sa cible ?
Viennent ensuite des études de phase I chez des volontaires sains. Des doses uniques et répétées allant jusqu’à 90 microgrammes ont été généralement bien tolérées, avec principalement des effets secondaires légers liés au sommeil, compatibles avec la nature éveillante des bloqueurs de H3. Les mesures sanguines ont montré un schéma clair et prévisible d’absorption et d’élimination du médicament. Pour vérifier qu’il atteignait bien sa cible dans le cerveau humain vivant, l’équipe a utilisé la tomographie par émission de positons, un type d’imagerie cérébrale capable de montrer le pourcentage de récepteurs occupés par un médicament. Même des doses relativement faibles de BP1.3656B bloquaient la plupart des récepteurs H3 dans plusieurs régions cérébrales importantes pour la motivation et la récompense, confirmant que, biologiquement, le médicament faisait ce pour quoi il avait été conçu.
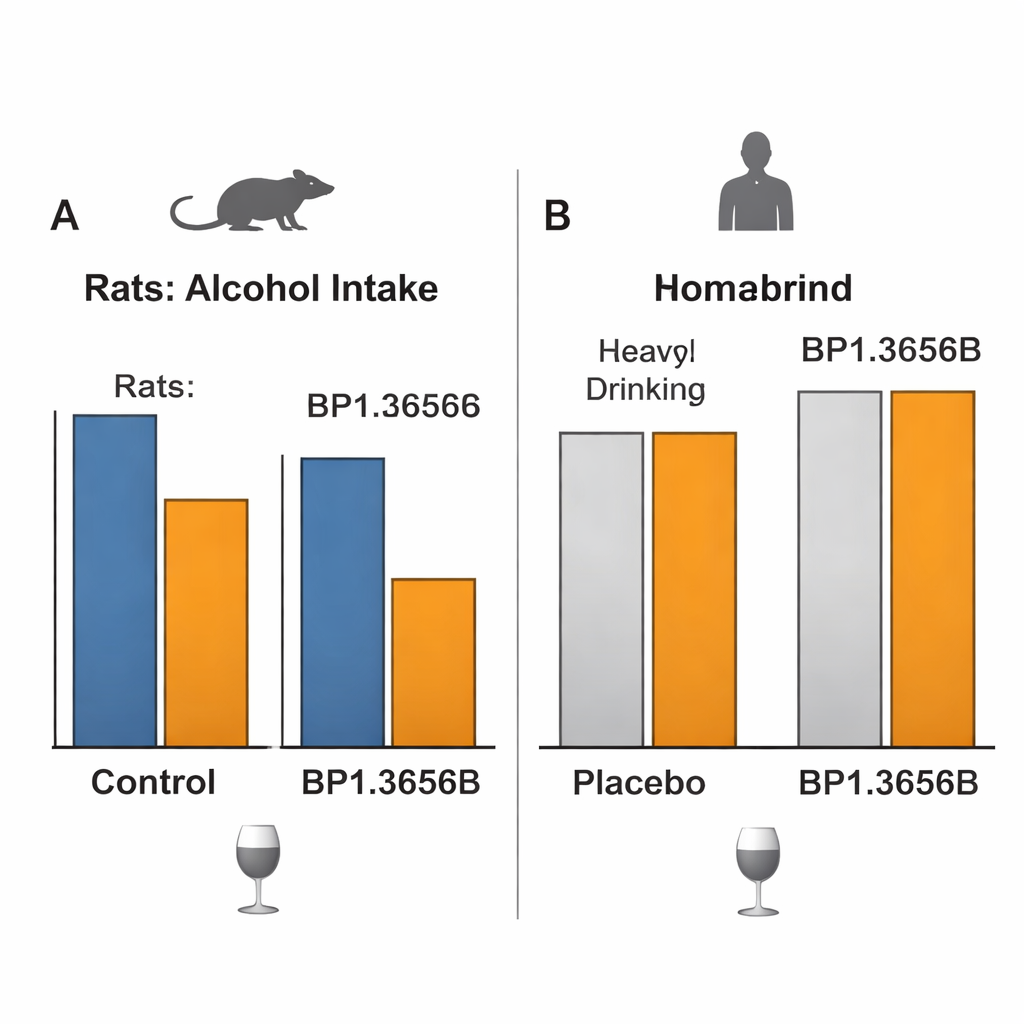
Quand des résultats prometteurs chez l’animal ne se traduisent pas chez l’homme
La question cruciale était de savoir si tout cela se traduirait par des changements significatifs de la consommation chez des personnes atteintes d’un trouble de consommation d’alcool. Dans une étude de laboratoire soigneusement contrôlée, des adultes ayant des problèmes d’alcool mais ne recherchant pas de traitement ont reçu BP1.3656B ou un placebo puis participé à des sessions où ils pouvaient s’administrer eux‑mêmes de l’alcool par voie intraveineuse en appuyant sur un bouton, dans des conditions conçues pour mesurer à la fois le plaisir et la motivation. Le médicament n’a eu aucun effet détectable sur la quantité d’alcool qu’ils choisissaient de recevoir. Un essai clinique plus vaste, de 12 semaines et multicentrique, chez des patients en recherche de traitement a ensuite testé trois doses quotidiennes de BP1.3656B contre placebo. Tous les groupes, y compris le placebo, ont considérablement réduit le nombre de jours de forte consommation et l’apport global en alcool au fil du temps, mais le médicament n’a dépassé le placebo sur aucune mesure majeure de consommation ou de craving, malgré une bonne tolérance et une occupation claire de la cible.
Ce que cela signifie pour les traitements futurs
Pour un lecteur non spécialiste, la conclusion est sobre mais importante : un médicament qui paraissait excellent en cellules, chez la souris et le rat — et qui atteignait clairement sa cible dans le cerveau humain — n’a pas aidé les personnes à boire moins. Cela ne signifie pas que la science était erronée, mais souligne l’imprévisibilité de la traduction des résultats animaux aux résultats humains. Les auteurs soutiennent que des études humaines en laboratoire, de petite taille et en phase précoce, qui testent directement l’impact d’un médicament sur la consommation d’alcool, devraient être utilisées plus systématiquement pour « réduire le risque » avant d’engager des essais coûteux et de grande envergure. Autrement dit, ce travail montre que nous avons besoin non seulement de nouvelles idées de médicaments, mais aussi de meilleures façons de décider lesquelles ont réellement une chance d’aider les personnes aux prises avec un trouble de consommation d’alcool.
Citation: Le Foll, B., Naassila, M., Jeanblanc, J. et al. Histamine H3 Receptor as a target for alcohol use disorder: challenging the predictability of animal models for clinical translation in drug development. Transl Psychiatry 16, 55 (2026). https://doi.org/10.1038/s41398-026-03807-y
Mots-clés: trouble de consommation d’alcool, récepteur de l’histamine H3, BP1.3656B, traitement de la dépendance, recherche translationnelle