Clear Sky Science · fr
La dédifférenciation des cellules de Schwann induite par la prostaglandine E2 entraîne l’invasion périneurale dans l’adénocarcinome canalaire pancréatique
Quand le cancer progresse le long des nerfs
Le cancer du pancréas est notoirement mortel, en partie parce qu’il ne se contente pas de croître en masse — il se propage souvent en rampant le long des nerfs voisins, un processus appelé invasion périneurale. Cette voie cachée est associée à la douleur, à une dissémination plus précoce et à une moins bonne survie, mais les cliniciens manquent encore d’outils efficaces pour la prévoir ou la bloquer. L’étude résumée ici révèle comment les tumeurs pancréatiques « reprogramment » chimiquement les cellules de soutien autour des nerfs, les transformant en complices actifs qui facilitent l’invasion des cellules cancéreuses. Comprendre ce partenariat nerf–tumeur pourrait ouvrir de nouvelles stratégies pour soulager la douleur et ralentir la progression de la maladie.
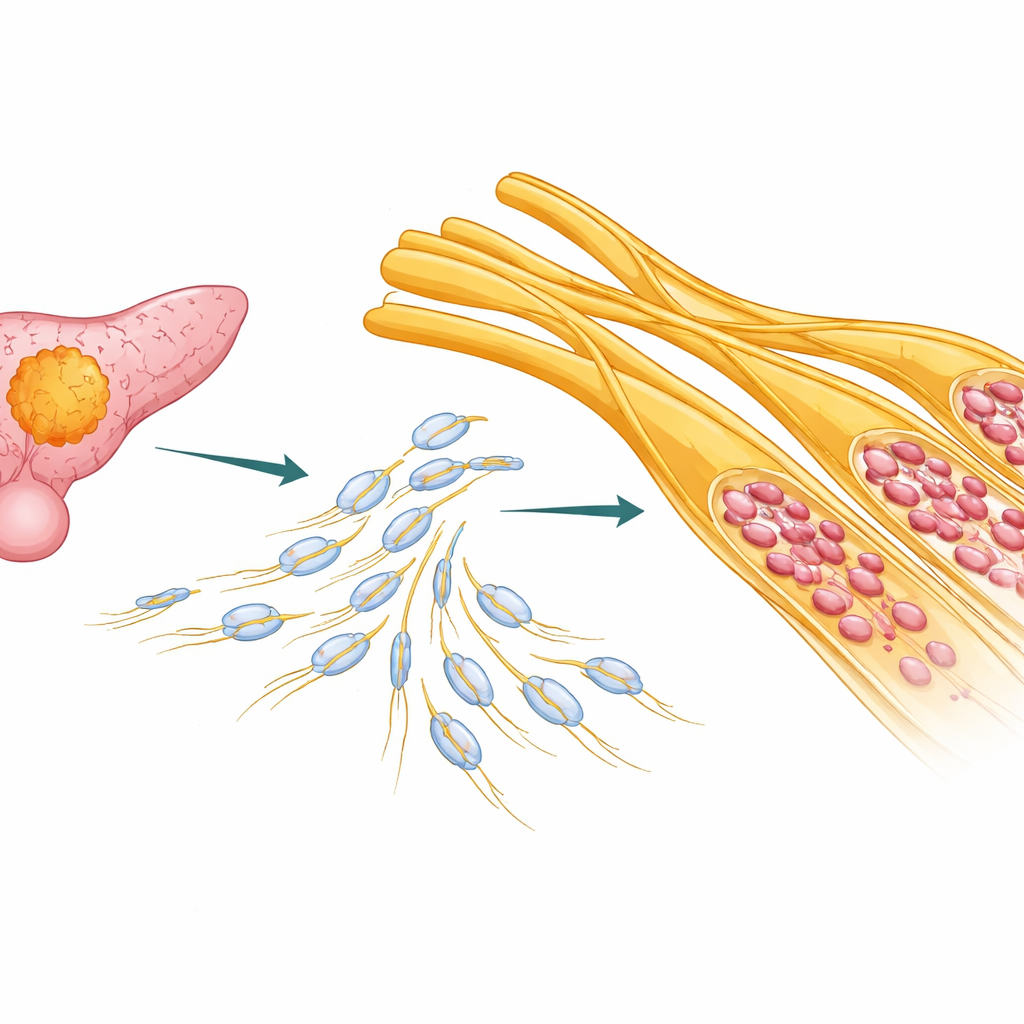
Des voies cachées à l’intérieur du pancréas
Chez de nombreux patients atteints d’adénocarcinome canalaire pancréatique, les cellules cancéreuses ne se contentent pas de s’étendre dans les tissus voisins : elles s’enroulent autour des nerfs et circulent le long d’eux. Les auteurs ont analysé des échantillons tumoraux et des ensembles de données publiques concernant plus d’une centaine de patients. Ils ont observé que les patients présentant une invasion nerveuse plus sévère avaient tendance à avoir de moins bons résultats, en particulier dans les sous‑types moléculaires moins agressifs du cancer du pancréas. Cela suggère que l’invasion périneurale n’est pas seulement un effet secondaire, mais un moteur significatif de la progression de la maladie qui devrait guider la stratification du risque et le traitement des patients.
Des cellules de soutien qui changent de camp
Les nerfs sont entourés et protégés par les cellules de Schwann, un type de cellule de soutien qui aide aussi les nerfs à se réparer après une blessure. Dans les tissus de cancer pancréatique, les chercheurs ont utilisé le séquençage ARN avancé, la transcriptomique spatiale et l’analyse unicellulaire pour cartographier la position des différents types cellulaires et les gènes qu’ils expriment. Ils ont découvert qu’une forme particulière de cellule de Schwann — ressemblant à l’état de « réparation » observé après une lésion nerveuse — se concentrerait précisément dans les régions où les nerfs étaient envahis par la tumeur. Ces cellules présentaient des signes de dédifférenciation : elles perdaient leur rôle isolant habituel pour devenir allongées, mobiles et très actives, exprimant des marqueurs tels que p75NTR, SOX2 et c‑Jun.
Un signal chimique de la tumeur vers le nerf
Pour déterminer ce qui pousse les cellules de Schwann à adopter cet état pro‑invasion semblable à la réparation, l’équipe a cultivé des cellules cancéreuses du pancréas avec des cellules de Schwann dans des systèmes de coculture en laboratoire. Ils ont constaté que les cellules tumorales augmentaient la mobilité des Schwann, modifiaient leur morphologie et activaient des gènes de dédifférenciation. Des analyses génétiques multicouches ont désigné une enzyme tumorale comme un coupable clé : PTGES, qui produit le messager lipidique prostaglandine E2 (PGE2). PTGES était particulièrement abondante dans les régions tumorales proches des nerfs envahis, et les niveaux de PGE2 augmentaient lorsque cellules cancéreuses et cellules de Schwann étaient mises en coculture. Lorsque les chercheurs bloquaient PTGES avec un inhibiteur de petite molécule ou l’abrogeaient génétiquement, les niveaux de PGE2 chutaient et les cellules de Schwann étaient beaucoup moins susceptibles de s’activer et de migrer.

Comment les cellules reprogrammées ouvrent la voie
L’ajout de PGE2 purifiée directement aux cellules de Schwann les a amenées à adopter les formes allongées et bipolaires typiques de l’état de réparation et à augmenter l’expression des marqueurs de dédifférenciation. Dans des cultures tridimensionnelles, ces cellules modifiées s’étiraient en direction des amas de cellules pancréatiques et des structures ressemblant à des nerfs, construisant de fait des « pistes » cellulaires qui guidaient les cellules tumorales. En regardant de plus près, les scientifiques ont trouvé que les cellules de Schwann stimulées par la PGE2 sécrétaient de fortes quantités de deux protéines clés : le facteur inhibiteur des leucémies (LIF), qui favorise la croissance et le remodelage nerveux, et ADAMTS‑1, une enzyme qui aide à dégrader la matrice extracellulaire environnante. Conjugués, ces facteurs sécrétés amincissaient les barrières physiques autour des nerfs et stimulaient la néo‑pousse nerveuse, créant des chemins assouplis et remodelés que les cellules cancéreuses pouvaient facilement emprunter.
Transformer le mécanisme en pistes thérapeutiques
Les expériences animales ont conforté ce schéma : lorsque les cellules cancéreuses du pancréas avaient d’abord été « pré‑conditionnées » par des cellules de Schwann, les tumeurs étaient plus volumineuses et provoquaient davantage de lésions nerveuses et de faiblesse des membres chez la souris. Des traitements bloquant PTGES ou neutralisant LIF ont réduit la charge tumorale, diminué l’invasion nerveuse et amélioré la fonction nerveuse, tout en préservant l’isolation nerveuse à l’examen histologique. Le modèle global qui émerge est une boucle paracrine : les tumeurs pancréatiques libèrent de la PGE2, qui reprogramme les cellules de Schwann en un état de réparation propice à l’invasion ; ces cellules sécrètent ensuite LIF et ADAMTS‑1, remodelent les nerfs et les tissus environnants et préparent la voie à la dissémination tumorale le long des nerfs. Pour les patients, ces travaux suggèrent que des médicaments ciblant l’axe PTGES–PGE2–cellules de Schwann, ou bloquant LIF, pourraient un jour aider à freiner l’invasion nerveuse, soulager la douleur et ralentir la progression du cancer du pancréas.
Citation: Wang, L., Liu, Q., Zhang, Z. et al. Prostaglandin E2-driven dedifferentiation of Schwann cells leads to perineural invasion in pancreatic ductal adenocarcinoma. Sig Transduct Target Ther 11, 122 (2026). https://doi.org/10.1038/s41392-026-02648-x
Mots-clés: cancer du pancréas, invasion périneurale, cellules de Schwann, prostaglandine E2, microenvironnement tumoral